| Autor |
Nachricht |
Cloud
Gast
|
 Cloud Verfasst am: 28. Mai 2006 15:51 Titel: Druck in einer Kugel und Zylinder Cloud Verfasst am: 28. Mai 2006 15:51 Titel: Druck in einer Kugel und Zylinder |
 |
|
guten tag,
ich wollte frage, wie man den Luftdruck in einer Kugel und in einem Zylinder (welche beide verschlossen sind) berechnen?
Dabei ist es auch wichtig zu wissen, dass sich dabei die temperatur ändert, folglich auch der Druck. und wie kann man dann den druck in einer glaskugel ermitteln?
vielen dank für eure tipps/hilfe |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 28. Mai 2006 16:05 Titel: dermarkus Verfasst am: 28. Mai 2006 16:05 Titel: |
 |
|
|
Normalerweise geht das prima mit der idealen Gasgleichung. Dass der Behälter kugelförmig oder zylinderförmig ist, brauchst du dabei für die Bestimmung des Volumens. |
|
 |
Nikolas
Ehrenmitglied

Anmeldungsdatum: 14.03.2004
Beiträge: 1873
Wohnort: Freiburg im Brsg.
|
 Nikolas Verfasst am: 28. Mai 2006 16:08 Titel: Nikolas Verfasst am: 28. Mai 2006 16:08 Titel: |
 |
|
Für eine konstante Temperatur wird die die allgemeine Zustandsgleichung weiterhelfen, oder für ein nicht-ideales Gas das Van-Der-Waals Gesetz [Wikipedia]. Wenn du jetzt bei konstantem Volumen die Temperatur änderst, wird sich der Druck proportional zur Termperaturänderung verhalten.
[ Gesetz von Amontons oder 2. Gesetz von Gay-Lussac]
Den Druck direkt zu messen wird ohne Drucksonde kaum möglich sein, ausser vielleicht über exotische Möglichkeiten wie die Kugel in Schwingungen zu versetzen, die je nach Innendruck verschieden sind.
_________________
Nikolas, the mod formerly known as Toxman.
Erwarte das Beste und sei auf das Schlimmste vorbereitet. |
|
 |
Cloud
Gast
|
 Cloud Verfasst am: 28. Mai 2006 16:24 Titel: Cloud Verfasst am: 28. Mai 2006 16:24 Titel: |
 |
|
ok, dass gesetz von gay lussac lautet ja folgendermaßen:
)
und was ist hier  ? Und T ist dann die Temperatur die dadrinnen herrscht ? ? Und T ist dann die Temperatur die dadrinnen herrscht ?
und 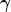 , wie bekomme ich den raus? das ist doch der volumenausdehnungskoeffizient oder? glaub ich, bin mir da aber nicht so sicher. kann ich den auch berechnen, wenn ich nur das Volumen und Temperatur als vorhandene größen habe? , wie bekomme ich den raus? das ist doch der volumenausdehnungskoeffizient oder? glaub ich, bin mir da aber nicht so sicher. kann ich den auch berechnen, wenn ich nur das Volumen und Temperatur als vorhandene größen habe?
danke
 |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 28. Mai 2006 17:01 Titel: dermarkus Verfasst am: 28. Mai 2006 17:01 Titel: |
 |
|
Ich hätte jetzt zunächst mal einfach
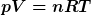
hergenommen. Welche Angaben hast du denn, was kannst du messen, welche experimentelle Situation hast du konkret, und was möchtest du konkret ausrechnen? |
|
 |
Cloud
Gast
|
 Cloud Verfasst am: 28. Mai 2006 17:35 Titel: Cloud Verfasst am: 28. Mai 2006 17:35 Titel: |
 |
|
naja, also ich habe folgend daten:
den äußeren luftdruck 747 Torr
den durchmesser der kugel 4,1 cm
und die dazugehörige Temperatur. einmal 0°C , Raumtemperatur und ca. 97,5 °C
und das Volumen dieser Kugel bleibt konstant. denn sie ist abgeschottet durch Quecksilber.
naja, und da müsste ich jetzt von den druck in der Glaskugel berechnen. und die ideale gasgleichung kann ich doch nicht nehmen. denn es ist ja luft in der glaskugel. also kein ideales gas.
oder ist das in diesem zusammenhang etwas egal? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 28. Mai 2006 17:45 Titel: dermarkus Verfasst am: 28. Mai 2006 17:45 Titel: |
 |
|
Was meinst du mit "abgeschottet" durch Quecksilber? Gibt es zwischen der Luft in der Glaskugel und der Außenluft eine Verbindung, die nur aus Quecksilber besteht? Falls ja, dann habe ich den Verdacht, dass da an der Glaskugel eine Art Barometer hängt, vielleicht ein U-Rohr mit Quecksilber drin?
Dann hätte sich eine deiner Fragen schon gelöst, denn an der Höhe der Quecksilbersäule rechts und links im U-Rohr kannst du die Druckdifferenz zwischen der Luft in der Glaskugel und der Außenluft ablesen.
Außerdem glaube ich, dass sich die Luft in deinem Versuchsaufbau in sehr guter Näherung als ideales Gas rechnen und beschreiben lässt. Wie sieht dein Versuchsaufbau genau aus? |
|
 |
Cloud
Gast
|
 Cloud Verfasst am: 28. Mai 2006 17:53 Titel: Cloud Verfasst am: 28. Mai 2006 17:53 Titel: |
 |
|
also, dass ist im prinzip so ein typisches gasthermometer.
aber wie kann ich die druckdifferenz anhand des höhenunterschied angeben? solch eine formel die nur aus diesen komponenten höhe besteht, woraus man den druck angeben kann, habe ich glaube bisher noch nicht gesehen.
aber wenn du meinst, man könnte die luft als ideales gas ansehen. dann kann man ja doch das gesetz von gay lussac anwenden oder? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 28. Mai 2006 18:03 Titel: dermarkus Verfasst am: 28. Mai 2006 18:03 Titel: |
 |
|
Also so ein Gasthermometer, bei dem die Höhendifferenz der Quecksilbersäulen anzeigt, wie warm das Gas ist?
Das Stück Quecksilbersäule, das auf der einen Seite mehr vorhanden ist als auf der anderen, erzeugt eine Druckdifferenz (in Torr gemessen), die der Höhendifferenz in mm Quecksilber entspricht. Das ist ja gerade die Definition der Druckeinheit Torr.
Du kannst das hier mit dem Gesetz von Gay-Lussac rechnen. Ich hätte jetzt allerdings einfach das ideale Gasgesetz verwendet und daraus gefolgert, dass das Verhältnis von Druck 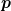 und Temperatur und Temperatur 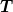 bei der Erwärmung konstant bleibt, weil sich das Volumen in guter Näherung nicht ändert. Dann ist die Rechnung noch einfacher und kürzer. bei der Erwärmung konstant bleibt, weil sich das Volumen in guter Näherung nicht ändert. Dann ist die Rechnung noch einfacher und kürzer. |
|
 |
|
















