| Autor |
Nachricht |
Mr. Sheesha
Anmeldungsdatum: 01.09.2007
Beiträge: 5
|
 Mr. Sheesha Verfasst am: 01. Sep 2007 17:30 Titel: Additivität der Partialdrücke & partielle Ableitungen Mr. Sheesha Verfasst am: 01. Sep 2007 17:30 Titel: Additivität der Partialdrücke & partielle Ableitungen |
 |
|
Hallo an Alle,
Ich habe eine Frage zur reversiblen adiabatischen Entmischung (Stoffe sind chemisch inert, es finden also keine Reaktionen statt).
Dort gilt laut Skript:
=\sum_{i=1}^r p_i(T,V,N_i))
=\sum_{i=1}^r G_i(T,p_i,N_i))
und
)
p ist der Druck der Mischung, die 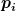 die Partialdrücke der einzelnen Komponenten, ebenso für G (Gibbs'sche freie Energie). N steht für die Teilchen- bzw. Molzahl. Aus der Additivität kann man jetzt für die chemischen Potentiale folgern: die Partialdrücke der einzelnen Komponenten, ebenso für G (Gibbs'sche freie Energie). N steht für die Teilchen- bzw. Molzahl. Aus der Additivität kann man jetzt für die chemischen Potentiale folgern:
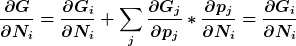
Wieso ergibt denn die Summe 0? Es ist mir klar dass alle Summanden mit  Null sind da Null sind da 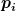 für für ) nicht von nicht von  abhängt, aber der i-te Summand - also abhängt, aber der i-te Summand - also  müsste doch ungleich Null sein, oder macht man hier was ganz anderes? Hoffe es kann mir jemand helfen. müsste doch ungleich Null sein, oder macht man hier was ganz anderes? Hoffe es kann mir jemand helfen.
Liebe Grüsse
Mr. Sheesha |
|
 |
magneto42
Anmeldungsdatum: 24.06.2007
Beiträge: 854
|
 magneto42 Verfasst am: 01. Sep 2007 23:28 Titel: magneto42 Verfasst am: 01. Sep 2007 23:28 Titel: |
 |
|
Hallo Mr. Sheesha.
| Mr. Sheesha hat Folgendes geschrieben: | Aus der Additivität kann man jetzt für die chemischen Potentiale folgern:
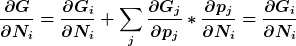 |
Bist Du sicher, daß das stimmt? Wenn ich Deine Angaben verwende, würde ich intuitiv folgendes rechnen:
}{\partial N_i} = \frac{\partial }{\partial N_i} \sum_{j=1}^r G_j(T,p_j,N_j) = \sum_{j=1}^r \frac{\partial G_j(T,p_j,N_j)}{\partial N_i} = \sum_{j=1}^r \frac{\partial G_j(T,p_j,N_j)}{\partial p_j} \cdot \frac{\partial p_j}{\partial N_i})
Im Vergleich mit deiner Gleichung fehlt mir damit ein Term. Bin ich damit auf dem Holzweg? Habe ich jetzt etwas übersehen oder hast Du diesen Term zweimal gezählt  ? ? |
|
 |
Mr. Sheesha
Anmeldungsdatum: 01.09.2007
Beiträge: 5
|
 Mr. Sheesha Verfasst am: 02. Sep 2007 00:15 Titel: Mr. Sheesha Verfasst am: 02. Sep 2007 00:15 Titel: |
 |
|
Hi Magneto,
Danke dir erst mal für die Antwort. Ich denke die Antwort auf deine Frage ist nein. Da wurde einfach die verallgemeinerte Kettenregel verwendet, also im Stil von:
Sei  = x(y, w(y,z))) . Dann gilt: . Dann gilt:
_z =( \frac{\partial x}{\partial y})_w +(\frac{\partial x}{\partial w})_y*(\frac{\partial w}{\partial y})_z)
(Die Variable im Index wird bei der partiellen Ableitung festgehalten)
Und ist ist es ja dasselbe da die Gibbs'sche freie Energie G(T,p,N) eine Funktion des Druckes ist und dieser wiederum von der Teilchen- bzw. Molzahl abhängt. Es muss was anderes sein, aber ich komme leider auch nach längerem studieren nicht drauf warum die angesprochene Summe Null ergibt.
Liebe Grüsse
Sheesha |
|
 |
magneto42
Anmeldungsdatum: 24.06.2007
Beiträge: 854
|
 magneto42 Verfasst am: 02. Sep 2007 00:50 Titel: magneto42 Verfasst am: 02. Sep 2007 00:50 Titel: |
 |
|
| hat Folgendes geschrieben: | | Und ist ist es ja dasselbe da die Gibbs'sche freie Energie G(T,p,N) eine Funktion des Druckes ist und dieser wiederum von der Teilchen- bzw. Molzahl abhängt |
Stimmt, hier war mein Denkfehler, danke  . Mein Buch gibt dafür an (edit: für ein ideales Gas): . Mein Buch gibt dafür an (edit: für ein ideales Gas):

Ich werde wohl auch noch ein bischen herumpuzzeln müssen  ... ... |
|
 |
Mr. Sheesha
Anmeldungsdatum: 01.09.2007
Beiträge: 5
|
 Mr. Sheesha Verfasst am: 02. Sep 2007 01:23 Titel: Mr. Sheesha Verfasst am: 02. Sep 2007 01:23 Titel: |
 |
|
|
Wär super wenn dir noch was einfällt, ich schlag mich schon seit Tagen damit rum. Wahrscheinlich ist es was ganz einfaches und ich komm einfach nicht drauf. |
|
 |
schnudl
Moderator

Anmeldungsdatum: 15.11.2005
Beiträge: 6979
Wohnort: Wien
|
 schnudl Verfasst am: 02. Sep 2007 22:12 Titel: Re: Additivität der Partialdrücke & partielle Ableitunge schnudl Verfasst am: 02. Sep 2007 22:12 Titel: Re: Additivität der Partialdrücke & partielle Ableitunge |
 |
|
Bei nur einer Teilchensorte lautete deine Gleichung, da
 = G_1(T, P, N))

Unabhängig vom physikalischen Hintergrund kann doch da was mit der Notation nicht stimmen, oder ? Bringst Du da nicht totale und partielle Ableitung durcheinander oder sonst was ?
Ich kenne den Prozess dahinter zwar nicht, aber was ist mit der Temperatur ?
_________________
Wenn du eine weise Antwort verlangst, musst du vernünftig fragen (Goethe) |
|
 |
Mr. Sheesha
Anmeldungsdatum: 01.09.2007
Beiträge: 5
|
 Mr. Sheesha Verfasst am: 03. Sep 2007 00:24 Titel: Mr. Sheesha Verfasst am: 03. Sep 2007 00:24 Titel: |
 |
|
Hallo schnudl,
Ja bei nur einer Teilchensorte würde es so stehen wie du es geschrieben hast. Ich glaube schon dass ich das richtig aufgeschrieben habe, denn wir leiten ja hier nur partiell nach der Teilchenzahl ab und die totale Ableitung wäre eine Ableitung nach allen Variablen, also auch nach T und p. Die Summe in der Formel tritt auf, weil der Druck ebenfalls von der Teilchenzahl abhängt (wir benutzen also die verallgemeinerte Kettenregel, wie oben beschrieben).
Zu deiner Frage zum Prozess: es handelt sich um eine ideale Mischung beliebiger chemisch inerter Stoffe (also keine Reaktionen) und der Vorgang der Mischung verläuft isotherm.
mfg
Sheesha |
|
 |
schnudl
Moderator

Anmeldungsdatum: 15.11.2005
Beiträge: 6979
Wohnort: Wien
|
 schnudl Verfasst am: 03. Sep 2007 07:14 Titel: schnudl Verfasst am: 03. Sep 2007 07:14 Titel: |
 |
|
Bei einem Satz von Zustandsvariablen (T, P, N) ist die partielle Ableitung von G(T, P, N) nach N wohldefiniert. Wieso soll noch da noch ein Term dazukommen, wenn man schon nach N abgeleitet hat und die Ableitung schon dort steht?
Die "Gleichung" für n=1 führt das ja schon ad absurdum...(sorry, aber ich muss es klar sagen)
Was möchtest du denn eigentlich zeigen ? 
Dass das chemische Potential die partielle Ableitung der freien Entalpie bei festgehaltenem T und P ist, kann man anders zeigen und hat auch nichts mit einer adiabatischen Entmischung zu tun.
Das ideale Gas hat z.B. die Freie Entalphie
 = NkT \big(1-\ln(\alpha T^{5/2}/P) \big) )
Daher
}{\partial N} = kT = \mu)
Was du machst, ist, dass du nun sagst, dass bei einer Änderung von N sich auch P ändert. ZB wäre es denkbar, für das ideale Gas eine isochor/isotherme Zustandsänderung zu haben, wo sich aufgrund der Änderung von N auch P ändert, gemäss

Daher könnte man nun geneigt sein,
 = N/C )
als zusätzliche Änderungsmöglichkeit von G anzunehmen, und zu sagen
}{\partial N} + \frac{\partial G(T, P, N)}{\partial P} \cdot \frac{\partial P}{\partial N} = \frac{\partial G(T, P, N)}{\partial N} + \frac{\partial G(T, P, N)}{\partial P} \cdot \frac{1}{C})
Dies führt auf
 \cdot \frac{1}{C})
was aber sicher falsch ist (das chemische Potential hängt nicht von der extensiven Größe N ab), und mit der gewünschten partiellen Ableitung nichts mehr zu tun hat. Es handelt sich hier eher um eine totale Ableitung unter Berücksichtigung der Zustandsgleichung, aber dann stimmt etwas mit deiner Schreibweise nicht, wie ich schon sagte.
_________________
Wenn du eine weise Antwort verlangst, musst du vernünftig fragen (Goethe) |
|
 |
Mr. Sheesha
Anmeldungsdatum: 01.09.2007
Beiträge: 5
|
 Mr. Sheesha Verfasst am: 03. Sep 2007 13:05 Titel: Mr. Sheesha Verfasst am: 03. Sep 2007 13:05 Titel: |
 |
|
Hallo Schnudl,
Nach eingehender Ueberlegung glaube ich nun auch, dass du recht hast, und es sich um die totale Ableitung nach N bei festgehaltenem T,p handelt, also die Summe wuerde dann natuerlich gar nicht auftreten, da ja p=const. Diese Formel stand so bei uns im Skript und zwar ging es darum, den Zusammenhang zwischen den chemischen Potentialen der reinen Stoffe und denen in der Mischung aufzuzeigen.
Adiabatische Entmischung ist nur ein Beispiel eines reversiblen Prozesses. Im Skript steht, den benoetige man um auszurechnen, wie gross die Entropie in der Mischung ist (weil man dann einfach die Entropien der reinen Stoffe addieren kann). Damit wurde dann die Freie Energie in der Mischung hergeleitet und aus deren Ableitung nach dem Volumen die Additivitaet der Partialdruecke, was wiederum ergab, dass die Freie Enthalpie der Mischung sich ebenfalls als Summe der freien Enthalpien der reinen Stoffe darstellen laesst.
Eventuell habe ich hier etwas falsch verstanden und wir brauchen fuer die Herleitung des Zusammenhangs der chemischen Potentiale gar keinen reversiblen Prozess der Entmischung? Bin gerade etwas verwirrt...
Auf jeden Fall vielen Dank fuer deine Antwort, damit ist zumindest das Problem geklaert weshalb die Summe gleich Null ist.
mfg
Sheesha |
|
 |
|
















 ?
? . Mein Buch gibt dafür an (edit: für ein ideales Gas):
. Mein Buch gibt dafür an (edit: für ein ideales Gas):
 ...
...