| Autor |
Nachricht |
andyxt
Anmeldungsdatum: 31.08.2005
Beiträge: 17
|
 andyxt Verfasst am: 10. Feb 2007 00:17 Titel: Berechnung der Nutzarbeit beim Dieselkreisprozess andyxt Verfasst am: 10. Feb 2007 00:17 Titel: Berechnung der Nutzarbeit beim Dieselkreisprozess |
 |
|
Hallo,
wie kann man Die Nutzarbeit bei einem Kreisprozess berechnen?
http://de.wikipedia.org/wiki/Diesel-Prozess
Dort ist eine schöne Grafik (pV-Diagramm). Die markierte Fläche ist ja die Nutzarbeit .
Und hier ist eine Formel (plus Diagramm):
http://www.maschinenbau-fh.de/t_diesel.html
Ich verstehe die Formel bei der Nutzarbeit nicht ganz. Was bedeutet das "k"? Und wie kann man die Arbeit für die einzelnen Prozesse berechnen? So damit man zu der Endformel (wie auf der Seite kommt).
Danke im Voraus.
Gruß Andy
_________________
Zwei Dinge sind unendlich, das Universum und die menschliche Dummheit, aber bei dem Universum bin ich mir noch nicht ganz sicher.
Albert Einstein
Das, wobei unsere Berechnungen versagen, nennen wir Zufall. 
Albert Einstein |
|
 |
kommando_pimperlepim

Anmeldungsdatum: 15.11.2004
Beiträge: 133
|
 kommando_pimperlepim Verfasst am: 10. Feb 2007 13:09 Titel: ... kommando_pimperlepim Verfasst am: 10. Feb 2007 13:09 Titel: ... |
 |
|
Die Änderung der inneren Energie beim kompletten Prozess ist Null, da es ein Kreisprozess ist, der nach einem Zyklus in den Anfangszustand übergeht. Damit lautet der erste Hauptsatz: 
Oder 

Da isentropische Prozesse (auch adiabatisch genannt) ohne Wärmezufuhr sind, gilt 
Der Prozess der Wärmezufuhr findet isobar statt. Damit ist
)
Der Prozess der Wärmeabgabe findet isochor statt. Damit ist
)
Die spezifische Wärmekapazität  bei konstantem Volumen steht zu der Wärmekapazität bei konstantem Volumen steht zu der Wärmekapazität  bei konstantem Druck in der Beziehung bei konstantem Druck in der Beziehung
 Das ist eine Konstante, dabei ist Das ist eine Konstante, dabei ist 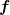 die Anzahl der Freiheitsgrade des Stoffes. Bei idealen Einatomigen Gasen ist die Anzahl der Freiheitsgrade des Stoffes. Bei idealen Einatomigen Gasen ist 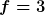 und damit und damit  Wenn du die Wärmen addierst und Wenn du die Wärmen addierst und  durch durch  ausdrückst, gelangt der sog. Adiabatenexponent ausdrückst, gelangt der sog. Adiabatenexponent 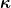 in die Gleichung. in die Gleichung. |
|
 |
andyxt
Anmeldungsdatum: 31.08.2005
Beiträge: 17
|
 andyxt Verfasst am: 11. Feb 2007 16:48 Titel: andyxt Verfasst am: 11. Feb 2007 16:48 Titel: |
 |
|
Danke erst mal für die Antwort. Sie bringt mich schon mal einen ganzes Stück weiter 
Bleibt bloß noch die Frage: Was ist der Unterschied zwischen den beiden Wärmekapazitäten (konstanter Druck und konstantes Volumen)? Wie berechnet man diese Wärmekapazitäten? Ist die Adiabatenkonstante k immer 5/3 oder hängt dies auch noch von den Freiheitsgeraden ab (oder ist das dann keine Adiabatenkonstante wenn andere Freiheitsgerade vorhanden sind)? Und was genau sagen die Freiheitsgerade aus? Irgendwie komme ich nicht mit diesem Begriff ganz klar. 
_________________
Zwei Dinge sind unendlich, das Universum und die menschliche Dummheit, aber bei dem Universum bin ich mir noch nicht ganz sicher.
Albert Einstein
Das, wobei unsere Berechnungen versagen, nennen wir Zufall. 
Albert Einstein |
|
 |
kommando_pimperlepim

Anmeldungsdatum: 15.11.2004
Beiträge: 133
|
 kommando_pimperlepim Verfasst am: 13. Feb 2007 13:19 Titel: kommando_pimperlepim Verfasst am: 13. Feb 2007 13:19 Titel: |
 |
|
Die ganze Geschichte fängt in der Definition der Temperatur an:

Die Zahl der Freiheitsgrade 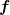 ist für ideale einatomige Gase 3 und für mehratomige Gase größer. Eine Präzise Definition kenne ich nicht. Im Physik-Grundstudium vermeiden Vorlesungen und Lehrbücher eine konkrete Definition des Begriffs bisher. Die Zahl hat aber definitiv was mit den Bewegungsmöglichkeiten der Moleküle oder Atome zu tun. Bei mehratomigen Gasen kommen mehr Freiheitsgrade dazu, weil sie die Fähigkiet haben, zu rotieren. Ich habe bisher nie verstanden, warum ein einzelnes Atom nicht rotieren kann. Aber wenn man das erstmal so hinnimmt, kann man die spezifischen wärmen berechnen. ist für ideale einatomige Gase 3 und für mehratomige Gase größer. Eine Präzise Definition kenne ich nicht. Im Physik-Grundstudium vermeiden Vorlesungen und Lehrbücher eine konkrete Definition des Begriffs bisher. Die Zahl hat aber definitiv was mit den Bewegungsmöglichkeiten der Moleküle oder Atome zu tun. Bei mehratomigen Gasen kommen mehr Freiheitsgrade dazu, weil sie die Fähigkiet haben, zu rotieren. Ich habe bisher nie verstanden, warum ein einzelnes Atom nicht rotieren kann. Aber wenn man das erstmal so hinnimmt, kann man die spezifischen wärmen berechnen.
Dafür braucht man dur die Beziehungen
) , ,
) , ,
und die universelle Gasgleichung in differentieller Form:
)
Dann kann man z. B. die spezifischen molaren Wärmekapazitäten definiert als
)
für isochore und isobare Prozesse herleiten.
isochorer Prozess:

Wegen (2) und (4) ist  und durch Kürzen ist und durch Kürzen ist 
isobarer Prozess
Wegen (3) und 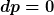 kann man (1) umschreiben zu kann man (1) umschreiben zu
 also ist also ist

und mit (2) und (4)
 und man sieht und man sieht 
Damit ist 
Mit Massenspezifischen Wärmen würde das gleiche rauskommen. Die spezifischen Wärmen hätten nur andere Vorfaktoren, die sich in 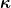 aber rauskürzen würden. aber rauskürzen würden. |
|
 |
andyxt
Anmeldungsdatum: 31.08.2005
Beiträge: 17
|
 andyxt Verfasst am: 14. Feb 2007 19:22 Titel: andyxt Verfasst am: 14. Feb 2007 19:22 Titel: |
 |
|
Danke für die Hilfe. Jetzt hab ich das verstanden. 
_________________
Zwei Dinge sind unendlich, das Universum und die menschliche Dummheit, aber bei dem Universum bin ich mir noch nicht ganz sicher.
Albert Einstein
Das, wobei unsere Berechnungen versagen, nennen wir Zufall. 
Albert Einstein |
|
 |
|
|

















