| Autor |
Nachricht |
Physinetz
Anmeldungsdatum: 20.09.2006
Beiträge: 327
|
 Physinetz Verfasst am: 05. Jan 2011 18:57 Titel: Thermodynamik: Wärme berechnen Physinetz Verfasst am: 05. Jan 2011 18:57 Titel: Thermodynamik: Wärme berechnen |
 |
|
Hallo,
habe folgende Aufgabe:
In einem Behälter befinden sich 2,5kg Nassdampf mit der Temperatur  und mit dem Volumen und mit dem Volumen  . .
Durch Berieselung mittels Wasser an der Außenwand soll der Dampf auf  gekühlt werden, die konstante spez. Wärmekapazität des Kühlwassers beträgt gekühlt werden, die konstante spez. Wärmekapazität des Kühlwassers beträgt )
a)...b)...c)... in den ersten Aufgaben wurde mittels Nassdampftabelle Dampfgehalt,und Druck im Zustand 1 und 2 berechnet:
 
d) Welche Wärme Q muss vom Behälter abgeführt werden?
Hier stehe ich ein wenig auf dem Schlauch.
Mein Ansatz:
Meiner Meinung nach bleibt das Volumen konstant (wenn ja, warum?).Es wird also keine Volumenänderungsarbeit verrichtet.
Damit reduziert sich der erste Hauptsatz der Thermodynamik 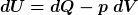 auf: auf:
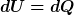
In meinem Skript finde ich nun folgende Formel:
 dv)
da sich das Volumen nicht ändert meine ich die Formel müsse sich reduzieren auf 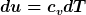 . .
Falls nun 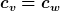 von der Bezeichnung her wäre, könnte ich das ja nun einfach einsetzen für die beiden Temperaturen. von der Bezeichnung her wäre, könnte ich das ja nun einfach einsetzen für die beiden Temperaturen.
Stimmen meine Überlegungen?
Ich könnte auch über die Enthalpien gehen, dazu habe ich auch eine Tabelle aus der ich dies herauslesen könnte, falls das auch mit Enthalpien geht?
Ich hoffe irgendjemand hat hier Ahnung von Thermodynamik
Besten Dank  |
|
 |
BbM
Gast
|
 BbM Verfasst am: 05. Jan 2011 19:23 Titel: BbM Verfasst am: 05. Jan 2011 19:23 Titel: |
 |
|
Ich habe zwar keine Ahnung
aber da gibt es doch Enthalpietabellen
Die Differenz ist dann Q |
|
 |
o~O

Anmeldungsdatum: 30.11.2010
Beiträge: 184
|
 o~O Verfasst am: 05. Jan 2011 19:55 Titel: o~O Verfasst am: 05. Jan 2011 19:55 Titel: |
 |
|
Vielleicht solltest du dir als erstmal mal den Dampfgehalt berechnen. Du weißt nur, das du Nassdampf hast, aber nicht mit welchen Parameter. Du kannst dir das spezifische Volumen ausrechnen des Nassdampfes, da du ja Masse und Volumen hast.
v = 2,5kg / 0,2m²
Nun kannst du diesen Wert in deiner Wasserdampftabelle suchen als Funktion von v=f(T1,p1), und bestimmst den Dampfanteil. Daraus
resultierend, kann dir dann auch die Enthalpie h1 rauslesen.
Selbes gilt übrigends für den Zustand 2, wobei man hier noch prüfen müsste, ob überhaupt noch Nassdampf vorliegt oder schon unterkühle Flüßigkeit. Das geht einfach dadurch, da du annimmst, das v konstant ist. Nun kannst du auch für den Zustand 2 die spezifische Enthalpie ausrechnen.
p.s. Der weg über Enthalpien ist immer besser, da cp = f(T,p) ist. Für ideale Gase ist das nicht so wild, da kann man auch ruhig mit deiner Formel rechnen, aber nimm lieber Enthalpien, besonders wenn es um Nassdampf geht. |
|
 |
Physinetz
Anmeldungsdatum: 20.09.2006
Beiträge: 327
|
 Physinetz Verfasst am: 05. Jan 2011 21:15 Titel: Physinetz Verfasst am: 05. Jan 2011 21:15 Titel: |
 |
|
Ja Dampfgehalt und alles zu bestimmen ist kein Problem.
Aber wie mache ich das dann mit der Wärme über Enthalpien? Komme irgendwie nicht auf die richtige Formel?!
Weil mit  kann ich ja nicht arbeiten, da ich keine feste Temperatur habe die ich einsetzen kann. Habe ja zwei Werte für die Temperatur, passt also nicht... kann ich ja nicht arbeiten, da ich keine feste Temperatur habe die ich einsetzen kann. Habe ja zwei Werte für die Temperatur, passt also nicht...
Ideen? |
|
 |
o~O

Anmeldungsdatum: 30.11.2010
Beiträge: 184
|
 o~O Verfasst am: 06. Jan 2011 08:31 Titel: o~O Verfasst am: 06. Jan 2011 08:31 Titel: |
 |
|
^^ Ich weiß ja, das Leute dazu neigen die kompliziertesten Formeln zu nehmen, aber auf die Differentialgleichung kannst du gut und gerne verzichten.
Überlegen wir uns das mal. Was ist Wärme ? Die einfachste definition die wir kennen ist
Q = m * CP * (T2 - T1) .
Die können wir aber nicht nehmen, da cp = f (p,T). Bedenken wir aber, das dieser Therm cp * (T2-T1) = h2 - h1 ist, geht das doch schon viel leichter.
Nun kannst du natürlich versuchen diese Therme h2 und h1 zu berechnen. Aber lass da lieber die Finger von. Das geht nur nach hinten los. Hol dir eine Wasserdampftafel, oder ein entsprechendes Programm, und berechne dir einfach h1 = f (p1,T1,x1) und h2= f (p2,T2,x2)
Wobei natürlich wenn beide im Nassdampfgebiet sind, p1 = f (T1) und T1 = f (p1) ist. Da ja bekanntlich im Nassdampfgebiet Druck und Temperatur konstant sind.
Also : Nimm dir eine Wasserdampftafel, hol dir die Werte raus und du kannst dir deine Wärme berechnen. |
|
 |
Physinetz
Anmeldungsdatum: 20.09.2006
Beiträge: 327
|
 Physinetz Verfasst am: 06. Jan 2011 14:00 Titel: Physinetz Verfasst am: 06. Jan 2011 14:00 Titel: |
 |
|
Ok soweit verstanden, aber wenn ichs trotzdem über die differentielle Form angehen will (so ist unsere Vorgehensweise nunmal) , wäre dass dann nicht so:
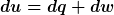
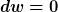 da keine Volumenänderungsarbeit und keine technische Arbeit vorliegt da keine Volumenänderungsarbeit und keine technische Arbeit vorliegt
Also:
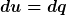
mittels  und und  und und folgt ja dann: folgt ja dann:

Also eingesetzt:
=q_{12})
Und habe ja eigentlich alle gegeben....nun müsste ja das gleiche rauskommen wie bei 
??? |
|
 |
o~O

Anmeldungsdatum: 30.11.2010
Beiträge: 184
|
 o~O Verfasst am: 07. Jan 2011 08:51 Titel: o~O Verfasst am: 07. Jan 2011 08:51 Titel: |
 |
|
Das sieht soweit erstmal ganz richtig aus. Nur deine Überlegung warum auf einmal dq = cv * dT ist, finde ich seltsam. Ich dachte dq = cv *dT sei nur eine Näherung. Kann mich aber auch täuschen.
Ich gehe halt eher ingenieurmäßig ran und hole mir dann die Werte und fertig ist. |
|
 |
|
















