| Autor |
Nachricht |
Tilli2
Anmeldungsdatum: 20.03.2021
Beiträge: 1
|
 Tilli2 Verfasst am: 20. März 2021 02:43 Titel: Ständig Wärme durch permanenten Überdruck? Tilli2 Verfasst am: 20. März 2021 02:43 Titel: Ständig Wärme durch permanenten Überdruck? |
 |
|
Meine Frage:
Wärme ist Teilchenbewegung. Wir nehmen ein Gas und füllen es bei Raumtemperatur in eine Flasche. Die Gasteilchen fliegen durcheinander und treffen natürlich auch auf die Innenfläche der Flasche.
Nun füllen wir die gleiche Menge Gas nochmal ein. Dann müßten ständig doppelt soviele Gasteilchen auf die selbe Innenfläche der Flasche treffen. Dann müßte doch die Flasche wärmer werden und ständig wärmer bleiben, solange diese dicht ist.
Wo ist der Denkfehler?
Meine Ideen:
mein Ansatz ist, ich weiß es momentan wirlich nicht. Wer kann helfen? |
|
 |
Nobby1
Anmeldungsdatum: 19.08.2019
Beiträge: 1650
|
 Nobby1 Verfasst am: 20. März 2021 10:03 Titel: Nobby1 Verfasst am: 20. März 2021 10:03 Titel: |
 |
|
Es gilt pV = nRT
Wenn n verdoppelt wird, kann nur p auf das doppelte steigen.V ist ja konstant. Man müsste schon T auf die Hälfte erniedrigen um den gleichen Zustand wieder herzustellen. |
|
 |
Tilli3
Gast
|
 Tilli3 Verfasst am: 20. März 2021 10:39 Titel: Tilli3 Verfasst am: 20. März 2021 10:39 Titel: |
 |
|
|
natürlich stimmt die Formel, und mit ihr ist das "Problem" schnell gelöst. Aber ich sehe hier eine Diskrepanz zwischen Formel und reiner Anschauung. In dieser Anschauung muß ein Fehler sein. Ich finde ihn aber nicht. |
|
 |
Nobby1
Anmeldungsdatum: 19.08.2019
Beiträge: 1650
|
 Nobby1 Verfasst am: 20. März 2021 10:55 Titel: Nobby1 Verfasst am: 20. März 2021 10:55 Titel: |
 |
|
|
Der Fehler ist, dass Du meinst die Teilchen bewegen sich schneller, nur das wäre eine Temperatur Erhöhung. Es gibt nur ein höheren Druck da mehr Teilchen auf die gleiche Oberfläche treffen. Die Geschwindigkeit wäre gleich . |
|
 |
Huggy
Anmeldungsdatum: 16.08.2012
Beiträge: 785
|
 Huggy Verfasst am: 20. März 2021 10:55 Titel: Huggy Verfasst am: 20. März 2021 10:55 Titel: |
 |
|
Wenn das Gas in einer Flasche und die Flasche im thermischen Gleichgewicht sind, also gleiche Temperatur haben, dann wird im zeitlichen Mittel genau so viel Energie vom Gas auf die Flasche übertragen wie von der Flasche aufs Gas. Bei einem einzelnen Stoß kann Energie in die eine oder andere Richtung übertragen werden, je nachdem wie die Schwingungsrichtung des getroffenen Flaschenatoms zu der Bewegungsrichtung des Gasteilchens ist.
Die Zahl der Gasatome hat dabei keinen Einfluss auf die Flaschentemperatur. Sie ändert aber die pro Zeiteinheit hin und her transportierte Energie. |
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 20. März 2021 16:40 Titel: Re: ständig Wärme durch permanenten Überdruck? Myon Verfasst am: 20. März 2021 16:40 Titel: Re: ständig Wärme durch permanenten Überdruck? |
 |
|
Folgendes nur als Ergänzung zum oben Gesagten.
| Tilli2 hat Folgendes geschrieben: | | Wärme ist Teilchenbewegung. |
Besser: Thermische Energie ist Teilchenbewegung.
| Zitat: | Dann müßten ständig doppelt soviele Gasteilchen auf die selbe Innenfläche der Flasche treffen. Dann müßte doch die Flasche wärmer werden und ständig wärmer bleiben, solange diese dicht ist.
Wo ist der Denkfehler? |
Da ist nicht unbedingt ein Denkfehler.
Auch bei doppelter Stoffmenge des Gases kann dieses dieselbe Temperatur haben, dies dann bei doppeltem Druck, wie schon geschrieben.
Wenn die Flasche und das Gas nicht dieselbe Temperatur haben, ist die Wärmeübertragung pro Zeit bei höherem Druck grösser - Wärmeübertragung vom Gas zur Flasche, wenn das Gas die höhere Temperatur hat als die Flasche, und sonst umgekehrt. Genau deshalb, weil, wie Du schreibst, pro Zeit und Fläche doppelt soviele Gasteilchen auf die Flasche treffen. Falls die Flasche kälter ist als das Gas, wird sie sich deshalb bei doppelter Stoffmenge des Gases stärker erwärmen - bis letztendlich Gas, Flasche und Umgebung ein neues thermisches Gleichgewicht erreicht haben bei einheitlicher Temperatur.
Durch die doppelte Teilchenzahl des Gases hat dieses auch die doppelte innere Energie und kann mehr Wärme abgeben. |
|
 |
Tilli5
Gast
|
 Tilli5 Verfasst am: 21. März 2021 04:03 Titel: Vakuum? Tilli5 Verfasst am: 21. März 2021 04:03 Titel: Vakuum? |
 |
|
| Huggy hat Folgendes geschrieben: |
Die Zahl der Gasatome hat dabei keinen Einfluss auf die Flaschentemperatur. Sie ändert aber die pro Zeiteinheit hin und her transportierte Energie. |
Die Teilchenanzahl hat keinen Einfluß auf die Temperatur im System? Warum ist es dann im Vakuum so kalt? Wir können doch die Flasche theoretisch mit nur einem Teilchen befüllen. Wie ist dann wohl die Temperatur darin? Bin jetzt etwas verwirrt. |
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 21. März 2021 08:04 Titel: TomS Verfasst am: 21. März 2021 08:04 Titel: |
 |
|
Im Vakuum ist es nicht warm oder kalt; im Vakuum existiert kein Temperaturbegriff.
Was du meinst ist nicht die Temperatur eines Systems, sondern dessen Abkühlung, d.h. die aus dem System an die Umgebung abgeführte Wärme. Bei einem bzgl. Stoffaustausch abgeschlossenen System wie einer Flasche oder einem Raumanzug existieren drei Mechanismen zum Wärmetransport: Wärmeleitung, Konvektion aufgrund eines umströmenden Mediums, Wärmestrahlung. Die ersten beiden Mechanismen existieren im Vakuum nicht, da kein umgebendes Medium vorliegt; d.h. der Wärmetransport ist sogar geringer als bei einem zusätzlich vorhandenen, kühleren umgebenden Medium; er erfolgt ausschließen über Wärmestrahlung.
_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago.
Zuletzt bearbeitet von TomS am 21. März 2021 08:28, insgesamt einmal bearbeitet |
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 21. März 2021 08:27 Titel: Re: ständig Wärme durch permanenten Überdruck? TomS Verfasst am: 21. März 2021 08:27 Titel: Re: ständig Wärme durch permanenten Überdruck? |
 |
|
| Tilli2 hat Folgendes geschrieben: | Wärme ist Teilchenbewegung. Wir nehmen ein Gas und füllen es bei Raumtemperatur in eine Flasche. Die Gasteilchen fliegen durcheinander und treffen natürlich auch auf die Innenfläche der Flasche.
Nun füllen wir die gleiche Menge Gas nochmal ein. Dann müßten ständig doppelt soviele Gasteilchen auf die selbe Innenfläche der Flasche treffen. Dann müßte doch die Flasche wärmer werden und ständig wärmer bleiben, solange diese dicht ist. |
Der erste begriffliche Fehler ist, dass es gerade nicht um Wärme geht. Wärme entspricht der mit einem umgebenden System ausgetauschten thermischen Energie. Dass es umgangssprachlich in einem Raum warm ist, hat nichts mit dem physikalischen Begriff der Wärme zu tun. In der Physik spricht man dann von Wärme, wenn thermische Energie ausgetauscht wird, insbs. wenn diese von einem Körper höherer zu einem Körper niedrigerer Temperatur fließt. Im Falle deiner Flasche spielt Wärme zunächst keine Rolle.
Die allgemeine Gasgleichung

alleine hilft auch nicht weiter. Sie beschreibt den Zusammenhang zwischen den Zustandsgrößen eines idealen Gases im thermodynamischen Gleichgewicht. Sie beschreibt keinen Prozess (die o.g. Wärme wäre eine entsprechende Prozessgröße).
Im vorliegenden Fall hast du es mit zwei Zuständen zu tun, nämlich dem vor und dem nach der Zuführung des zusätzlichen Gases. Bei identischem Volumen V gilt daher für die beiden Zustände i = 1,2

Um zu verstehen, wie sich Druck p und Temperatur T in Abhängigkeit von der Teilchenzahl ändern, musst du außerdem noch Details des Prozesses beschreiben.
Wenn du z.B. das zusätzliche Gas sehr langsam zuführst und sich die Flasche in einem Reservoir mit Temperatur
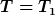
befindet, kannst du die Temperatur während des Prozesses konstant halten; es gilt


D.h. der Druck wächst proportional zur Teilchenzahl.
Durch die notwendige Kompression führst du dem System mechanische Arbeit zu; durch den Kontakt mit dem Reservoir kann jedoch Wärme abgeführt werden, so dass die Temperatur konstant bleibt.
Ich denke aber, das ist nicht das, was du im Sinn hast. Du möchtest stattdessen das Gas komprimieren jedoch thermisch vollständig von der Umgebung isolieren, richtig?
_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago. |
|
 |
Tilli6
Gast
|
 Tilli6 Verfasst am: 21. März 2021 10:36 Titel: Re: ständig Wärme durch permanenten Überdruck? Tilli6 Verfasst am: 21. März 2021 10:36 Titel: Re: ständig Wärme durch permanenten Überdruck? |
 |
|
| TomS hat Folgendes geschrieben: |
Ich denke aber, das ist nicht das, was du im Sinn hast. Du möchtest stattdessen das Gas komprimieren jedoch thermisch vollständig von der Umgebung isolieren, richtig? |
Hallo Tom, gut daß du als ein Moderator jetzt antwortest. Ich habe nämlich Probleme mit dem Registrieren. Habe Benutzername und Passwort per e-mail zugewiesen bekommen. Funktioniert aber nicht. Es heißt dann, wäre schon vergeben. Was aber komischerweise funktioniert, ist, daß ich mich immer mehr vervielfältige und ohne Registrierung poste. Zuerst war ich Tilli2, inzwischen bin ich Tilli6, um posten zu können. Was ist zu tun?
Nun zu meiner physikalischen Frage:
Wie gesagt, nicht die Formeln sind es, die ich nicht verstehe, sondern die reine Anschauung. Ich versuche jetzt, die reine Anschauung noch klarer darzustellen:
Wir nehmen nun bei Raumtemperatur zwei gleiche Flaschen. In die eine Flasche füllen wir eine Gasmenge mit Raumtemperatur ein. In die zweite Flasche füllen wir die doppelte Gasmenge ein. Dann warten wir eine Weile, um die Wärmeentwicklung des Einfüllvorganges abklingen zu lassen. Aber auch danach stoßen die Teilchen weiterhin an die Flaschenwandungen. In der zweiten Flasche stoßen also doppelt so viele Teilchen auf die Flaschenwandung, wie in der ersten. Ist nicht ein Stoß mechanische Arbeit? Wie ein Hammerschlag? Ein Hammerschlag erwärmt das Werkstück (bzw. überträgt thermische Energie). Das weiß man aus der reinen Anschauung seit Jahrtausenden. Die zweite Flasche kriegt nun doppelt soviele "Hammerschläge" ab. Trotzdem ist die zweite Flasche nicht wärmer als die erste. Man kann die Hand daran halten und merkt, beide Flaschen haben Raumtemperatur. Die Anschauung also ist es, die mir Probleme bereitet. |
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 21. März 2021 11:03 Titel: Myon Verfasst am: 21. März 2021 11:03 Titel: |
 |
|
"Hammerschläge" trifft es nicht so ganz. Es handelt sich um elastische Stösse zwischen den Gasteilchen und den Molekülen der Flaschenoberfläche. Im Mittel wird dabei Energie vom Körper/Gas mit höherer Temperatur (höherer mittlerer Teilchengeschwindigkeit) zum Körper/Gas mit tieferer Temperatur übertragen.
Die Wärmeübertragung pro Zeit und Fläche ist bei höherem Druck und gleicher Gastemperatur höher als bei tieferem Druck, siehe auch oben. Füllt man ein Gas mit Temperatur Tg in eine Flasche (Tg grösser als die Temperatur der Flasche), so wird sich die Flasche in einem bestimmten Temperaturintervall umso stärker erwärmen, je grösser die Teilchenzahl und der Druck des Gases ist.
Wenn das Gas und die Flasche die gleiche Temperatur haben, wie Du im letzten Beitrag annimmst, so wird keine Wärme übertragen. Bei den Stössen von Gasteilchen mit verschiedenen Geschwindigkeiten nehmen die Teilchen im Mittel gleich viel Energie auf, wie sie an die Flasche abgeben. Dies ist unabhängig vom Druck des Gases.
Zuletzt bearbeitet von Myon am 21. März 2021 11:07, insgesamt einmal bearbeitet |
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 21. März 2021 11:04 Titel: TomS Verfasst am: 21. März 2021 11:04 Titel: |
 |
|
Wenn der Benutzername schon vergeben ist, musst du dir halt eine anderen überlegen; ich heiße z.B. TomS, weil Tom schon vergeben war.
Zu deinem Problem: nochmal, es geht darum, wie du zu welchem Zielzustand gelangst; du kannst nicht einfach sagen, ich fülle Gas in die Flasche, du musst schon genauer spezifizieren, wie das vor sich gehen soll.
Im vorliegenden Fall könntest du von einem Zylinder der Größe 2V mit der Anzahl von Gasatomen 2N ausgehen; das Gas im Zylinder habe Raumtemperatur T und -druck p.
Nun komprimierst die das Gas durch einen Stempel im Zylinder auf die Hälfte des ursprünglich Volumens, d.h. von 2V auf V. Dadurch führst du dem Gas keine Wärme Q zu, jedoch mechanische Arbeit W durch das Komprimieren gegen den Druck.
1) Oben habe ich beschrieben, dass im Zuge dieser Kompression ein Wärmeaustausch mit der Umgebung möglich sein soll, so dass trotz zugeführter Arbeit W die Temperatur T konstant bleiben soll, d.h. entsprechend Wärme Q vom Gas im Zylinder an die Umgebung abgeführt wird.
2) Eine Alternative wäre, dass du den Zylinder thermisch vollständig isolierst, d.h. im Zuge dieser Kompression findet kein Wärmeaustausch mit der Umgebung statt, die zugeführter Arbeit W wird vollständig in Innere Energie des Gases U umgewandelt, sowohl Temperatur T als auch Druck p werden ansteigen.
Verstehst du den Unterschied?
Dann zu deiner Frage:
Bei höherem Druck jedoch identischer Temperatur finden mehr Teilchenstöße pro Zeit und Fläche statt. Aber durch einen Stoß wird keine mechanische Arbeit verrichtet, da das Volumen der Flasche konstant bleibt. Wenn du stattdessen einen verschiebbaren Stempel oder einen aufblasbaren Ballon verwenden würdest, dann würde sich das Volumen vergrößern und Arbeit verrichtet werden.
| Tilli6 hat Folgendes geschrieben: | | ... Inder zweiten Flasche stoßen also doppelt so viele Teilchen auf die Flaschenwandung, wie in der ersten ... Ein Hammerschlag erwärmt das Werkstück (bzw. überträgt thermische Energie). Das weiß man aus der reinen Anschauung seit Jahrtausenden. Die zweite Flasche kriegt nun doppelt soviele "Hammerschläge" ab. Trotzdem ist die zweite Flasche nicht wärmer als die erste. Man kann die Hand daran halten und merkt, beide Flaschen haben Raumtemperatur. Die Anschauung also ist es, die mir Probleme bereitet. |
Wenn die Flasche noch kälter als das Gas und mit diesem noch nicht im thermodynamischen Gleichgewicht ist, dann führt das natürlich zu einem messbaren Effekt: die Flasche erwärmt sich schneller, je höher der Druck ist (bei gleicher Temperatur). Aber im thermodynamischen Gleichgewicht haben Flasche und Gas dann eben die selbe Temperatur.
_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago. |
|
 |
|
|















