| Autor |
Nachricht |
annafragt
Anmeldungsdatum: 28.01.2021
Beiträge: 309
|
 annafragt Verfasst am: 02. Sep 2021 12:46 Titel: Relative Molekülmasse annafragt Verfasst am: 02. Sep 2021 12:46 Titel: Relative Molekülmasse |
 |
|
Meine Frage:
Hallo,
Ich habe mich ein wenig verwirrt bei der Gegenüberstellung zweier Aufgaben und frage mich, wieso für die Berechnung der Gefrierpunktserniedrigung T bei dissoziierenden/lösenden Substanzen die Kryoskopische Konstante des Lösungsmittels, die Masse der gelösten Sibstanz, die Masse des Lösungsmittels und das Dissoziationsverhalten der Substanz notwendig ist, aber für die relative Molekülmasse einer nicht dissoziierenden Substanz nur die Masse der Substanz erforderlich ist.
1) Braucht man auch für die relative Molekülmasse einer dissoziierenden Substanz nur die Masse der Substanz? Eigentlich schon oder, weil M= m/n. ?
2) Ist das so, dass man nur für eine dissoziierenden Susbtanz die Gefrierpunktserniedrigung bestimmen kann, weil wenn sich eine Substanz nicht löst, kann sie auch keine Gefrierpunktserniedrigung bewirken? Oder wie ist es zu verstehen?
Ich hoffe, meine Frage ist verständlich und würde mich über eine Antwort sehr freuen.
Meine Ideen:
Danke und liebe Grüße Anna
| Beschreibung: |
|
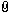
Download |
| Dateiname: |
16A4AEA9-F1E6-4660-A94F-323712F492D4.jpeg |
| Dateigröße: |
222.43 KB |
| Heruntergeladen: |
155 mal |
|
|
 |
willyengland
Anmeldungsdatum: 01.05.2016
Beiträge: 869
|
 willyengland Verfasst am: 02. Sep 2021 13:09 Titel: willyengland Verfasst am: 02. Sep 2021 13:09 Titel: |
 |
|
"dissoziierend" heißt ja, dass sich der Stoff in seine Ionen trennt, z.B. NaCl.
Aber es gibt auch nicht dissoziierende Stoffe, die sich lösen, z.B. Zucker.
Da es unterschiedliche Möglichkeiten für die Dissoziation gibt, vgl. z.B. NaCl und CaCl2, muss man das eben wissen, wie es dissoziiert.
Es ist richtig, dass ein Stoff der sich nicht löst auch keine Gefrierpunktserniedrigung bewirkt.
_________________
Gruß Willy |
|
 |
annafragt
Anmeldungsdatum: 28.01.2021
Beiträge: 309
|
 annafragt Verfasst am: 26. Sep 2021 19:03 Titel: annafragt Verfasst am: 26. Sep 2021 19:03 Titel: |
 |
|
Vielen Dank,
Ich habe mir vorgenommen, meinem Tutor mal wegen der verwirrend und ungenau gestellten Übungsaufgaben zu schreiben. Vorher wollte ich aber noch eine Verwirrung klären und würde mich über eine Antwort sehr freuen.
Bei Aufgabe 95 hatten wir ja gesagt, für die Ermittlung der relativen Molekülmasse benötigt man nur die Maße (M=m/n).
Wieso ist nun bei Aufgabe 98 und 99 (quasi dieselbe Frage) bei 98 E richtig, sprich das relative Molekulargewicht von der Masse der Sibstanz, des Lösungsmittels und der kryoskoposchen Konstante des Lösungsmittel abhängig und bei 99 D richtig?
Sind die Lösungen richtig oder habe ich recht, dass die relative Molekülmasse auch hier nur von der Masse abhängig ist und nicht von den anderen Parametern?
Danke und liebe Grüße
Anna
| Beschreibung: |
|
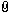
Download |
| Dateiname: |
A63BCCEB-3259-4186-A3AE-D3F68286F13D.jpeg |
| Dateigröße: |
242.91 KB |
| Heruntergeladen: |
143 mal |
|
|
 |
Füsik-Gast
Gast
|
 Füsik-Gast Verfasst am: 27. Sep 2021 10:05 Titel: Kryoskopie Füsik-Gast Verfasst am: 27. Sep 2021 10:05 Titel: Kryoskopie |
 |
|
Du solltest dir das Grundprinzip der Kryoskopie klar machen und was man dort direkt mißt.
Man hat die Masse eines bestimmten Lösungsmittels mit bekannter kryoskopischer Konstanten und die Masse eines darin gelösten Stoffes.
Durch den Effekt der Gefrierpunktserniedrigung ist der Gefrierpunkt der Lösung geringer als der des reinen Lösungsmittels.
Da dieser Effekt zu den kolligativen Eigenschaften zählt,hat man zuerst nur eine Aussage der Teilchenzahl n gelöster Teilchen,die in der Lösung vorliegen.
Geht man jetzt davon aus,daß der gelöste Stoff undissoziiert vorliegt,
entspricht die "gemessene" Teilchenzahl auch der Teilchenzahl des gelösten Stoffes.
Über die Einwaage m und die ermittelte Stoffmenge n kommt man auf die molare Masse M nach M=m/n .
Umgekehrt kann man bei einem Stoff bekannter molarer Masse M und einer Einwaage m durch Kryoskopie feststellen,ob und wie dissoziiert dieser in der Lösung vorliegt(Bestimmung des Dissoziationsgradens per Kryoskopie..).
Die Umrechnungen der molaren Masse M auf Molekülmassen,bzw. relative Molekülmasse ist einfach mathematisch.
Man kann auch simpel die Einheit g/mol von M weglassen:
"Die molare Masse ist hingegen die Summe aller Atommassen der einzelnen Elemente eines Moleküls bezogen auf ein Mol dieser Teilchen und wird in Masse pro Mol (meist g/mol) angegeben. Der Zahlenwert der relativen Molekülmasse und der molaren Masse ist dabei gleich. .."
Füsik-Gast.
|
|
 |
|
|















