| Autor |
Nachricht |
Sdxy
Anmeldungsdatum: 10.02.2013
Beiträge: 1
|
 Sdxy Verfasst am: 10. Feb 2013 12:30 Titel: Thema : gasgleichung (modifizierter Feuerlöscher TNT - Druck Sdxy Verfasst am: 10. Feb 2013 12:30 Titel: Thema : gasgleichung (modifizierter Feuerlöscher TNT - Druck |
 |
|
Meine Frage:
Ein modifizierter Feuerlöscher enthält den Sprengstoff TNT (p = 1,6 g/cm3), der die spez. Verbrennungswärme qv = 2,72 x 10 hoch 7 J/kg besitzt.
Welcher Druck herrscht in dem Feuerlöscher nach plötzlicher vollständiger Verbrennung des TNT zu gasförmigen Endprodukten mit dem mittleren Freiheitsgrad von 7? Folge?
Ich bin maßlos überfordert :-/
Meine Ideen:
qv = w/m
p = m/V
U = f/2 x NkT = f/2 x p x V = qv x m
1/2 x p = qv x (Dichte (=m/V)) |
|
 |
magician4
Anmeldungsdatum: 03.06.2010
Beiträge: 914
|
 magician4 Verfasst am: 10. Feb 2013 17:56 Titel: magician4 Verfasst am: 10. Feb 2013 17:56 Titel: |
 |
|
wenn ichs grad recht sehe....
...kommst du zur loesung der aufgabe nicht daran vorbei, die gasteilchenzahl welche aus deinem TNT entsteht zu ermitteln:
- nur so kannst du die (berechenbare*) ) energie aus einem (frei waehlbaren: das volumen des feuerloeschers ist nicht entscheidend: nimm dir 1L oder sowas) bezugsvolumen TNT dann auf die bei seiner verbrennung generierte teilchenzahl projezieren ) energie aus einem (frei waehlbaren: das volumen des feuerloeschers ist nicht entscheidend: nimm dir 1L oder sowas) bezugsvolumen TNT dann auf die bei seiner verbrennung generierte teilchenzahl projezieren
- gem. der vorgegebenen zahl an mittleren freiheitsgraden "7" und der bekannten energie pro freiheitsgrad E(fg) = 1/2 k*T laesst sich mit E(teilchen) = 7/2 kT dann aber die mittlere temperatur der gasteilchen daraus berechnen
- du kennst sodann das volumen (= dein frei gewaehltes bezugsvolumen), die teilchenzahl und die temperatur, und kannst sodann in umstellung der allg. gasgleichung (ueber deren anwendbarkeit in diesem fall man trefflich streiten kann) den zugehoerigen druck berechnen
.... unter dem das gebinde dann zu bersten hat, so meine einschaetzung
was dir hier jedoch nach wie vor fehlt ist die chemische seite des problems: wieviele mol teilchen bekommst du aus 1 L festem TNT?
hierzu folgende info:
unterstellt man eine standardmaessige vollstaendige langsame verbrennung im sauerstoff-ueberschuss**) , so waere folgende idealisierte verbrennungsgleichung zu formulieren*** , so waere folgende idealisierte verbrennungsgleichung zu formulieren***) : :
TNT ("trinitrotoluol") =  , M = 227,13 g/mol , M = 227,13 g/mol

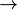 aus 1 mol TNT = 227,13 g TNT entstehen mithin 11 mol gasteilchen aus 1 mol TNT = 227,13 g TNT entstehen mithin 11 mol gasteilchen
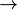 unser bezugsvolumen von 1 L enthaelt bei der mitgeteilten dichte des TNT von unser bezugsvolumen von 1 L enthaelt bei der mitgeteilten dichte des TNT von  = 1,6 g/cm³ 1600g TNT entsprechend = 1,6 g/cm³ 1600g TNT entsprechend  7,044 mol TNT, aus denen gem. obiger verbrennungsgleichung sodann 7,044 mol TNT, aus denen gem. obiger verbrennungsgleichung sodann  77,49 mol gasteilchen entstehen 77,49 mol gasteilchen entstehen
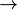 77,49 mol teilchen ist also die gesuchte teilchenzahl aus 1 L festem TNT , auf welche du die berechnete energie**** 77,49 mol teilchen ist also die gesuchte teilchenzahl aus 1 L festem TNT , auf welche du die berechnete energie****) zu projezieren hast zu projezieren hast
... und den rest schaffst du jetzt sicherlich alleine
gruss
ingo
*)
fuer das von mir vorgeschlagene bezugsvolumen 1 L waeren dies E = 1600 g * 2,72 *  J/g = 4,352 * J/g = 4,352 *  J J
**)
das ist so ziemlich der unrealistischte teil der gesamten aufgabenstellung, wenn wir ueber TNT reden
um mich nun aber nicht in chemischen details zu verlieren: die wirklichkeit ist voellig anderes, selbst wenn wir "nur" ueber eine verbrennung redeten, und "verbrennung" ist nun grad aber nicht die typische anwendung bei TNT.
vielmehr ist der typische anwendungsfall "explosion", und der funzt abermals voellig anders, hat demzufolge andere energien und insbesondere voellig andere auftretende spitzendruecke
***)
ich gehe davon aus, dass ich uns die feinheiten warum und wieso grad diese stoechiometrie herauskommt bei der idealisierten verbrennung ersparen kann: andernfalls frag bitte nochmals nach
****)
korrektopaldistens muesstest du eigentlich auch die in dem festen TNT vor verbrennung ja ebenfalls "gebundene" waermenenge bei experimentbeginn hier dazuaddieren (denn die ist ja nicht ploetzlich einfach verschwunden), energetische betrachtungen zum zusaetzlich eingebundenen sauerstoff anstellen u.v.a.m.
die aufgabenstellung scheint jedoch zu wuenschen, dass dies vernachlaessigt wird |
|
 |
|
|















