| Autor |
Nachricht |
Katsuha
Anmeldungsdatum: 30.08.2012
Beiträge: 3
|
 Katsuha Verfasst am: 30. Aug 2012 17:42 Titel: Wärmelehre / Temperatur Katsuha Verfasst am: 30. Aug 2012 17:42 Titel: Wärmelehre / Temperatur |
 |
|
Hallo zusammen!
Ich stehe hier leider vor einem kleinen Problem und hoffe, dass ihr mir dabei behilflich sein könnt.
Ich habe eine Physikaufgabe auf morgen zu bewältigen und bin noch ungewiss, ob ich sie mit den richtigen Ansätzen gelöst habe.
Hier die Aufgabe aus unserem Script:
Julia liebt den Tee mit etwas Vollrahm. Beim Zubereiten lässt sie Wasser kochen.
Sie macht 0.6 Deziliter Tee (= 0.06 l); dieser Tee hat die Temperatur 90°C. Dann
fügt sie den Rahm hinzu. Mit ihren Lippen spürt sie, wann das Getränk zum Trinken
nicht zu heiss ist. Das ist gerade dann der Fall, wenn das Getränk nicht mehr als
40°C warm ist.
Julia fügt nur soviel Rahm wie nötig hinzu, damit sie ihren Tee gerade trinken kann.
Berechnen Sie die Menge Rahm in Deziliter, welche Julia benötigt. Wählen Sie für
den Rahm eine sinnvolle Anfangstemperatur (auf 10°C gerundet). Die Tasse
nimmt praktisch gar keine Energie dem Tee weg. Ferner wartet Julia nicht, dass
sich der Tee von selbst abkühlt. Der Tee hat die gleiche spezifische
Wärmekapazität wie Wasser.
(Die spezifischen Wärmekapazitäten zu dem Tee (4,2 kJ / kg * T) und dem Vollrahm (3,5 kJ / kg * T) waren auch angegeben.)
Ich habe diese Aufgabe mit der Formel c = Q / m * T angegangen und habe zuerst das Q ausgerechnet.
Also Q = c * m * T = 4,5 * 0.06 * 90 = 22,68
Dieses habe ich dann in die Formel eingesetzt und mit den Werten zu dem Vollrahm weitergerechnet:
m = Q / c * T = 22,68 / 3,5 * 50 (90-40) = 0.1296
Kann diese Resultat stimmen? Hoffentlich habe ich mich klar und verständlich ausgedrückt, sonst einfach nachfragen.
Vielen Dank im voraus!
Mit freundlichen Grüssen,
Kat |
|
 |
magician4
Anmeldungsdatum: 03.06.2010
Beiträge: 914
|
 magician4 Verfasst am: 30. Aug 2012 21:49 Titel: magician4 Verfasst am: 30. Aug 2012 21:49 Titel: |
 |
|
tip vorweg: schreib dir bitte bei berechnungen nicht nur die zahlen, sondern auch die zugehoerigen einheiten mit dazu: sowas macht fehler immer sehr viel augenfaelliger, auch und besonders, wenn man sich da mit den formeln mal irgendwie verdaddelt hat
zu deiner eigentlichen frage:
| Zitat: | | (Die spezifischen Wärmekapazitäten zu dem Tee (4,2 kJ / kg * T) und dem Vollrahm (3,5 kJ / kg * T) waren auch angegeben.) |
da zweifel ich aber mal stark...
stand da nicht in wirklichkeit " *K " ?
| Zitat: | | Ich habe diese Aufgabe mit der Formel c = Q / m * T angegangen |
eine solche formel gibt es nicht.
eine waermemenge ist nur (in dieser art)*) definiert zwischen zwei temperaturen, mithin Q= c * m * definiert zwischen zwei temperaturen, mithin Q= c * m * T T
(oder umgestellt c = Q / m * 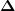 T ) T )
| Zitat: | | Also Q = c * m * T = 4,5 * 0.06 * 90 = 22,68 |
hier hast du grad die waermemenge berechnet, welche du fuer eine temperaturaenderung von 90K an 60 g wasser benoetigen wuerdest.
die ist aber nicht wirklich interessant.
wirklich interessant ist hingegen diejenige waermemenge welche dir quasi "freiwird", indem du den tee von 90°C auf 40° C abkuehlst, mithin also ein 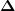 T von -50 K dem tee aufzwingst T von -50 K dem tee aufzwingst
)
dieses  ist mit den dir gegebenen daten berechenbar. ist mit den dir gegebenen daten berechenbar.
es muss gleich der waermemenge  sein, welche der rahm aufnimmt** sein, welche der rahm aufnimmt**) : :
 )
(ich hab mal unterstellt, dass sie den rahm mit geschaetzten 10°C just aussm kuehlschrank geholt hat)
so... und nun solltest du den rest eigentlich allen schaffen, oder?
gruss
ingo
*)
i.e. wenn du also mit einer linearen waermekapazitaet rechnen darfst, dort unterwegs mithin also auch nix anderes wie z.b. einfrieren, verdampfen usw. passiert waehrend der temperaturaenderung um 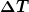 , also von , also von  auf auf 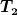
**)
lass dich durch das vorzeichen von  nicht irritieren: die von vorgang 1 bereitgestellte waermemenge "verlaesst" gewissermassen den tee, und hat daher waehrend des verlassens konventionsgemaess ein negatives vorzeichen. nicht irritieren: die von vorgang 1 bereitgestellte waermemenge "verlaesst" gewissermassen den tee, und hat daher waehrend des verlassens konventionsgemaess ein negatives vorzeichen.
in dem moment wo sie von vorgang 2 - der rahmerwaermung - aufgenommen wird, "betritt" sie quasi das system "rahm" - und wird dort daher positiv bilanziert.
korrektopaldistens muesste man also schreiben: 
... oder man macht es sich ganz leicht, und schreibt einfach:  |
|
 |
Katsuha
Anmeldungsdatum: 30.08.2012
Beiträge: 3
|
 Katsuha Verfasst am: 31. Aug 2012 08:18 Titel: Katsuha Verfasst am: 31. Aug 2012 08:18 Titel: |
 |
|
Hallo Ingo
Vielen Dank für deine Hilfe! Soviel Informationen hätte ich in meinen kühnsten Träumen nicht erwarten können.
Ich glaube, die Aufgabe ist mir nun klar - nur zur Sicherheit, kann das Resultat von 0,12 l Vollrahm stimmen?
Physik ist leider wirklich nicht meine grösste Stärke, darum bin ich auch immer argwöhnisch gegen die von mir erhaltenen Resultate...
Mit freundlichen Grüssen,
Kat |
|
 |
magician4
Anmeldungsdatum: 03.06.2010
Beiträge: 914
|
 magician4 Verfasst am: 31. Aug 2012 12:27 Titel: magician4 Verfasst am: 31. Aug 2012 12:27 Titel: |
 |
|
| Zitat: | Soviel Informationen hätte ich in meinen kühnsten Träumen nicht erwarten können.
|
eigentlich ist exakt dies aber das ziel derer, die in diesem forum als erklaerer mitwirken (so zuminest nehme ich die anderen hier wahr): dass jemand der eine frage vernuenftig und mit eigenbemuehungen stellt - also exakt das was du getan hast - eine antwort bekommt, die ihn weiterbringt, die dinge erklaert, und die ihn in die lage versetzt das geschilderte problem zu loesen.
m.a.w.: das ziel ist es, dass du die dinge verstehst
..was in diesem fall ja auch augenscheinlich geklappt hat.
| Zitat: | | kann das Resultat von 0,12 l Vollrahm stimmen? |
wie ich bereits einleitend sagte: EINHEITEN !
das resultat (wenn du dich der von mir gewaehlten ausgangstemperatur fuer rahm anschliessen magst) ist 0,12 kg , also 120 g, ja: auf dieses ergebnis komme ich auch
120g fluessigkeit sind jedoch nur dann auch 120 ml (resp. 0,12 l) wenn der rahm eine dichte von 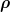 = 1 g/cm³ haette, die er nicht hat. = 1 g/cm³ haette, die er nicht hat.
daher, und da dir die aufgabenstellung nicht verraet welche dichte fuer rahm du in ansatz bringen sollst, kannst du dein ergebnis eben nicht in liter zum ausdruck bringen, sondern musst es dabei belassen dort 120 g auszuweisen.
aber den rechenweg scheinst du korrekt zuende gefuehrt zu haben: freut mich dass es dir nuetzlich war
gruss
ingo
p.s.: 2/3 rahm mit 1/3 tee.... * grusel....das ist selbst fuer eingefleischte "tee-mit-milch-fans" echt ne haerte.... |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 31. Aug 2012 13:06 Titel: franz Verfasst am: 31. Aug 2012 13:06 Titel: |
 |
|
OT
Lecker Tee 
Aber ernsthaft: In welchen Tee kommt Sahne, außer vielleicht Assam-Kehricht. |
|
 |
magician4
Anmeldungsdatum: 03.06.2010
Beiträge: 914
|
 magician4 Verfasst am: 31. Aug 2012 17:15 Titel: magician4 Verfasst am: 31. Aug 2012 17:15 Titel: |
 |
|
fette sind geschmackstraeger, und runden somit auch geschmacklich das ergebnis von aromenextraktionen ggf. interessant ab.
insoweit macht also auch sahne sinn, fuer den ders mag.
ich hab beispielsweise gern ein troepfchen davon zu early grey/jasmin, und ein stueckchen kandis dazu in kalter jahreszeit... find ich einfach lecker
gruss
ingo |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 31. Aug 2012 18:22 Titel: franz Verfasst am: 31. Aug 2012 18:22 Titel: |
 |
|
Madig-ranzigen Yak-Speck im Earl Grey?
Ich sach mal garnix, sonst kracht in paar Minuten hier links eine 50 Mt Fliegerbombe ohne Zündverzögerung durchs Fenster. ...

Naja; wünsche Dir eine robuste Gesundheit! |
|
 |
magician4
Anmeldungsdatum: 03.06.2010
Beiträge: 914
|
 magician4 Verfasst am: 31. Aug 2012 22:30 Titel: magician4 Verfasst am: 31. Aug 2012 22:30 Titel: |
 |
|
nee.... nicht der stoff fuer weicheier nd landratten...
bei mir kommt nur der echte earl grey auffn tisch, also zweifelhafte teestaubfegereste dubioser provinienz, welche in monatelanger schiffsueberfahrt das grundaroma verfaulten bilgenwassers angenommen haben, welches hilflos mit etwas oel halbvergammelter bergamotten zu ueberdecken versucht wird...
aber die sache mit der yakbutter klingt interessant...
gruss
ingo
* guckt grad ob er irgendwo noch etwas aceton und celluloseacetat rumstehen hat, oder obs doch der klassiker "halbkonz. schwefelsaure + aluminium" wird... |
|
 |
Katsuha
Anmeldungsdatum: 30.08.2012
Beiträge: 3
|
 Katsuha Verfasst am: 07. Sep 2012 15:08 Titel: Katsuha Verfasst am: 07. Sep 2012 15:08 Titel: |
 |
|
Hallo zusammen,
Tut mir Leid für die späte Antwort, hatte eine etwas stressige Woche und bin daher erst jetzt dazugekommen, wieder dieses Forum aufzusuchen.
Wiederum: Vielen herzlichen Dank für die Hilfe!
Das mit den Einheiten ist mir nun auch klar, glücklicherweise konnte ich diesen Fehler während der Präsentation der Aufgabe verhindern (sie ist übrigens dank Deiner kräftigen Mithilfe geglückt).
Zu OT:
Diesen Tee würde ich wohl auch nicht freiwillig konsumieren... Da ist mir ein schöner Kräuter- resp. Gewürze-Tee mit einem Löffel Honig und einer kleinen Menge Vollmilch viel lieber. 
Mit freundlichen Grüssen,
Kat |
|
 |
|
|
















