| Autor |
Nachricht |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 01. Jan 2008 20:30 Titel: Mischungstemperatur Mudi Verfasst am: 01. Jan 2008 20:30 Titel: Mischungstemperatur |
 |
|
Ich krieg die Aufgabe überhaupt nicht hin! ich find irgenwie auch keine formel für diese aufgabe  könntet ihr mir bitte hier weiter helfen könntet ihr mir bitte hier weiter helfen 
ich muss die aufgabe nächste woche abgeben 
Hier ist die Aufgabe:
100g Eis mit der Temperatut 0°C werden mit 200g Wasser der Temperatur 90°C übergossen. Welche Mischungstemperatur stellt sich ein? Welche Mischungstemperatur ergibt sich, wenn das Eis die Temp. -10°C hat?
wär supppppa hamma lieb wenn ihr mir dabei helfen würdet
thx
 |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 01. Jan 2008 21:38 Titel: dermarkus Verfasst am: 01. Jan 2008 21:38 Titel: |
 |
|
Magst du mal in Worten sagen, was du gefühlsmäßig erwartest, was da passiert, und was du ganz ungefähr für ein Ergebnis schätzst?
Und mal die Formeln hier aufschreiben, die du bisher für so ähnliche Aufgaben kennengelernt hast? (Das braucht keine fertige Formel sein, die komplett auf diese Aufgabe passt!) |
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 02. Jan 2008 01:18 Titel: Mudi Verfasst am: 02. Jan 2008 01:18 Titel: |
 |
|
ya also in physik bin ich ne niete ich hab ne 5 xD
und darum will ich nen referat machen (schriftl.) und der lehrer hat mir 5 aufgaben gegeben und bei der komm ich net weiter
soweit ich weiss kann man glaub ich net diese formel einsetzen:
W=c*m*T
naja ich habs versucht und ich hab 37620 J raus aba is des die Mischungstemepratur? 
ya und dann hab ich 37620/2.09(j/g*K)*200 g = 78 K
und dann hab ich 90K + 78K = 168 K
ya aba ich glaub des is totally wrong oda?  xD xD
ich weiss echt net weiter
*ahhhh*  
  
liebe grüße
mudi |
|
 |
Dalton
Anmeldungsdatum: 19.12.2007
Beiträge: 45
|
 Dalton Verfasst am: 02. Jan 2008 13:36 Titel: Dalton Verfasst am: 02. Jan 2008 13:36 Titel: |
 |
|
| Mudi hat Folgendes geschrieben: | | naja ich habs versucht und ich hab 37620 J raus aba is des die Mischungstemepratur? |
Nein, Joule ist die Einheit für Energie nicht für die Temperatur.
Sind die Temperaturen, Massen und spezifischen Wärmekapazitäten der zu mischenden Stoffen bekannt, dann kannst du die Mischungstemperatur berechnen, wenndu die Wärmeenergien  und und 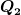 kennst. Die Wärmeenergie der Mischung bezeichnen wir mit kennst. Die Wärmeenergie der Mischung bezeichnen wir mit  . Dann gilt: . Dann gilt: 
(Soweit klar?)
Du weißt darüber hinaus, dass (  ist die Mischungstemperatur) ist die Mischungstemperatur)



ist.
Versuche nun eine Gleichung zu erstellen, und stelle dann nach der Mischungstemperatur  auf. auf. |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 02. Jan 2008 16:05 Titel: dermarkus Verfasst am: 02. Jan 2008 16:05 Titel: |
 |
|
| Mudi hat Folgendes geschrieben: |
W=c*m*T
|
Das ist schonmal eine Formel von den Formeln, die hier nützlich sein könnten 
Magst du mal genau dazusagen, wo du diese Formel kennengelernt hast?
Hat diese Formel etwas mit Erwärmen von Wasser zu tun?
Sag mal in Worten, was das W, das c, das m und das T in dieser Formel bedeuten. Kennst du eine Aufgabe, in der du schon mal mit dieser Formel gerechnet hast?
---------------------------------------
Außer Formeln sammeln ist es am Anfang erst mal am wichtigsten, zu überlegen, was da überhaupt passiert. Die Aufgabenstellung sagt, da wird 90°C heißes Wasser auf Eis draufgekippt.
Sag erstmal ganz ohne zu rechnen:
1) Was wird mit dem Eis passieren?
2) Was wird mit dem heißen Wasser passieren?
3) Wird die Mischungstemperatur
... a) heißer sein als 90°C?
... b) irgendwo zwischen 0°C und 90°C liegen?
... c) kälter sein als 0°C ? |
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 02. Jan 2008 20:38 Titel: Mudi Verfasst am: 02. Jan 2008 20:38 Titel: |
 |
|
ähm was ist den Q? woher weiss ich Tm? 
die formel hab ich im unterricht gelernt  bin in der 9. klasse bin in der 9. klasse  
also w ist work(energie); m ist die masse (hier 200g) c ist die konstante (eis) ich glaub es nur 
ya ähm ich glaub das eis wird schmelzen 
und die temp. wird glaub ich unter 0° sein
lg mudi |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 02. Jan 2008 20:50 Titel: dermarkus Verfasst am: 02. Jan 2008 20:50 Titel: |
 |
|
| Mudi hat Folgendes geschrieben: |
also w ist work(energie); m ist die masse (hier 200g) c ist die konstante (eis) ich glaub es nur 
|
Da bist du auf einem guten Weg  Magst du das noch ein bisschen genauer sagen? Wofür verwendet man diese Formel? Wie heißt die Konstante, die du da meinst, genau? Welchen Wert hat diese Konstante? Was genau ist das T in deiner Formel? (Du darfst auch gerne spicken, zum Beispiel in deinem Heftaufschrieb, dort wo du die Formel gelernt hast, oder bei den Aufgaben, die du schon mal mit dieser Formel gerechnet hast Magst du das noch ein bisschen genauer sagen? Wofür verwendet man diese Formel? Wie heißt die Konstante, die du da meinst, genau? Welchen Wert hat diese Konstante? Was genau ist das T in deiner Formel? (Du darfst auch gerne spicken, zum Beispiel in deinem Heftaufschrieb, dort wo du die Formel gelernt hast, oder bei den Aufgaben, die du schon mal mit dieser Formel gerechnet hast  ) )
| Zitat: |
ya ähm ich glaub das eis wird schmelzen 
|
Einverstanden  Also brauchen wir noch eine Formel, und zwar eine Formel für das Schmelzen von Eis. Kennst du da eine oder kannst du eine finden? Also brauchen wir noch eine Formel, und zwar eine Formel für das Schmelzen von Eis. Kennst du da eine oder kannst du eine finden?
| Zitat: |
und die temp. wird glaub ich unter 0° sein
|
Vorsicht, ich glaube, da machst du den dritten Schritt vor dem zweiten.
Mach erst mal den zweiten Schritt: Was wird mit dem heißen Wasser passieren? Wird es wärmer werden oder kälter? Würdest du dich trauen, nach dem Mischen die Hand reinzuhalten? Was passiert mit der Energie des heißen Wassers? |
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 02. Jan 2008 23:03 Titel: Mudi Verfasst am: 02. Jan 2008 23:03 Titel: |
 |
|
Die Formel benutzt man wenn bei einem körper die masse (m) die Temp. steigt und die innere energie erhöht wird 
Die konstante für eis ist o,38 J/g*K und für Wasser 4,2 J/g*K
Ich finde echt keine Formel für das eis schmelzen ich hab ansgt das ich das net mehr schaffe  ihr seit meine letzte hoffnung ihr seit meine letzte hoffnung
hmmm...also das wasser wird doch wärmer und was mit der energie passiert hab ich echt keine ahnung, hmmm...vllt wird die enrgie abgewandert naja
ich komm net weiter      
lg |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 02. Jan 2008 23:20 Titel: dermarkus Verfasst am: 02. Jan 2008 23:20 Titel: |
 |
|
| Mudi hat Folgendes geschrieben: | Die Formel benutzt man wenn bei einem körper die masse (m) die Temp. steigt und die innere energie erhöht wird 
Die konstante für eis ist o,38 J/g*K und für Wasser 4,2 J/g*K
|
Prima 
Und woran sieht man in der Formel, um wieviel die Temperatur steigt?
| Zitat: |
Ich finde echt keine Formel für das eis schmelzen
|
Tipp: Hast du schon mal was von Schmelzwärme gehört? Findest du dazu etwas in deinem Heft oder in deinem Physikbuch?
// edit: oder dort  http://www.physikerboard.de/topic,10350,-definition-spezifische-schmelzwaerme.html#63604 http://www.physikerboard.de/topic,10350,-definition-spezifische-schmelzwaerme.html#63604
| Zitat: |
hmmm...also das wasser wird doch wärmer und was mit der energie passiert hab ich echt keine ahnung, hmmm...vllt wird die enrgie abgewandert
|
Du näherst dich der Sache 
Welches Wasser wird wärmer, welches wird kälter? Was passiert mit dem kalten Wasser, das aus dem Schmelzen des Eises entstanden ist? Und was passiert mit dem Wasser, das am Anfang das heiße Wasser bei 90°C war? Von wo nach wo wandert hier die Wärmeenergie? |
|
 |
Second_Q
Anmeldungsdatum: 30.09.2007
Beiträge: 155
Wohnort: DE
|
 Second_Q Verfasst am: 02. Jan 2008 23:47 Titel: Second_Q Verfasst am: 02. Jan 2008 23:47 Titel: |
 |
|
Wie währe es damit :

100g (  ) Eis mit der Temperatur 0°C ( ) Eis mit der Temperatur 0°C (  ) )
200g (  ) Wasser der Temperatur 90°C ( ) Wasser der Temperatur 90°C (  ) )

Mischtemperatur (  ) )
 |
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 02. Jan 2008 23:55 Titel: Mudi Verfasst am: 02. Jan 2008 23:55 Titel: |
 |
|
Ich weiss nicht was Q ist, kann mir das bitte jmd sagen  und was is T? is das DeltaT? und was is T? is das DeltaT?
ich hab das net mit diesen buchtstaben gelernt 
wir benutzen immer:
w=work
c=konstante
m=masse
ΔT= Delta T
aber was Q is hab ich echt keine ahung 
lg
naja ok ich versuchs mal wie du es sagst:
100g*0°C+200g*90°/300g = 60
also müsste die Mischungstemp. 60 sein   
omg is das richitig????!!!! |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 03. Jan 2008 00:02 Titel: dermarkus Verfasst am: 03. Jan 2008 00:02 Titel: |
 |
|
Du darfst gerne Deine Buchstaben benutzen 
Für das Erwärmen also gerne die Formel

und für das Schmelzen das, was du über Schmelzwärme weißt 
Hast du schon eine Antwort auf meine Fragen von oben gefunden? Also zum Beispiel auch, von wo nach wo die Wärmeenergie in unserem Beispiel wandert?
//edit:
| Mudi hat Folgendes geschrieben: |
omg is das richitig????!!!! |
Ich empfehle immer gerne, erstmal zu verstehen, worum es geht, dann brauchst du nämlich gar keine fertigen Formeln von anderen verwenden, die du selbst noch gar nicht nachvollzogen hast  Und ich finde, beim Selberverstehen bist du gerade schon auf einem prima Weg Und ich finde, beim Selberverstehen bist du gerade schon auf einem prima Weg  |
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 03. Jan 2008 00:56 Titel: Mudi Verfasst am: 03. Jan 2008 00:56 Titel: |
 |
|
ya schon aba ich hab immer noch keine formel xD
ich habs am anfang damit verucht
37620/2.09(j/g*K)*200 g = 78 K
und dann hab ich 90K + 78K = 168 K
aba das hat mia net weitergeholfen
hmmm...und zu deinen fragen
also vllt könnte es sein das die temp. auf null bleibt
naja ich schreib morgen weiter geh jezz schlafen
bye |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 03. Jan 2008 01:07 Titel: dermarkus Verfasst am: 03. Jan 2008 01:07 Titel: |
 |
|
Eine fertige Komplettformel brauchst du auch gar nicht für diese Aufgabe  Schrittweise und mit Selberverstehen geht das ganze am Ende viel besser und obendrein richtiger Schrittweise und mit Selberverstehen geht das ganze am Ende viel besser und obendrein richtiger 
(Die Formeln, die Dalton und Second_Q hier aufgeschrieben haben, reichen übrigens nicht, um zum richtigen Ergebnis zu kommen.)
Schlaf gut und bis morgen  |
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 03. Jan 2008 15:03 Titel: Mudi Verfasst am: 03. Jan 2008 15:03 Titel: |
 |
|
hmmm...okiii und wie soll ich jetzt die mischungstemp. herausbekommen?
ich hab immer noch keine richtige lösung gefunden
was soll ich denn jetzt als antwort hinschreiben 
ach ich bin so frustriert wegen dieser aufgabe   |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 03. Jan 2008 17:08 Titel: dermarkus Verfasst am: 03. Jan 2008 17:08 Titel: |
 |
|
Da hast du dich ein bisschen ablenken lassen von den Beiträgen seit Second_Qs Beitrag zwischendurch. Und du brauchst nicht ungeduldig auf eine Sofortlösung hoffen, Schritt für Schritt verstehst und schaffst du das viel besser 
Mach am besten da weiter, wo wir schon waren:
| dermarkus hat Folgendes geschrieben: | | Mudi hat Folgendes geschrieben: | Die Formel benutzt man wenn bei einem körper die masse (m) die Temp. steigt und die innere energie erhöht wird 
Die konstante für eis ist o,38 J/g*K und für Wasser 4,2 J/g*K
|
Prima 
Und woran sieht man in der Formel, um wieviel die Temperatur steigt?
| Zitat: |
Ich finde echt keine Formel für das eis schmelzen
|
Tipp: Hast du schon mal was von Schmelzwärme gehört? Findest du dazu etwas in deinem Heft oder in deinem Physikbuch?
// edit: oder dort  http://www.physikerboard.de/topic,10350,-definition-spezifische-schmelzwaerme.html#63604 http://www.physikerboard.de/topic,10350,-definition-spezifische-schmelzwaerme.html#63604
| Zitat: |
hmmm...also das wasser wird doch wärmer und was mit der energie passiert hab ich echt keine ahnung, hmmm...vllt wird die enrgie abgewandert
|
Du näherst dich der Sache 
Welches Wasser wird wärmer, welches wird kälter? Was passiert mit dem kalten Wasser, das aus dem Schmelzen des Eises entstanden ist? Und was passiert mit dem Wasser, das am Anfang das heiße Wasser bei 90°C war? Von wo nach wo wandert hier die Wärmeenergie? |
|
|
 |
darmon
Anmeldungsdatum: 12.11.2007
Beiträge: 23
|
 darmon Verfasst am: 03. Jan 2008 17:52 Titel: darmon Verfasst am: 03. Jan 2008 17:52 Titel: |
 |
|
|
beim eis mit 0°c sollte ein tm von 71,9°c rauskommen...... |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 03. Jan 2008 18:15 Titel: dermarkus Verfasst am: 03. Jan 2008 18:15 Titel: |
 |
|
| darmon hat Folgendes geschrieben: | | beim eis mit 0°c sollte ein tm von 71,9°c rauskommen...... |
Ich finde, dieser Einwurf ist vielleicht gut gemeint, aber leider nicht hilfreich. Denn erstens stimmt dieses Ergebnis nicht, und zweitens lenkt es vom Selber-Weiterüberlegen ab, wenn man irgendwas Fertiges serviert bekommt. Und es geht ja hier nicht darum, wie gut andere diese Aufgabe schaffen, sondern darum, Mudi dabei zu helfen, diese Aufgabe selbst zu schaffen.  |
|
 |
darmon
Anmeldungsdatum: 12.11.2007
Beiträge: 23
|
 darmon Verfasst am: 03. Jan 2008 19:01 Titel: darmon Verfasst am: 03. Jan 2008 19:01 Titel: |
 |
|
hab doch nur das ergebnis reingeschrieben, wie er diesen wert errechnen muss, sollte er schon selber herausfinden, aber um zu vergleichen ob er richtig liegt hilft das ganze schon.
ausserdem liegt doch die spezifische wärmekapazität von eis bei 2,1 J/g*k oder täusch ich mich da???? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 03. Jan 2008 19:19 Titel: dermarkus Verfasst am: 03. Jan 2008 19:19 Titel: |
 |
|
| Zitat: |
ausserdem liegt doch die spezifische wärmekapazität von eis bei 2,1 J/g*k oder täusch ich mich da???? |
Oh, danke, da hast du Recht,
das c von Eis ist tatsächlich 2,1 J/(g*K)
und nicht 0,38 J/(g*K), denn das wäre viel eher das c von Kupfer.
| darmon hat Folgendes geschrieben: | hab doch nur das ergebnis reingeschrieben, wie er diesen wert errechnen muss, sollte er schon selber herausfinden, aber um zu vergleichen ob er richtig liegt hilft das ganze schon.
|
Na, das falsche Ergebnis hilft ja leider selbst zu Vergleichszwecken nichts, und selbst wenn es richtig wäre, ein richtiges Ergebnis vor Augen lenkt viele leider sehr vom Selberdenken ab. |
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 04. Jan 2008 13:23 Titel: Mudi Verfasst am: 04. Jan 2008 13:23 Titel: |
 |
|
upppss sry  da hab ich falsch geguckt da hab ich falsch geguckt 
also was soll ich jetzt machen? ich weiss garnicht was ich jetzt als antwort schreiben muss  wie soll ich jetzt weiter machen? wie soll ich jetzt weiter machen?
ich hab nur paar tage zeit dann is schluss *waaaaaaaaaaaah*
 |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 04. Jan 2008 13:51 Titel: Mudi Verfasst am: 04. Jan 2008 13:51 Titel: |
 |
|
okay dann mach ich das mal
also ich benutze dann mal diese formel
W=c*m*deltaT
2,1 J/g*K * 100g * 90°C = 18900 J
richtig?
muss ich hier für deltaT 90°C oder 0°C einsetzten?
okay und jetzt?
thx |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 04. Jan 2008 14:08 Titel: dermarkus Verfasst am: 04. Jan 2008 14:08 Titel: |
 |
|
| Mudi hat Folgendes geschrieben: |
also ich benutze dann mal diese formel
W=c*m*deltaT
|
Hoppla, Vorsicht, diese Formel hat aber gar nichts mit dem Schmelzen von Eis zu tun. Das hier war die Formel für das Erwärmen.
--------------------------
Für das Schmelzen von Eis brauchst du das mit der Schmelzwärme (klick mal auf den Link zu deinem anderen Thread!) |
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 04. Jan 2008 14:10 Titel: Mudi Verfasst am: 04. Jan 2008 14:10 Titel: |
 |
|
häää?? da gibt es doch aber keine formel  |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 04. Jan 2008 14:38 Titel: dermarkus Verfasst am: 04. Jan 2008 14:38 Titel: |
 |
|
Aber genug Informationen  Wenn du die verstanden hast, dann ist die Rechnung so übersichtlich, dass ich glaube, dass du da nicht mal eine Formel dafür brauchst Wenn du die verstanden hast, dann ist die Rechnung so übersichtlich, dass ich glaube, dass du da nicht mal eine Formel dafür brauchst 
Weißt du denn schon, wieviel Energie man braucht, um 1 kg Eis zu schmelzen? |
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 04. Jan 2008 15:44 Titel: Mudi Verfasst am: 04. Jan 2008 15:44 Titel: |
 |
|
Ja da hast du schon recht! 
ok aber wie soll jetzt weitervorgehen um auf ne rechnung und ne lösung zu kommen 
ich finde aber keine rechnung für schmelzen  was soll ich machen? was soll ich machen?
ok ich schreib jetzt mal auf was ich weiss:
1. Das eis wird aufjedenfall schmelzen
2. Beim heißen wird die temp. sinken (Vermutung)
3. c für eis: 2,1 J/g*K und c Wasser = 4,2 J/g*K
4. keine ahnung was mit der energie passiert
wie soll ich jetzt ne rechnung haben oder ne lösung?
thx |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 04. Jan 2008 16:50 Titel: dermarkus Verfasst am: 04. Jan 2008 16:50 Titel: |
 |
|
| Mudi hat Folgendes geschrieben: |
ok aber wie soll jetzt weitervorgehen um auf ne rechnung und ne lösung zu kommen 
|
Ich schlage vor: 2 Sachen.
------------------
Zum einen überlegen wir uns, wie das mit dem Schmelzen ist. Das machen wir drüben in deinem anderen Thread, und zwar so lange, bis wir herausgefunden haben, wieviel Energie man braucht, um 100 g Eis zu schmelzen.
| Zitat: |
ich finde aber keine rechnung für schmelzen  was soll ich machen? was soll ich machen?
|
--> das machen wir dort weiter: http://www.physikerboard.de/ptopic,63601,.html#63601
------------------
Und zum anderen machen wir hier weiter, um die Sache so gut zu verstehen, dass wir anfangen können, den Rest zu rechnen:
| Zitat: |
ok ich schreib jetzt mal auf was ich weiss:
1. Das eis wird aufjedenfall schmelzen
2. Beim heißen wird die temp. sinken (Vermutung)
3. c für eis: 2,1 J/g*K und c Wasser = 4,2 J/g*K
|
Prima, damit bin ich einverstanden  Lass uns das nehmen, um weiterzudenken: Lass uns das nehmen, um weiterzudenken:
* Wer sorgt dafür, dass das Eis schmilzt? Woher kommt die Energie für das Schmelzen?
* Wer sorgt dafür, dass das heiße Wasser abkühlt? Wer klaut dem heißen Wasser da die Energie? |
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 04. Jan 2008 22:51 Titel: Mudi Verfasst am: 04. Jan 2008 22:51 Titel: |
 |
|
Okay 
Das eis schmiltzt doch wegen dem heißen wasser, oder?
Mit dieser Energie sache versteh ich es noch net so ganz...
Das Eis sorgt dafür dass das heiße wasser sich abkühlt.
Das Eis klaut die energie.
das sind meine vermutungen  |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 04. Jan 2008 23:08 Titel: dermarkus Verfasst am: 04. Jan 2008 23:08 Titel: |
 |
|
Einverstanden  Von wo nach wo wandert da also Wärmeenergie? Von wo nach wo wandert da also Wärmeenergie? |
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 04. Jan 2008 23:17 Titel: Mudi Verfasst am: 04. Jan 2008 23:17 Titel: |
 |
|
|
ähm... vom heißen wasser > eis |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 04. Jan 2008 23:50 Titel: dermarkus Verfasst am: 04. Jan 2008 23:50 Titel: |
 |
|
Einverstanden, da wandert Wärmeenergie vom heißen Wasser zum Eis:
Das heiße Wasser gibt Wärmeenergie ans Eis ab und wird dadurch kälter,
das Eis nimmt Wärmeenergie auf und schmilzt dadurch.
Wieviel Wärmeenergie gibt also das heiße Wasser dabei ab? |
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 05. Jan 2008 12:47 Titel: Mudi Verfasst am: 05. Jan 2008 12:47 Titel: |
 |
|
ok
ähm hä? vllt 4,2 KJ oder 2,1 KJ?  |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 05. Jan 2008 14:21 Titel: dermarkus Verfasst am: 05. Jan 2008 14:21 Titel: |
 |
|
Na, Zahlen kennen wir dazu bisher noch nicht.
Aber was wir jetzt schon sagen können, ist, dass das die Wärmeenergie, die das heiße Wasser an das Eis abgibt, genausogroß ist wie die Wärmeenergie, die das Eis aus dem heißen Wasser aufnimmt, um zu Schmelzen.
Einverstanden? |
|
 |
ForeverMassari
Anmeldungsdatum: 05.01.2008
Beiträge: 2
|
 ForeverMassari Verfasst am: 05. Jan 2008 14:24 Titel: ForeverMassari Verfasst am: 05. Jan 2008 14:24 Titel: |
 |
|
Du kannst vom Glück reden dass ich am Montag eine Physik-Arbeit schreiben werde und gerade im Internet nach Aufgaben zur Berechnung der Mischungstemperatur gesucht habe, weil mein Buch nicht so viele anzubieten hat.
Also jetzt zu deiner Aufgabe, die berechnet man so:
Das Eis nimmt ja die Wärmeenergie auf, also
(v = Mischungstemperatur)
W(auf)= 2,1 Kj / Kg*K * 0,1 kg * (v - 0°C)
W(ab) = 4,18 Kj / Kg*K * 0,2 kg * (90°C - v)
W(auf) = W(ab)
Ich habe dir jetzt nur den Ansatz aufgeschrieben, den Rest musst du wohl selber machen, weil wenn ich dir die ganze Lösung aufschreibe, hast du nichts von, sonst lernst du es ja nicht.   
Falls du noch Fragen hast, dann einfach schreiben |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 05. Jan 2008 14:29 Titel: dermarkus Verfasst am: 05. Jan 2008 14:29 Titel: |
 |
|
Entschuldige, ForeverMassari, dein Ansatz stimmt leider nicht, denn das Eis schmilzt ja und wird zu Wasser, sobald man versucht, es auf Temperaturen über 0°C zu erwärmen.
Und eine kleine Frage an dich: Hast du schon eine Vermutung, warum ich hier gerade so viel Zeit investiere, Mudi zu helfen, die Sache selbst zu verstehen und selbst Ansätze zu finden, anstatt einfach nur irgendwelche fertigen Lösungen oder Teillösungen oder fertige Ansätze hinzuschreiben? |
|
 |
ForeverMassari
Anmeldungsdatum: 05.01.2008
Beiträge: 2
|
 ForeverMassari Verfasst am: 05. Jan 2008 14:32 Titel: ForeverMassari Verfasst am: 05. Jan 2008 14:32 Titel: |
 |
|
Er muss ja erst die Mischungstemperatur berechnen. Und danach berechnen dass das eis schmilzt und so..
Also ich hätte es so gemacht. |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 05. Jan 2008 14:37 Titel: dermarkus Verfasst am: 05. Jan 2008 14:37 Titel: |
 |
|
Es ist gerade ein bisschen schwierig, das hier zu erklären, ohne für Mudi schon etwas vorwegzunehmen.
Aber deine Reihenfolge führt zu keinem richtigen Ergebnis.
Wir werden hier vielmehr zuerst das Schmelzen des Eises und was dabei passiert berechnen, und dann danach die Mischungstemperatur berechnen, die sich beim Mischen des kalten Wassers von 0°C (das aus dem Schmelzen des Eises entstanden ist) und des warmen Wassers (das während des Schmelzens durch Abkühlen aus dem heißen Wasser entstanden ist) einstellt. |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 05. Jan 2008 18:09 Titel: dermarkus Verfasst am: 05. Jan 2008 18:09 Titel: |
 |
|
|
Magst du nun, da wir das drüben mit der Schmelzwärme geklärt haben, mal hier zusammenfassen, was du bis jetzt alles weißt, und was du damit im nächsten Schritt berechnen könntest? |
|
 |
Mudi
Anmeldungsdatum: 01.01.2008
Beiträge: 68
|
 Mudi Verfasst am: 05. Jan 2008 18:23 Titel: Mudi Verfasst am: 05. Jan 2008 18:23 Titel: |
 |
|
okiii
also ich weiss jetzt dass ich 34 KJ Energie brauch um 100 g. eis zu schmelzen.
aber was bringt mir des die mischungstemp. heurauszufinden? naja ok
die energie geht vom heißen wasser zum den 100g Eis und wird so schmelzen wegen der enrgiezufuhr.
so
lg |
|
 |
|
















 könntet ihr mir bitte hier weiter helfen
könntet ihr mir bitte hier weiter helfen 



 xD
xD









