| Autor |
Nachricht |
as_string
Moderator

Anmeldungsdatum: 09.12.2005
Beiträge: 5791
Wohnort: Heidelberg
|
 as_string Verfasst am: 08. Mai 2007 01:49 Titel: Was löst sich schneller in Wasser? Zucker oder Salz? as_string Verfasst am: 08. Mai 2007 01:49 Titel: Was löst sich schneller in Wasser? Zucker oder Salz? |
 |
|
Hallo!
Eine Freundin von mir macht zur Zeit ein Praktikum in einem Kindergarten. Sie soll dort mit den Kindern (5 Jahre alt) einfache Versuche durchführen, um ihnen ein frühes Grundverständnis von einfachen Tatsachen der Natur zu ermöglichen. Sie hat dafür eine ganze "Liste" von möglichen Versuchen bekommen. Es geht wohl hauptsächlich um Aggregatszustände (erstmal), z. B. dass um uns herum nicht "nichts" ist, sondern Luft, die z. B. Wasser verdrängen kann (ein leeres Glas umgedreht in ein Wasserbecken--> Glas bleibt leer beim Untertauchen, weil es gar nicht "leer" ist, sondern schon Luft drin). usw.
Bei einem der Versuche hat sie mich dann gefragt:
"Warum löst sich Zucker schneller in Wasser, als Salz?" (dass es so sei, steht in der Beschreibung, nur nicht die Erklärung, die sie aber den Kids geben muss)
Ich erstmal: "Ich würde eher sagen, dass sich Salz schneller löst??!?"  . Wenn ich manchmal so den Zuckersatz in meinem Kaffee anschaue... . Wenn ich manchmal so den Zuckersatz in meinem Kaffee anschaue...
Naja: Ich wusste es nicht wirklich. Am Lösungsvorgang an sich kann es mE nicht wirklich liegen. Man sollte zumindest mehr Kochsalz in Wasser lösen können, als Zucker. Ich nehme das einfach mal so an, weil ja Salz in entsprechende Ione zerfällt, während Zucker eher große organische Moleküle sind, keine Ahnung. Schneller scheint es deshalb aber nicht zu gehen...
Das einzige, was mir eingefallen ist, war, dass ich der Ansicht bin, dass es an der Oberflächengröße liegen könnte. Salz ordnet sich ja ziemlich regelmäßig im Gitter an und hat dadurch eine recht glatte Oberfläche. Selbst wenn es "pulvrig" ist, werden die kleinen Pulverkörner sicher eine für ihr Gewicht recht kleine Oberfläche haben, schätze ich. Bei Zucker ist die wahrscheinlich viel größer, weil kein so schönes, regelmäßiges Gitter entsteht.
Aber ob es das wirklich ist?
Ich persönlich finde den Versuch ja für Kids in dem Alter wirklich übertrieben. Ich glaube nicht, dass man mit 5 so was verstehen kann. Ich würde da erst mit Dingen anfangen, die sie mit ein wenig Hilfe mehr oder weniger selbst rausbekommen können. Bei Salz und Zucker hat man mit 5 doch überhaupt keine Vorstellung und wie das mit Lösen in einem Lösungsmittel "funktioniert" schon mal gar nicht. Ist ja letztendlich auch ein wirklich komplizierter Prozess, besonders wenn es recht unterschiedlich abläuft, wie bei Zucker und Wasser, oder?
Würde mich freuen über ein paar Gedanken von Euch zu dem Thema!
Gruß
Marco |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 08. Mai 2007 02:54 Titel: dermarkus Verfasst am: 08. Mai 2007 02:54 Titel: |
 |
|
Ich habe den Verdacht, dass die Ziel-Erkenntnis dieses Versuches sogar ein bisschen ungenau formuliert ist: Denn Zucker löst sich viel besser in Wasser als Salz (man kann viel mehr Zucker in derselben Menge Wasser auflösen als Salz), aber ob sich Zucker oder Salz schneller lösen, dürfte auch von der jeweils verwendeten Korngröße abhängen, solange man wenig genug Zucker und Salz nimmt, dass man locker das ganze Salz in der gegebenen Menge Wasser auflösen kann. (Bei einem Vergleich von Kandiszucker und fein zerstäubtem Salz dürfte es spannend werden.)
---------------------------------------------------------
Ich hab mal ein bisschen experimentiert:
Einen Teelöffel Zucker (Haushaltszucker "fein") in ein kleines Wasserglas geben, und einen Teelöffel Salz in ein zweites kleines Wasserglas. (Die Größe meiner Zuckerkörner ist sehr ähnlich wie die der Salzkörner, die Zuckerkörner sind eher ein kleines bisschen größer als die Salzkörner.) Und dann beide gleichzeitig rühren.
Schon nach kurzer Zeit (grob eine Minute) ließ sich der Zucker komplett verrühren, und die Flüssigkeit im Zuckerwasserglas war klar, und aller Zucker vom Boden des Glases war verrührt. Währenddessen war die Flüssigkeit im Salzwasserglas immer noch milchig trüb, erst als ich nach einigem weiteren vergeblichen Rühren angefangen habe, die Lösung deutlich zu verdünnen (einen Teil der Salz-"Emulsion" in eine Glasschale geben und zusätzliches Wasser hinzugießen), wurde das zu einer klaren Salzlösung.
Ich glaube, dass dieser schnelle Versuch bestätigt: Zucker löst sich deutlich besser in Wasser als Salz.
(Ich denke, um das Experimentieren der Kids vorzubereiten, lohnt es sich für die Praktikantin ganz sicher, selbst vorher intensiv auszuprobieren, welche Gefäßgrößen und welche Mengen oder Portionen an Zucker und Salz man am besten nehmen kann, und wie man am besten vorgehen kann (vielleicht in kleinen Portionen immer mehr Salz bzw Zucker dazukippen, bis es sich nicht mehr zu einer klaren Lösung verrühren lässt?), damit man den Effekt schön deutlich sieht. Vielleicht hängt so etwas ja auch vom Härtegrad des Leitungswassers in der jeweiligen Region ab!? )
---------------------------------------
Die Erklärung mit der unterschiedlichen Oberfläche kann hier wohl nicht alles erklären, denn in meinem Versuch waren die Korngrößen gleich oder sehr ähnlich groß. Damit kann man nur erklären, warum sich Puderzucker deutlich schneller in Wasser löst als Kandiszucker.
http://dc2.uni-bielefeld.de/dc2/grundsch/versuche/gs-v-048.htm
Wichtig für den Vergleich von Zucker und Salz dürfte vor allem sein, dass die Löslichkeit von Zucker in Wasser wesentlich größer ist als die von Salz.
http://www.chemie-entdecken-nrw.org/loes106.pdf
Denn die Ionen im Salzkristall haben eine deutlich höhere Bindungsenergie als die neutralen Zuckermoleküle im Zuckerkorn:
Salz löst sich viel schlechter in Wasser als Zucker, weil die Teilchen in den Salzkörnern viel fester zusammenhängen als die Teilchen in den Zuckerkörnern. |
|
 |
as_string
Moderator

Anmeldungsdatum: 09.12.2005
Beiträge: 5791
Wohnort: Heidelberg
|
 as_string Verfasst am: 08. Mai 2007 14:16 Titel: as_string Verfasst am: 08. Mai 2007 14:16 Titel: |
 |
|
Hallo Markus!
OK, es liegt also letztendlich an der größeren Bindungsenergie im Kochsalzkristall als in kristallinem Zucker.
Vielen Dank, auch für die anderen Typs! 
Ich werde es entsprechend weiter geben. Den Versuch an sich hat sie wohl schon ein paar mal selbst ausprobiert, von dieser Seite her sollte es also keine großen Überraschungen geben. Interessant wäre natürlich, wenn man die Kinder vielleicht in Zweiergruppen zusammenarbeiten lassen könnte und die Versuche dann die Kinder selbst machen lassen könnte. Ich weiß allerdings auch nicht, wie viele es insgesamt sind. Ich denke aber mal, dass sie diese Seite der Aufgabe ganz gut im Griff hat, so wie ich sie kenne. 
Sie soll jetzt erstmal diese Liste "abarbeiten" mit den vorgegebenen Versuchen. Sie hofft aber darauf, dass sie, wenn sie bewiesen hat, dass sie das ganz gut mit den Kids macht, danach auch eigene Ideen ausprobieren kann. Ich hatte da auch schon kleinere Ideen, was man da machen könnte, aber naja, erstmal abwarten, bis sie sie wirklich braucht. Ich komme dann nochmal auf Euch zurück, wenn es so weit ist. Ihr habt ja immer interessante Ideen für so was! 
Gruß
Marco |
|
 |
pressure
Anmeldungsdatum: 22.02.2007
Beiträge: 2496
|
 pressure Verfasst am: 09. Mai 2007 19:14 Titel: pressure Verfasst am: 09. Mai 2007 19:14 Titel: |
 |
|
|
Zucker oder auch D-Glucose ist ein Molekül, dass im Wasser meist als Halbaccetat vorkommt. Dieses ist in der Lage 6 !! Wasserstoffbrücken auszubauen und ist damit in Wasser perfekt lösbar, da Wasser genauso Wasserstoffbrücken ausbaut. Ein Salz hingegen ist im Wasser gespalten in Anionen und Kationen, die dann von den polaren Wassermolekülen umlagert werden. Damit ist ein Salz zwar auch in Wasser gut lösbar, Glucose aber um einiges besser, eben weil genau die gleichen Zwischenmolekularekräft am Werk sind und dies in 6-facher Ausführung. |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 10. Mai 2007 01:30 Titel: dermarkus Verfasst am: 10. Mai 2007 01:30 Titel: |
 |
|
Danke, pressure  , durch deinen Beitrag bin ich darauf aufmerksam geworden, dass unsere bisherige Antwort nur einen Teil dessen betrachtet hat, was hier wichtig zu sein scheint: , durch deinen Beitrag bin ich darauf aufmerksam geworden, dass unsere bisherige Antwort nur einen Teil dessen betrachtet hat, was hier wichtig zu sein scheint:
Ich bin mir noch nicht sicher, ob man aus dieser Überlegung für die Glucose (6 Wasserstoffbrücken pro gelöstem Glucosemolekül) folgern kann, dass die Hydratationsenergie von Glucose größer ist als die von Salz.
Denn es kommt ja noch darauf an, ob man die Hydratationsenergie pro mol oder zum Beispiel pro kg Glucose betrachtet, und ein Glucosemolekül ( ) wiegt mit 180 u deutlich mehr als NaCl (23 u + 35 u). Ich halte es deshalb noch nicht für ausgeschlossen, dass die Hydratationsenergie pro Masse für Salz größer oder ähnlich groß ist wie die für Glucose. ) wiegt mit 180 u deutlich mehr als NaCl (23 u + 35 u). Ich halte es deshalb noch nicht für ausgeschlossen, dass die Hydratationsenergie pro Masse für Salz größer oder ähnlich groß ist wie die für Glucose.
-------------------------------------------------
Für Salze habe ich Zahlenwerte für die Gitterenergie, Hydratationsenergie und Lösungswärme pro mol gefunden, siehe Seite 35 von 37 in
http://duepublico.uni-duisburg-essen.de/servlets/DerivateServlet/Derivate-11014/folie097-128.pdf
Da finde ich zum Beispiel, dass die Lösungswärme von KCl +13 kJ/mol beträgt, das heißt, beim Lösen von KCl in Wasser wird keine Wärmeenergie freigesetzt, sondern verbraucht. (Die dafür nötige Wärmeenergie wird dem Wasser entzogen, das heißt, das Wasser kühlt ab, während sich KCl in ihm löst.)
Dass sich das Salz trotzdem löst, liegt an der Entropiezunahme, die mit dem Lösungsvorgang verbunden ist.
(Die Lösungswärme = |Gitterenergie|-|Hydratationsenergie| ist also die Wärmeenergie, die für das Lösen aufgewendet werden muss; wenn sie positiv ist, dann kühlt die Lösung beim Lösen ab, wenn sie negativ ist, dann erwärmt sich die Lösung beim Lösevorgang.)
=============================================
Die Lösungswärme, also die Änderung der inneren Energie während des Lösungsvorganges, ist also nicht allein dafür entscheidend, ob und wie gut sich ein Stoff in Wasser löst! Entscheidend ist vielmehr eine Kombination aus Änderung der inneren Energie 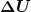 und Änderung der Entropie und Änderung der Entropie 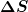 . Das ist die Änderung der freien Energie . Das ist die Änderung der freien Energie  : :

Siehe zum Beispiel
http://www.uni-koeln.de/math-nat-fak/anorgchem/meyer/aktuelles/pdf/aaac/12_Thermodynamik_II.pdf
unter anderem die Formeln auf Seite 18 des Links.
Für gute Löslichkeit (möglichst negatives  ) ist also förderlich: ) ist also förderlich:
- eine kleine Gitterenergie
- eine Hydratationsenergie mit großem Betrag
- (und folglich eine kleine Lösungswärme)
- eine große Entropiezunahme beim Lösungsvorgang
- eine hohe Temperatur
Um herauszufinden, ob die bessere Löslichkeit von Zucker gegenüber Salz tatsächlich von dem Unterschied in der Gitterenergie bestimmt wird, müssten wir also erst noch überprüfen, ob die Hydratationsenergien und die Entropiezunahmen vergleichbar groß sind.
Dazu wäre es natürlich schön, wenn wir noch Zahlen zur Gitterenergie und Hydratationsenergie von Zucker und zur Entropiezunahme beim Lösen von Salz und Zucker finden oder bestimmen könnten. |
|
 |
Gurkenklub.TV
Gast
|
 Gurkenklub.TV Verfasst am: 19. März 2021 13:39 Titel: Danke Gurkenklub.TV Verfasst am: 19. März 2021 13:39 Titel: Danke |
 |
|
|
Vielen Dank! Das konnte mir sogar bei den Chemie Hausaufgaben über Löslichkeit helfen! |
|
 |
rodyz
Anmeldungsdatum: 18.01.2024
Beiträge: 2
|
 rodyz Verfasst am: 18. Jan 2024 13:47 Titel: Bei mir löst sich (Koch-)Salz schneller rodyz Verfasst am: 18. Jan 2024 13:47 Titel: Bei mir löst sich (Koch-)Salz schneller |
 |
|
Ich mache Experimente mit Grundschülern. Bei mir war das Ergebnis umgekehrt. Das Salz hat sich schneller gelöst, sowohl bei den Schülern, als auch bei mir, weil ich das Ergebnis nicht glauben wollte.
Versuchsbedingungen: jeweils ein gestrichen voller Plastiklöffel (weniger als ein halber Teelöffel ) Haushaltssalz und brauner Rohrzucker.
Ich denke, bei diesem Versuch ist es schwer, identische Versuchsbedingungen herzustellen, insbesondere, was die Korngröße betrifft. Und vielleicht lag es bei mir auch an der Zuckerart brauner Rohrzucker. Ich werde das Experiment demnächst mit weißem Zucker wiederholen. |
|
 |
willyengland
Anmeldungsdatum: 01.05.2016
Beiträge: 715
|
 willyengland Verfasst am: 18. Jan 2024 16:20 Titel: willyengland Verfasst am: 18. Jan 2024 16:20 Titel: |
 |
|
Ja, ja ...
Trifft ein Experimentalphysiker einen Theoretiker auf dem Flur:
"Hier mein neuestes Messergebnis!" und hält dem Theoretiker ein Blatt mit der Messkurve hin.
Der schaut darauf und erklärt es.
Da sagt der Experimentalphysiker:
"Oh, Entschuldigung, ich habe es falsch rum gehalten!"
"Ach", sagt der Theoretiker, "das ist ja noch viel leichter zu erklären."
_________________
Gruß Willy |
|
 |
rodyz
Anmeldungsdatum: 18.01.2024
Beiträge: 2
|
 rodyz Verfasst am: 18. Jan 2024 17:34 Titel: Ergänzung rodyz Verfasst am: 18. Jan 2024 17:34 Titel: Ergänzung |
 |
|
Ergänzung:
Es waren 350 ml H2O.
PS: Ich gehöre zu den Wissenschaftlern, die Physik studiert hätten, wenn sie Mathe gekonnt hätte ;-).
Was hab ich studiert? |
|
 |
|
|
















 . Wenn ich manchmal so den Zuckersatz in meinem Kaffee anschaue...
. Wenn ich manchmal so den Zuckersatz in meinem Kaffee anschaue...


