| Autor |
Nachricht |
Duphy
Anmeldungsdatum: 26.09.2017
Beiträge: 5
|
 Duphy Verfasst am: 26. Sep 2017 12:08 Titel: Doppelkammer mit Gas Duphy Verfasst am: 26. Sep 2017 12:08 Titel: Doppelkammer mit Gas |
 |
|
Meine Frage:
Hallo 
Die Aufgabenstellung lautet:
Eine Zylinderkammer der Länge d (horizontal liegend) ist in zwei gleich große Kammern aufgeteilt, die durch eine bewegliche Trennwand separiert werden. In beiden Teilkammern ist am Anfang der gleiche Druck, das gleiche Volumen und die gleiche Temperatur vorhanden. Nun wird der ersten (linken) Kammer eine Wärmeenergie Q zugeführt wodurch die zweite Kammer nun den Druck  hat. Die Fragen sind: hat. Die Fragen sind:
a) Wie viel Arbeit  wurde der zweiten Kammer zugeführt wurde der zweiten Kammer zugeführt
b) Was sind jeweils die Endtemperaturen in den Kammern
c) Welche Wärme  wurde der linken Kammer zugeführt. wurde der linken Kammer zugeführt.
Gegeben ist: 
Meine Ideen:
Da es sich in der 2 Kammer um eine adiabatische Kompression handelt, kann ich durch  das Volumen der rechten Kammer bestimmen und mit das Volumen der rechten Kammer bestimmen und mit ^{\kappa-1} ) die Temperatur. die Temperatur.
Ich verstehe aber nicht wie ich die Arbeit in der 2 Kammer bestimme. Der Druck in der 1 Kammer müsste ja auch  betragen damit auf die Trennwand keine Kraft wirkt, auch hier weiß ich nicht wie ich für die Wärmeenergie ansetzten soll bzw. um welche Zustandsänderung es sich handelt. betragen damit auf die Trennwand keine Kraft wirkt, auch hier weiß ich nicht wie ich für die Wärmeenergie ansetzten soll bzw. um welche Zustandsänderung es sich handelt.
Ist die berechnete Temperatur  auch die richtige Teillösung für die Frage b) ? auch die richtige Teillösung für die Frage b) ?
Schonmal vielen Dank für die Hilfe  |
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 26. Sep 2017 13:44 Titel: Myon Verfasst am: 26. Sep 2017 13:44 Titel: |
 |
|
Willkommen im Forum
Zu b) Du hast ja noch nicht nach 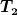 aufgelöst, aber ja, über die Adiabatengleichungen kann die Temperatur bestimmt werden. aufgelöst, aber ja, über die Adiabatengleichungen kann die Temperatur bestimmt werden.
Zu a) Die beim adiabatischen Prozess zugeführte Arbeit ist

Zu c) Bekannt sind  . Damit ergibt sich über die Zustandsgleichung für id. Gase auch . Damit ergibt sich über die Zustandsgleichung für id. Gase auch  . Mit der Temperatur lässt sich die innere Energie in der Kammer 1 bzw. deren Änderung bestmmen ( . Mit der Temperatur lässt sich die innere Energie in der Kammer 1 bzw. deren Änderung bestmmen ( , wenn , wenn 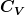 die auf die Masse bezogene spez. Wärmekapazität ist). Die zugeführte Wärme ist dann die Summe aus der Änderung der inneren Energie plus der Arbeit, die das Gas während der Expansion leistet. die auf die Masse bezogene spez. Wärmekapazität ist). Die zugeführte Wärme ist dann die Summe aus der Änderung der inneren Energie plus der Arbeit, die das Gas während der Expansion leistet. |
|
 |
Duphy
Anmeldungsdatum: 26.09.2017
Beiträge: 5
|
 Duphy Verfasst am: 26. Sep 2017 14:17 Titel: Danke für die Antwort Duphy Verfasst am: 26. Sep 2017 14:17 Titel: Danke für die Antwort |
 |
|
Danke für die Antwort, wollte nochmal paar Sachen nachfragen.
Meintest du für die b) mit  die Werte nachdem ich die Wärmeenergie zugeführt habe? Das wäre dann die Werte nachdem ich die Wärmeenergie zugeführt habe? Das wäre dann  und für und für  betrachte ich die Volumenänderung in der 2 Kammer betrachte ich die Volumenänderung in der 2 Kammer  ) . Dann über . Dann über  die Temperatur ermitteln, die Differenz der Temperaturen bilden und die Temperatur ermitteln, die Differenz der Temperaturen bilden und  bestimmen. Habe ich das richtig Verstanden? bestimmen. Habe ich das richtig Verstanden?
Wie kommt man bei der a) auf die Formel für die Arbeit? Ich hatte sowas ähnliches gefunden mit p(V) aber dann würde das Volumen in einem log stecken.
Wie gesagt nochmal vielen Dank  |
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 26. Sep 2017 20:07 Titel: Re: Danke für die Antwort Myon Verfasst am: 26. Sep 2017 20:07 Titel: Re: Danke für die Antwort |
 |
|
Entschuldige bitte die späte Antwort.
| Duphy hat Folgendes geschrieben: | Meintest du für die b) mit  die Werte nachdem ich die Wärmeenergie zugeführt habe? Das wäre dann die Werte nachdem ich die Wärmeenergie zugeführt habe? Das wäre dann  und für und für  betrachte ich die Volumenänderung in der 2 Kammer betrachte ich die Volumenänderung in der 2 Kammer  ) . Dann über . Dann über  die Temperatur ermitteln, die Differenz der Temperaturen bilden und die Temperatur ermitteln, die Differenz der Temperaturen bilden und  bestimmen. Habe ich das richtig Verstanden? bestimmen. Habe ich das richtig Verstanden? |
Ja, das habe ich so gemeint. Nur dass das m in der von Dir erwähnten Form der Zustandsgleichung dann die Anzahl Mol sein muss. Falls das gegebene m tatsächlich eine Masse ist, so müsste auch die molare Masse des Gases bekannt sein und durch diese dividiert werden, um die Anzahl Mol zu erhalten.
| Zitat: | | Wie kommt man bei der a) auf die Formel für die Arbeit? Ich hatte sowas ähnliches gefunden mit p(V) aber dann würde das Volumen in einem log stecken. |
Mit  : :
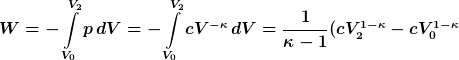=\frac{p_2V_2-p_0V_0}{\kappa-1}) |
|
 |
|
|
















