| Autor |
Nachricht |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 17. Jul 2017 21:55 Titel: Adiabat isentrop? Zustandsgleichung ideales Gas Silver1 Verfasst am: 17. Jul 2017 21:55 Titel: Adiabat isentrop? Zustandsgleichung ideales Gas |
 |
|
Hey,
ich wollte Fragen was genau der Unterschied zwischen adiabat & adiabat isentrop ist,
Ich habe folgende Aufgabe ;
Ein ideales Gas im Zustand p0=1bar und T0=270
C wird adiabat (isentrop) auf ein Zehntel seines Ausgangsvolumens
komprimiert.
Wie ändern sich Temperatur und der Druck des Gases?
Skizzieren Sie den Prozess und typische Isothermen in einem P-V-Diagramm!
Hinweis: 𝑝v =NRT, R=8,314 J/molK , 𝑝𝑉𝜅 = konstant, κ=1,4
Mein Problem:
Ich muss V0 raus finden aber ohne N weiß ich nicht genau wie ich das hinbekomme. Ich habe die Information 𝑝𝑉𝜅 = konstant gegeben, die ich nicht ganz verstehe.
Könnt ihr mir bei dem Ansatz helfen wie ich auf V0 komme ?
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 18. Jul 2017 10:54 Titel: Myon Verfasst am: 18. Jul 2017 10:54 Titel: |
 |
|
Wieso benötigst Du für die Aufgabenstellung das Ausgangsvolumen? Die Temperatur und der Druck ändern sich gemäss den Adiabatengleichungen

Damit kannst Du den Prozess auch im pV-Diagramm einzeichnen (für die Isotherme gilt demgegenüber pV=const.; überlege, ob die Isotherme steiler oder flacher verläuft als die Adiabatenkurve).
|
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 18. Jul 2017 11:12 Titel: Silver1 Verfasst am: 18. Jul 2017 11:12 Titel: |
 |
|
| Myon hat Folgendes geschrieben: | Wieso benötigst Du für die Aufgabenstellung das Ausgangsvolumen? Die Temperatur und der Druck ändern sich gemäss den Adiabatengleichungen

Damit kannst Du den Prozess auch im pV-Diagramm einzeichnen (für die Isotherme gilt demgegenüber pV=const.; überlege, ob die Isotherme steiler oder flacher verläuft als die Adiabatenkurve). |
Hey, danke für deine Antwort. Leider stehe ich allgemein dabei auf den Schlauch weil ich z.B auch nicht weiß wie ich sie in ein PV Diagramm einzeichnen soll ..
Das die Gleichung konstant ist bedeutet doch das

und dann muss ich die Gleichung umstellen um auf die Temperatur bzw auf den Druck zu kommen ?
sorry aber mit den Aufgabentyp habe ich wirklich Schwierigkeiten 
Zuletzt bearbeitet von Silver1 am 18. Jul 2017 12:47, insgesamt einmal bearbeitet |
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 18. Jul 2017 12:46 Titel: Myon Verfasst am: 18. Jul 2017 12:46 Titel: |
 |
|
Genau. Es gilt

Die erste Gleichung löst Du nach T1 auf, die zweite nach p1. Dann brauchst Du nur noch einzusetzen.
Was das pV-Diagramm angeht: Für eine Isotherme gilt pV=const., p ist somit proportioal zu 1/V. Isothermen haben also im pV-Diagramm die Form von Hyperbeln. Eine Adiabate ist dagegen steiler, da  . .
Eine Isotherme und eine Adiabate siehst Du in diesem Diagramm in der Wikipedia.
Für die Aufgabe zeichnest Du einfach noch ein paar Isothermen mehr ein (grösserer Abstand vom Ursprung, sozusagen weiter rechts oben).
|
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 18. Jul 2017 12:53 Titel: Silver1 Verfasst am: 18. Jul 2017 12:53 Titel: |
 |
|
| Myon hat Folgendes geschrieben: | Genau. Es gilt

Die erste Gleichung löst Du nach T1 auf, die zweite nach p1. Dann brauchst Du nur noch einzusetzen.
Was das pV-Diagramm angeht: Für eine Isotherme gilt pV=const., p ist somit proportioal zu 1/V. Isothermen haben also im pV-Diagramm die Form von Hyperbeln. Eine Adiabate ist dagegen steiler, da  . .
Eine Isotherme und eine Adiabate siehst Du in diesem Diagramm in der Wikipedia.
Für die Aufgabe zeichnest Du einfach noch ein paar Isothermen mehr ein (grösserer Abstand vom Ursprung, sozusagen weiter rechts oben). |
Vielen Dank für deine Antwort ich werde es jetzt nochmal Versuchen.
Eine Frage hätte ich noch, eigentlich ist ja nur folgende Gleichung gegeben:

Woher weiß ich das diese dann auch konstant ist ?

Meine Vermutung wäre das es 3 Formeln für ein adiabates system gibt und wenn eine davon konstant ist sind die anderen es automatisch auch liege ich da richtig ?
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 18. Jul 2017 13:06 Titel: Myon Verfasst am: 18. Jul 2017 13:06 Titel: |
 |
|
Ja, es gibt 3 Gleichungen für den Zusammenhang von p und V, T und V sowie T und p bei einem adiabatischen Prozess.
Die erwähnte Gleichung für V und T ergibt sich aus der Zustandsgleichung für ideale Gase nach einer Integration, siehe z.B. die Herleitung hier.
|
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 18. Jul 2017 13:29 Titel: Silver1 Verfasst am: 18. Jul 2017 13:29 Titel: |
 |
|
So ich habe die Aufgabe mal versucht zu rechnen. Ich bin mir jedoch nicht sicher ob ich bar nehmen muss oder bar in Pascal umrechnen muss ?
Ist es so richtig ?
Danke für deine Hilfe !
Bild aus externem Link als Anhang eingefügt. Bitte keine externen Links verwenden. Steffen
| Beschreibung: |
|
| Dateigröße: |
363.05 KB |
| Angeschaut: |
6338 mal |

|
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 18. Jul 2017 13:39 Titel: Myon Verfasst am: 18. Jul 2017 13:39 Titel: |
 |
|
|
Hier musst Du nicht in Pascal umrechnen. Der Druck ist richtig, bei der Temperatur haben sich beim Rechnen auf der 4. und 5. Zeile Fehler eingeschlichen.
|
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 18. Jul 2017 13:45 Titel: Silver1 Verfasst am: 18. Jul 2017 13:45 Titel: |
 |
|
|
Ich habe beim aufschreiben das ^k-1 vergessen aber im Taschenrechner habe ich es eingetippt das meinst du oder ?
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 18. Jul 2017 14:01 Titel: Myon Verfasst am: 18. Jul 2017 14:01 Titel: |
 |
|
Ja. Aber der Faktor T_0 ist dabei ohne diesen Exponent.
Im Übrigen: schon gefühlsmässig hätte das Resultat etwas stören sollen. Bei einer adiabatischen Kompression muss die Temperatur steigen. Vgl. das schnelle Aufpumpen eines Reifens, wo keine Zeit bleibt für einen Wärmeaustausch.
|
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 18. Jul 2017 14:22 Titel: Silver1 Verfasst am: 18. Jul 2017 14:22 Titel: |
 |
|
Okey ich habe nun nochmal Umgeformt und komme auf :
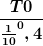
Also hoch 0,4 weil k-1 0,4 ergibt
Als Ergebnis habe ich nun 753K raus kann das sein?
Und beim Druck habe ich das selbe Spiel falsch gemacht oder ?
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 18. Jul 2017 14:25 Titel: Myon Verfasst am: 18. Jul 2017 14:25 Titel: |
 |
|
|
Ja, T1=753K ist richtig. Der Druck sollte stimmen (ist hier aber offenbar glücklicher Zufall, da p0=1 bar...).
|
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 18. Jul 2017 15:00 Titel: Myon Verfasst am: 18. Jul 2017 15:00 Titel: |
 |
|
Den ersten Hauptsatz brauchst Du hier eigentlich gar nicht. Für die zugeführte Wärme gilt im isochoren Fall

Im isobaren Fall ist mit  statt mit statt mit 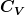 zur rechnen (nur für die Wärme!). Aus dem Hinweis zur rechnen (nur für die Wärme!). Aus dem Hinweis  kannst Du kannst Du 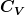 herauslesen. herauslesen.
|
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 18. Jul 2017 15:17 Titel: Silver1 Verfasst am: 18. Jul 2017 15:17 Titel: |
 |
|
Hmm aber es gab doch eine alternative zum rechnen oder ? Ich habs jetzt so gemacht komme aber nun nicht mehr weiter
ich habe für die Arbeit -1662,8J raus und deltaE 4157J
also hätte ich für Isobar 5819 J raus ?
aber für Isochor wüsste ich dann nicht wie ich auf das Ergebnis komme
Ich meinte mal von jemanden gehört zu haben das bei Isochor die Arbeit immer = 0 ist stimmt das ?
| Beschreibung: |
|
Download |
| Dateiname: |
9114c386-7ad5-4365-b376-85d7a6a216b7.jpg |
| Dateigröße: |
133.25 KB |
| Heruntergeladen: |
590 mal |
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 18. Jul 2017 15:51 Titel: Myon Verfasst am: 18. Jul 2017 15:51 Titel: |
 |
|
Ja, die zugeführte Wärme im isobaren Fall ist richtig.
Bei einem isochoren Prozess ist die Arbeit =0, ja, denn es gilt ja dW=-p*dV (und dV=0, da das Volumen nicht ändert).
Die zugeführte Wärme ist also genau gleich der Zunahme der inneren Energie, die Du schon berechnet hast.
Damit ist nur noch die Frage nach dem Grund für den unterschiedlichen Wärmebedarf zu beantworten. Das kannst Du anhand der Gleichung dE=dQ+dW (oder wie in der Aufgabe: E=Q+A) überlegen.
|
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 18. Jul 2017 15:57 Titel: Silver1 Verfasst am: 18. Jul 2017 15:57 Titel: |
 |
|
| Myon hat Folgendes geschrieben: | Ja, die zugeführte Wärme im isobaren Fall ist richtig.
Bei einem isochoren Prozess ist die Arbeit =0, ja, denn es gilt ja dW=-p*dV (und dV=0, da das Volumen nicht ändert).
Die zugeführte Wärme ist also genau gleich der Zunahme der inneren Energie, die Du schon berechnet hast. |
Und daher muss beim Isobaren Prozess mehr Arbeit verrichtet werden, daher entsteht auch ein größerer Wärmebedarf.
So richtig ?
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 18. Jul 2017 16:14 Titel: Myon Verfasst am: 18. Jul 2017 16:14 Titel: |
 |
|
|
Ja. Beim isobaren Prozess muss -damit der Druck konstant bleibt- das Volumen zunehmen. Beim isobaren Prozess muss deshalb mehr Wärme zugeführt werden, da die Wärme nicht nur zur Erhöhung der inneren Energie benötigt wird, sondern ein Teil auch für die Volumenarbeit "verbraucht" wird.
|
|
 |
|

















