| Autor |
Nachricht |
stereo
Anmeldungsdatum: 27.10.2008
Beiträge: 402
|
 stereo Verfasst am: 06. Jan 2009 14:09 Titel: Kritische Größen des van-der-Waals-Gases [ideales Gaß] stereo Verfasst am: 06. Jan 2009 14:09 Titel: Kritische Größen des van-der-Waals-Gases [ideales Gaß] |
 |
|
Hallo  Gesundes neues Jahr wünsch ich euch noch Gesundes neues Jahr wünsch ich euch noch
Aufgabe 1:
Bestimmen Sie den kritischen Druck, die kritische Temperatur und das kritische Volumen für 1 Mol eines Van-der-Waals-Gases. Berechnen Sie diese Größen für Sauerstoff 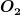 mit: mit:



Jetzt hab ich in meinem Buch nachgelesen, was denn eigentlich diese kritischen Größen aussagen, habe aber nur eine Tabelle gefunden, wo diese verzeichnet sind.
Ich vermute jetzt dass die kritischen Größen mit dem Phasenwechsel zusammenhängen. Also wenn die Isotherme Maximum, sowie Minimum besitzt. Da wäre ich mir aber jetzt unsicher welcher Druck denn nun der kritische ist, bzw welches Volumen. |
|
 |
stereo
Anmeldungsdatum: 27.10.2008
Beiträge: 402
|
 stereo Verfasst am: 06. Jan 2009 15:23 Titel: stereo Verfasst am: 06. Jan 2009 15:23 Titel: |
 |
|
Ok, ich weiß jetzt was der kritische Punkt ist. Wikipedia sei Dank.
Daraufhin habe ich jetzt auch den richtigen Abschnitt im Buch gefunden und glaube ich kann die Aufagebe jetzt lösen 
Jedoch habe ich eine mathematische Frage,
was bedeutet dieser Ausdruck:
_{T_k , V_k} = 0 \text{ und } \left( \frac{\delta^2 p}{\delta V^2} \right)_{T_k , V_k} = 0) |
|
 |
stereo
Anmeldungsdatum: 27.10.2008
Beiträge: 402
|
 stereo Verfasst am: 06. Jan 2009 16:20 Titel: stereo Verfasst am: 06. Jan 2009 16:20 Titel: |
 |
|
Ich suche ja jetzt den Wendepunkt, haben die 2 partiellen Ableitung was damit zu tun?
In meinem Buch steht, dass diese beiden Gleichung erfüllt sein müssen. Ich habe aber noch nie mit partiellen Ableitungen gearbeitet und kann mir unter den Ausdrücken nichts vorstellen. |
|
 |
Hagbard

Anmeldungsdatum: 07.02.2006
Beiträge: 320
Wohnort: Augsburg
|
 Hagbard Verfasst am: 06. Jan 2009 16:23 Titel: Hagbard Verfasst am: 06. Jan 2009 16:23 Titel: |
 |
|
Die beiden DGLs, bedeuten, dass sich am kritischen Punkt (bei der kritischen Temperatur Tk und dem kritischen Volumen Vk) die erste und zweite Ableitung der Funktion p(V) verschwindet. Was die erste und die zweite Ableitung einer Funktion mathematisch bedeuten weißt du ja sicher.
Gruß
_________________
Immer schön die Kirche im Dorf lassen... und dann in die Stadt ziehen. |
|
 |
stereo
Anmeldungsdatum: 27.10.2008
Beiträge: 402
|
 stereo Verfasst am: 06. Jan 2009 16:44 Titel: stereo Verfasst am: 06. Jan 2009 16:44 Titel: |
 |
|
Also das Maximum und das Minimum exisitert ja nur mathematisch, eigentlich gibt es nur einen Druck.
Aber genau hab ich das jetzt nicht verstanden mit dem 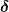 . .
Es geht mir hier auch mehr um das Allgemeine, als um die Gleichung. Ich kann mit dem Ausdruck an sich nichts anfangen.
Und wikipedia hilft mir hier grad nicht wirklich. |
|
 |
Hagbard

Anmeldungsdatum: 07.02.2006
Beiträge: 320
Wohnort: Augsburg
|
 Hagbard Verfasst am: 06. Jan 2009 16:54 Titel: Hagbard Verfasst am: 06. Jan 2009 16:54 Titel: |
 |
|
| stereo hat Folgendes geschrieben: | Also das Maximum und das Minimum exisitert ja nur mathematisch, eigentlich gibt es nur einen Druck.
Aber genau hab ich das jetzt nicht verstanden mit dem 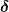 . .
Es geht mir hier auch mehr um das Allgemeine, als um die Gleichung. Ich kann mit dem Ausdruck an sich nichts anfangen.
Und wikipedia hilft mir hier grad nicht wirklich. |
Wenn es wirklich nur die Schreibweise ist, die dich verwirrt... man könnte auch einfach
 schreiben. Das Delta statt dem "d" soll nur zeigen, dass "p" nicht nur eine Funktion von "V" ist, sondern auch noch nach anderen Größen abgeleitet werden könnte. schreiben. Das Delta statt dem "d" soll nur zeigen, dass "p" nicht nur eine Funktion von "V" ist, sondern auch noch nach anderen Größen abgeleitet werden könnte.
_________________
Immer schön die Kirche im Dorf lassen... und dann in die Stadt ziehen. |
|
 |
wishmoep
Anmeldungsdatum: 07.09.2008
Beiträge: 1342
Wohnort: Düren, NRW
|
 wishmoep Verfasst am: 06. Jan 2009 17:05 Titel: wishmoep Verfasst am: 06. Jan 2009 17:05 Titel: |
 |
|
Ist es also üblich partielle Ableitungen auch mit 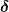 anstatt anstatt  zu kennzeichnen? zu kennzeichnen? |
|
 |
Hagbard

Anmeldungsdatum: 07.02.2006
Beiträge: 320
Wohnort: Augsburg
|
 Hagbard Verfasst am: 06. Jan 2009 17:09 Titel: Hagbard Verfasst am: 06. Jan 2009 17:09 Titel: |
 |
|
| wishmoep hat Folgendes geschrieben: | Ist es also üblich partielle Ableitungen auch mit 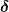 anstatt anstatt  zu kennzeichnen? zu kennzeichnen? |
Für mich ist das eher untypisch, aber ich habs trotzdem schon ein paar Mal gelesen. Vielleicht betont man mit dem Delta ja auch nochmal, dass man die partielle Ableitung in einem bestimmten "Arbeitspunkt" meint. Dazu meldet sich aber hier sicher nochmal jemand...
_________________
Immer schön die Kirche im Dorf lassen... und dann in die Stadt ziehen. |
|
 |
stereo
Anmeldungsdatum: 27.10.2008
Beiträge: 402
|
 stereo Verfasst am: 06. Jan 2009 22:09 Titel: stereo Verfasst am: 06. Jan 2009 22:09 Titel: |
 |
|
Ok, danke dir.
Dann hab ich jetzt die Van der Waals Gleichung für 1 mol nach p umgestellt.
 = \frac {RT}{V-b} - \frac{a}{V^2})
Daraus ergeben sich die Ableitungen:
 = - \frac {RT}{(V-b)^2} + \frac{2a}{V^3})
 = \frac {2RT}{(V-b)^3} - \frac{6a}{V^4})
 = - \frac {6RT}{(V-b)^5} + \frac{24a}{V^5})
Ist das soweit richtig?
Als nächstes müsste ich ja die 1. Ableitung 0 setzen. Und dann in der 3. Ableitung nach der Wendestelle schauen. |
|
 |
stereo
Anmeldungsdatum: 27.10.2008
Beiträge: 402
|
 stereo Verfasst am: 07. Jan 2009 11:45 Titel: stereo Verfasst am: 07. Jan 2009 11:45 Titel: |
 |
|
Ich habe jetzt die kritischen Größen heraus.
Aber wenn wir nochmal kurz über den Ansatz reden würden wäre ich sehr dankbar.
Also ich habe ein Gleichungssystem, und zwar:
_T = 0 = - \frac{RT}{(V-b)^2} + \frac {2a}{V^3})
und
_T = 0 = \frac{2RT}{(V-b)^3} - \frac {6a}{V^4})
Damit komm ich jetzt auch ans Ziel. Aber der Hintergrund ist doch der dass ich den Wendepunkt suche und ich hatte mal in der Schule gelernt, dass ein Punkt ein Wendepunkt ist, wenn die 1. und 3. Ableitung gleich 0 ist. Jedoch bin ich dem Buch und deinem Rat gefolgt, die 1. und die 2. Ableitung gleich 0 zu setzen.
Was mir auch mathematisch logisch erscheint  |
|
 |
Hagbard

Anmeldungsdatum: 07.02.2006
Beiträge: 320
Wohnort: Augsburg
|
 Hagbard Verfasst am: 07. Jan 2009 17:06 Titel: Hagbard Verfasst am: 07. Jan 2009 17:06 Titel: |
 |
|
Deine Gleichungen sind richtig abgeleitet und mit dem von dir verfolgten Weg, die Nullstellen der ersten und zweiten Ableitung zu benutzen liegst du richtig, denn die Änderung der Krümmung (also der zweiten Ableitung) muss einen Nulldurchgang machen, bevor sie ihr Vorzeichen ändern kann. Hast du also entgegen deiner Erinnerung richtig gemacht  . .
_________________
Immer schön die Kirche im Dorf lassen... und dann in die Stadt ziehen. |
|
 |
stereo
Anmeldungsdatum: 27.10.2008
Beiträge: 402
|
 stereo Verfasst am: 12. Jan 2009 21:46 Titel: stereo Verfasst am: 12. Jan 2009 21:46 Titel: |
 |
|
Ich hätte da noch 2 Fragen, und zwar:
Wie komme ich auf die kritischen Größen für die Zustandgleichung von Berthelot bzw Dieterici.
Muss ich hier auch ableiten und die 1., sowie die 2. Ableitung gleich 0 setzen?
Und Frage 2 wäre: was ist die reduzierte Form der Gleichungen?
Bei der Van der Waals Gleichung wäre das:

Was bringt mir diese und wie leite ich sie her? Ich will das für die anderen 2 Gleichungen noch machen 
edit: Ich weiß was die reduzierte Form nun ist und wie ich sie herleite  Was hat sie aber für eine Anwendung? Was hat sie aber für eine Anwendung? |
|
 |
stereo
Anmeldungsdatum: 27.10.2008
Beiträge: 402
|
 stereo Verfasst am: 12. Jan 2009 22:58 Titel: stereo Verfasst am: 12. Jan 2009 22:58 Titel: |
 |
|
Berthelot hab ich nun auch gelöst 
Hatte einen kleinen Rechenfehler gemacht. |
|
 |
Hagbard

Anmeldungsdatum: 07.02.2006
Beiträge: 320
Wohnort: Augsburg
|
 Hagbard Verfasst am: 13. Jan 2009 08:52 Titel: Hagbard Verfasst am: 13. Jan 2009 08:52 Titel: |
 |
|
Wenn es dir nicht zu viel Mühe macht deine Herleitung hier in Latex-Form zu posten, dann mach das doch bitte noch. Dann findet man durch die Suchfunktion mit diesem Thread ein wertvolles Stück Physik (ums geschwollen auszudrücken). Meiner Erfahrung nach merkt man auch immer, ob man alle Einzelheiten verstanden hat, wenn man anderen etwas erklären muss.
Gruß
_________________
Immer schön die Kirche im Dorf lassen... und dann in die Stadt ziehen. |
|
 |
stereo
Anmeldungsdatum: 27.10.2008
Beiträge: 402
|
 stereo Verfasst am: 13. Jan 2009 10:46 Titel: stereo Verfasst am: 13. Jan 2009 10:46 Titel: |
 |
|
Ok, also hier die Zustandsgleichung von Berthelot:
(V-n b)=nRT)
für 1mol gilt:
(V- b)=RT)
Umgestellt nach p:
 = \frac{RT}{V-b} - \frac{a}{TV^2})
Die Bedingungen für die kritischen Größen sind hier:
_T = 0 = - \frac{RT_c}{(V_c-b)^2} + \frac {2a}{T_cV_c^3})
_T = 0 = \frac{2RT_c}{(V_c-b)^3} - \frac {6a}{T_cV_c^4})
Die 1. Gleichung nach T umstellen:
^2 2a}{RV_c^3} ~~\Rightarrow ~~ T_c= \frac{(V_c-b)\sqrt{2a}}{V_c\sqrt{RV_c}})
T in Gleichung 2 eingesetzt:
\sqrt{2a}}{(V_c-b)^3 V_c \sqrt{RV_c}} = \frac {6aV_c\sqrt{RV_c}}{V_c^4(V_c-b)\sqrt{2a}})
Diese Gleichung nach V umstellen, man erhält:

Nun erhält man die kritische Temperatur indem man V_c = 3b in die erste umgestellt Gleichung einsetzt:
\sqrt{2a}}{3b\sqrt{3bR}} = \frac 2 3 \sqrt{\frac{2a}{3bR}})
V_c und T_c in p(V) einsetzen um den kritischen Druck zu erhalten:

Wofür verwendet man die reduzierte Form? |
|
 |
Bine
Gast
|
 Bine Verfasst am: 17. Apr 2009 17:26 Titel: Bine Verfasst am: 17. Apr 2009 17:26 Titel: |
 |
|
Hey,
ich hab aber nochmal eine Frage zur Herleitung der kritischen Größen der Dieterici-Gleichung. Wie kommt man daran? |
|
 |
|
















 Gesundes neues Jahr wünsch ich euch noch
Gesundes neues Jahr wünsch ich euch noch
 .
.