| Autor |
Nachricht |
Hilfebedürftiger
Anmeldungsdatum: 24.03.2010
Beiträge: 103
|
 Hilfebedürftiger Verfasst am: 31. März 2010 17:42 Titel: Arbeit bei isobarer Erwärmung Hilfebedürftiger Verfasst am: 31. März 2010 17:42 Titel: Arbeit bei isobarer Erwärmung |
 |
|
Ein ideales Gas nimmt bei Raumtemperatur (293K) und Atmosphärendruck (1013 hPa) ein Volumen von 15l an.
a) Wieviel Mol des Gases befinden sich in dem Volumen?
b) Bestimmen Sie die Arbeit, die das Gas verrichtet, wenn es isobar auf 65°C erwärmt wird.
zu a)
Mit der Zustandsgleichung idealer Gase erhält man 0,62 Mol.
zu b)
Nach dem 1. Hauptsatz der Thermodynamik und der Tatsache dass es sich um eine isobare Erwärmung handelt müsste die Arbeit doch so zu berechnen sein:
 . .
Mit n=0,62 Mol , R=8,31 J/(mol*K) und der Temperaturdifferenz von 45,15 Kelvin komme ich auf eine Arbeit von 232,62J. Das Ergebnis soll aber 233,4J sein, also liege ich um ein knappes Joule daneben und sehe den Fehler nicht ? |
|
 |
Hilfebedürftiger
Anmeldungsdatum: 24.03.2010
Beiträge: 103
|
 Hilfebedürftiger Verfasst am: 31. März 2010 18:11 Titel: Hilfebedürftiger Verfasst am: 31. März 2010 18:11 Titel: |
 |
|
Ich habe jetzt noch Variante 2 probiert, nämlich über die Volumendifferenz. Aufgrund des konstanten Drucks gilt:
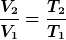
Mit T1=293K, T2=338K und V1=15l (oder 15dm³) erhalte ich V2=17,31l.
Also wäre die Temperaturdifferenz 2,3114dm³.
Nun habe ich  gerechnet und liege knapp über dem gewünschten Ergebnis.... gerechnet und liege knapp über dem gewünschten Ergebnis....  |
|
 |
para
Moderator

Anmeldungsdatum: 02.10.2004
Beiträge: 2874
Wohnort: Dresden
|
 para Verfasst am: 31. März 2010 18:14 Titel: para Verfasst am: 31. März 2010 18:14 Titel: |
 |
|
Das würde ich in dem Rahmen als eher unbedenkliche Rundungsfehler betrachten.
Ein noch leicht anderer Weg: Setzt man dort für p = 101300 Pa, V = 15 L, T = 293 K, ΔT = 45,15 K ein, erhält man eine Arbeit von 234,1 J. Da aber (wegen der 293 K Raumtemperatur) wahrscheinlich von 0°C = 273 K ausgegangen wurde, erhält man mit ΔT = 45 K eine Arbeit von 233,4 J.
Generell sollte man möglichst wenig mit numerischen Zwischenergebnissen arbeiten (bzw. diese im Taschenrechner behalten), um Rundungsfehler zu vermeiden.
Gegen so eine Unklarheit, ob mit 273 K oder 273,15 K gerechnet wurde kann man natürlich nichts machen.
_________________
Formeln mit LaTeX |
|
 |
GvC
Anmeldungsdatum: 07.05.2009
Beiträge: 14861
|
 GvC Verfasst am: 31. März 2010 18:25 Titel: GvC Verfasst am: 31. März 2010 18:25 Titel: |
 |
|
Das sind einfach nur Rundungsfehler und die Vorstellung des Musterlösers, dass zwischen 293K und 65°C eine Temperaturdifferenz von 45K besteht (und nicht, wie es richtig sein müsste, 45,15K). Wenn Du aus dem Taschenrechner den ungerundeten Wert für die Stoffmenge und die Gaskonstante mit 6 Stellen hinter dem Komma benutzt und nur 45K für die Temperaturdifferenz einsetzt, kommst Du genau auf die Musterlösung. Aber was soll das? Ist Dir eine Abweichung von 3,3 Promille vielleicht zu viel? Irgendwie erscheint mir Dein Sinn für Genauigkeit ziemlich übertrieben.
EDIT: para war schneller. |
|
 |
Hilfebedürftiger
Anmeldungsdatum: 24.03.2010
Beiträge: 103
|
 Hilfebedürftiger Verfasst am: 31. März 2010 18:39 Titel: Hilfebedürftiger Verfasst am: 31. März 2010 18:39 Titel: |
 |
|
Ich bin ein harter Pedant, deswegen will ich die Ergebnisse auf 8 Stellen hinter dem Komma genau!!!
Nein, der Grund ist eher folgender: Wir haben zu den Aufgaben keinen Lösungsweg, sondern nur das numerische Ergebnis. Dadurch soll man überprüfen können ob man richtig gerechnet hat. Es ist aber auch schon vorgekommen dass ich einen falschen Ansatz gewählt habe und auf ein Ergebnis kam, was dem tatsächlichen Ergebnis zwar sehr nah kam, aber schlicht durch die Verwendung falscher Zusammenhänge nicht richtig war. Daher dachte ich mir nutze ich diese Forum mal und poste meinen Lösungsweg um festzustellen, ob er denn richtig ist.
Man könnte natürlich auch einfach fragen woher denn dieser vermeintliche Drang nach absoluter Exaktheit kommt, anstatt ihn einfach zu unterstellen ;-) |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 31. März 2010 23:51 Titel: franz Verfasst am: 31. März 2010 23:51 Titel: |
 |
|
OT
| Hilfebedürftiger hat Folgendes geschrieben: | | Ich bin ein harter Pedant, deswegen will ich die Ergebnisse auf 8 Stellen hinter dem Komma genau! |
Dagegen ist prinzipiell nichts zu sagen. Es gibt jedoch für die Rechnung mit Näherungswerten (und um solche dreht es sich ja fast immer, wenn es nicht gerade um [;\pi;] geht) bestimmte "Spielregeln" (sicher bekannt), und bei deren Befolgung verabschiedet man sich sehr schnell von den acht Stellen und ist vielleicht noch zufrieden mit zwei.
mfG |
|
 |
|
















