| Autor |
Nachricht |
Veryyy
Anmeldungsdatum: 14.08.2009
Beiträge: 142
|
 Veryyy Verfasst am: 10. Sep 2009 22:34 Titel: mittlere freie Weglänge zwei Formeln Zusammenhang Veryyy Verfasst am: 10. Sep 2009 22:34 Titel: mittlere freie Weglänge zwei Formeln Zusammenhang |
 |
|
Hallo,
ich bin bei der mittleren freien Weglänge auf zwei verschiedene Formeln gestoßen

und

Nun habe ich eine Aufgabe gegeben und bekomme je nach Formel ein anderes Ergebnis...
Die Aufgabe ist: Wie groß ist die mittlere freie Weglänge eines Heliumatoms in Luft (273K, 1 atm)? Der Radius eines He-Atoms beträgt 128pm
Mit der ersten Formel erhalte ich

Mit der zweiten Formel erhalte ich

Also habe ich versucht herauszufinden, ob die Formel gleich sind:
mit 
und

komme ich wenn ich die beiden Formeln gleichsetze auf

bei der ersten Formel und

Nun ist aber  ungleich ungleich 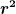 , oder? , oder?
und somit wären die beiden Formeln verschieden...
Habe ich da richtig gerechnet? Und wie finde ich dann heraus, welche von den beiden Formeln ich bei dieser Aufgabe und auch allgemein bei anderen Aufgaben anwenden kann?
Ach ja, ich habe in Wikipedia gefunden, dass man die zweite Formel bei Molekülen anwenden kann.. Die erste Formel kann man für ein einfaches Gas anwenden... allerdings weiß ich nicht genau, was ein einfaches Gas ist.. Oder bedeutet einfach nur, dass es kein Molekül ist, sondern nur ein Atom besitzt? Dann müsste ich ja die erste Formel anwenden, oder?
Wäre nett, wenn mir jemand helfen könnte.
Gruß, Veryyy |
|
 |
Mahlzeit
Gast
|
 Mahlzeit Verfasst am: 10. Sep 2009 23:27 Titel: Mahlzeit Verfasst am: 10. Sep 2009 23:27 Titel: |
 |
|
Die Wirkungsquerschnittsfläche ist nicht
 , ,
sondern
 . .
Wie die 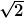 genau zustande kommt, weiß ich leider nich, aber es hat was mit der Bewegung der Teilchen zu tun, wodurch ein Zusammenprall zwischen den Teilchen wahrscheinlicher wird. Würden alle Teilchen stehen und sich nur eins bewegen, würde die genau zustande kommt, weiß ich leider nich, aber es hat was mit der Bewegung der Teilchen zu tun, wodurch ein Zusammenprall zwischen den Teilchen wahrscheinlicher wird. Würden alle Teilchen stehen und sich nur eins bewegen, würde die 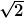 wegfallen. Teilchen, die sich in der Luft schneller bewegen, haben eine höhere Stoßwahrscheinlichkeit. Da die kinetische Energie der Teilchen und damit ihre Geschwindigkeit aber gaußverteilt ist, kommt im Mittel dann halt die wegfallen. Teilchen, die sich in der Luft schneller bewegen, haben eine höhere Stoßwahrscheinlichkeit. Da die kinetische Energie der Teilchen und damit ihre Geschwindigkeit aber gaußverteilt ist, kommt im Mittel dann halt die 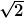 raus. raus.
Oder so ähnlich  |
|
 |
Veryyy
Anmeldungsdatum: 14.08.2009
Beiträge: 142
|
 Veryyy Verfasst am: 11. Sep 2009 00:34 Titel: Veryyy Verfasst am: 11. Sep 2009 00:34 Titel: |
 |
|
Danke für deine Antwort
Du meinst also dass die beiden Formeln gleich sind?
Allerdings kann ich mir nicht ganz vorstellen, dass der Wirkungsquerschnitt

ist.
Der Querschnitt müsste hier nach meiner Vorstellung der Flächeninhalt eines Kreises sein: Also 
Wie kommst du denn auf deine Formel? |
|
 |
Mahlzeit
Gast
|
 Mahlzeit Verfasst am: 11. Sep 2009 13:35 Titel: Mahlzeit Verfasst am: 11. Sep 2009 13:35 Titel: |
 |
|
Wie gesagt, beträgt der Wirkungsquerschnitt nur  , wenn sich die anderen Teilchen in Ruhe befinden. Je schneller die anderen Teilchen, desto höher ist die Wahrscheinlichkeit eines Zusammenstoßes. Daher auch die Abhängigkeit der mittleren freien Weglänge von der Temperatur. Ein Zusammenstoß beinhaltet ja nicht, dass nur dein eines betrachtetes Atom mit einem anderen zusammenstößt, sondern dass andere Atome mit deinem betrachteten zusammenstoßen können. , wenn sich die anderen Teilchen in Ruhe befinden. Je schneller die anderen Teilchen, desto höher ist die Wahrscheinlichkeit eines Zusammenstoßes. Daher auch die Abhängigkeit der mittleren freien Weglänge von der Temperatur. Ein Zusammenstoß beinhaltet ja nicht, dass nur dein eines betrachtetes Atom mit einem anderen zusammenstößt, sondern dass andere Atome mit deinem betrachteten zusammenstoßen können.
Erklären kann ich leider nicht, wie man auf den Faktor  kommt, aber wenn die anderen Teilchen im Mittel die selbe kinetische Energie besitzen, ist das so. kommt, aber wenn die anderen Teilchen im Mittel die selbe kinetische Energie besitzen, ist das so.
[/code] |
|
 |
Mahlzeit
Gast
|
 Mahlzeit Verfasst am: 11. Sep 2009 13:37 Titel: Mahlzeit Verfasst am: 11. Sep 2009 13:37 Titel: |
 |
|
Hups, jetzt hab ich was falsch gemacht und kann nicht mehr editieren. Hier nochmal richtig:
Wie gesagt, beträgt der Wirkungsquerschnitt nur  , wenn sich die anderen Teilchen in Ruhe befinden. Je schneller die anderen Teilchen, desto höher ist die Wahrscheinlichkeit eines Zusammenstoßes. Daher auch die Abhängigkeit der mittleren freien Weglänge von der Temperatur. Ein Zusammenstoß beinhaltet ja nicht, dass nur dein eines betrachtetes Atom mit einem anderen zusammenstößt, sondern dass andere Atome mit deinem betrachteten zusammenstoßen können. , wenn sich die anderen Teilchen in Ruhe befinden. Je schneller die anderen Teilchen, desto höher ist die Wahrscheinlichkeit eines Zusammenstoßes. Daher auch die Abhängigkeit der mittleren freien Weglänge von der Temperatur. Ein Zusammenstoß beinhaltet ja nicht, dass nur dein eines betrachtetes Atom mit einem anderen zusammenstößt, sondern dass andere Atome mit deinem betrachteten zusammenstoßen können.
Erklären kann ich leider nicht, wie man auf den Faktor  kommt, aber wenn die anderen Teilchen im Mittel die selbe kinetische Energie besitzen, ist das so. kommt, aber wenn die anderen Teilchen im Mittel die selbe kinetische Energie besitzen, ist das so. |
|
 |
Veryyy
Anmeldungsdatum: 14.08.2009
Beiträge: 142
|
 Veryyy Verfasst am: 11. Sep 2009 16:37 Titel: Veryyy Verfasst am: 11. Sep 2009 16:37 Titel: |
 |
|
ok, das hab ich so ungefähr verstanden. Danke.
Das heißt, wenn sich nur mein eines Teilchen bewegt, benutze ich die 1. Formel. Wenn sich aber alle Teilchen bewegen (wie das doch normalerweise immer der Fall ist, oder? ) benutze ich die 2. Formel.
Also müsste ich auch bei meiner Aufgabe die 2. Formel anwenden.
ich frage mich jetzt, wozu man dann überhaupt die 1. Formel braucht? Man kann den absoluten Nullpunkt doch nicht erreichen. Also bewegen sich immer alle Teilchen...
Oder hängt es noch mit was anderem zusammen, welche Formel ich anwenden muss? |
|
 |
Mahlzeit
Gast
|
 Mahlzeit Verfasst am: 11. Sep 2009 18:04 Titel: Mahlzeit Verfasst am: 11. Sep 2009 18:04 Titel: |
 |
|
Fehler aus meinem vorherigen Post: Die Wirkungsquerschnittsfläche beträgt niemals  , sondern , sondern  . Die Wirkungsquerschnittsfläche ergibt sich nämlich nicht nur aus dem Radius des betrachteten Atoms, sondern auch aus dem Radius des Stoßpartners. Bei gleich großen Atomen also . Die Wirkungsquerschnittsfläche ergibt sich nämlich nicht nur aus dem Radius des betrachteten Atoms, sondern auch aus dem Radius des Stoßpartners. Bei gleich großen Atomen also ^2 = \pi \cdot d^2) . .
Deine ersten beiden Formeln im ersten Post sind identisch, weil  (wenn sich alle Atome im Raum bewegen, was immer der Fall ist, wie du schon richtig erkannt hast). (wenn sich alle Atome im Raum bewegen, was immer der Fall ist, wie du schon richtig erkannt hast). |
|
 |
Mahlzeit
Gast
|
 Mahlzeit Verfasst am: 11. Sep 2009 18:08 Titel: Mahlzeit Verfasst am: 11. Sep 2009 18:08 Titel: |
 |
|
Nachtrag: Die zweite Formel kannst du immer für gleiche Stoßpartner verwenden, bei unterschiedlich großen Atomen/Molekülen ändert sich das 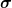 . . |
|
 |
Veryyy
Anmeldungsdatum: 14.08.2009
Beiträge: 142
|
 Veryyy Verfasst am: 12. Sep 2009 13:24 Titel: Veryyy Verfasst am: 12. Sep 2009 13:24 Titel: |
 |
|
| Zitat: | | Die Wirkungsquerschnittsfläche ergibt sich nämlich nicht nur aus dem Radius des betrachteten Atoms, sondern auch aus dem Radius des Stoßpartners. |
Ja, stimmt... das kann man sich ja so vorstellen, dass das betrachtete Teilchen den doppelten Radius hat und die anderen Teilchen die im Raum verstreut sind, punktförmig sind. Dann bleibt ja trotzdem die Wahrscheinlichkeit gleich groß, dass sie sich stoßen.
| Zitat: | | Deine ersten beiden Formeln im ersten Post sind identisch |
Das ist ja eigentlich praktisch, dann muss ich sie nämlich nicht auseinanderhalten.
jetzt sehe ich auch, warum ich zwei unterschiedliche Ergebnisse habe.. ich habe nämlich bei der 1. Formel  gewählt.. und nicht gewählt.. und nicht 
Das heißt ich muss immer ²) wählen, oder? Dann sind nämlich auch beide Formeln identisch. wählen, oder? Dann sind nämlich auch beide Formeln identisch.
Vielen Dank für deine Hilfe  |
|
 |
|
|

















