| Autor |
Nachricht |
kaliber44
Anmeldungsdatum: 09.06.2008
Beiträge: 7
|
 kaliber44 Verfasst am: 08. Sep 2008 11:18 Titel: Wasserstoffatom und die Energiestufen kaliber44 Verfasst am: 08. Sep 2008 11:18 Titel: Wasserstoffatom und die Energiestufen |
 |
|
Bei der folgenden Aufgabe habe ich nicht wirklich ne Ahnung wie ich sie lösen soll:
,,Berechnen sie die Frequenz des emittierten Photons, wenn in einem Wasserstoffatom ein Elektron von der 12 auf die 10 Energiestufe übergeht?"
Kann mir einer helfen? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 08. Sep 2008 11:28 Titel: dermarkus Verfasst am: 08. Sep 2008 11:28 Titel: |
 |
|
Magst du mal erzählen, was du dazu schon weißt, und was du dir dazu selbst schon überlegt und aus deinen Aufschrieben zusammengesucht hast?
Kennst du eine Formel, die dir hier weiterhelfen könnte, oder findest du eine in deinen Aufschrieben oder in deinem Physikbuch? Welche Variable in dieser Formel ist die Nummer der Energiestufen? |
|
 |
kaliber44
Anmeldungsdatum: 09.06.2008
Beiträge: 7
|
 kaliber44 Verfasst am: 08. Sep 2008 11:42 Titel: kaliber44 Verfasst am: 08. Sep 2008 11:42 Titel: |
 |
|
Hey, ich weíß eigentlich so gut wie nix darüber. Haben das Themea erst letzte Stunde kurz angeschniten. Haben nur eine Formel dazu aufgeschrieben, und zwar potentielle+kinetische Energie:
W(h)=-1/8*(m(e)*e^n)/(E^2*h^2*n2)
Ja, das wäre die einzige Formel die wir aufgeschrieben haben, bin mir aber nicht sicher , ob sie etwas damit zu tun hat. Da ich in der Schule(drei Freistunden) bin hab ich auch leider mein Physikbuch nicht da. Im Internet konnte ich nicht wirklich etwas finden,was mir helfen könnte. Die Nummer der Energiestufen sind wahrscheinlich 12 und 10.
Wäre cool, wenn du ne Formel dazu kennen würdest oder etwas hast was mir weiterhelfen könnte. Jedoch musst du eins bedenken, bin kein Physikkenner ,hab eher Probleme damit  |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 08. Sep 2008 11:55 Titel: dermarkus Verfasst am: 08. Sep 2008 11:55 Titel: |
 |
|
Ja, genau, diese Formel meine ich 
Damit du sie sinnvoll verwenden kannst, solltest du allerdings zunächst mal die Tippfehler daraus beseitigen und dann überlegen, was du schon darüber weißt, was die Buchstaben darin bedeuten.
* Meinst du statt ) vielleicht vielleicht ) ? Das ? Das 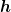 ist einfach nur das Plancksche Wirkungsquantum, also eine Konstante. ist einfach nur das Plancksche Wirkungsquantum, also eine Konstante.
* Bist du dir bei dem  im Zähler sicher? im Zähler sicher?
* Meinst du unten im Nenner wirklich 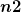 (was soll das sein?) oder vielleicht statt dessen irgend einen Ausdruck mit (was soll das sein?) oder vielleicht statt dessen irgend einen Ausdruck mit 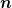 , in dem du nur ein Rechenzeichen vergessen hast ? , in dem du nur ein Rechenzeichen vergessen hast ?
* Was meinst du mit dem 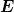 im Nenner? Kann es sein, dass du da einen ganz anderen Buchstaben als ein E meinst, der etwas ganz anderes als eine Energie meint? im Nenner? Kann es sein, dass du da einen ganz anderen Buchstaben als ein E meinst, der etwas ganz anderes als eine Energie meint?
Magst du deine Formel vielleicht am besten mal mit korrigierten Tippfehlern mit Latex hier eingeben? Da wird die Formel gleich viel schöner, und eventuelle Tippfehler bleiben nicht so leicht unbemerkt.
Und dann dazusagen, ob du zum Beispiel schon weißt, was das 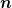 in dieser Formel sein soll? in dieser Formel sein soll?
// edit: Weißt du schon, was mit "Energiestufen eines Atoms" gemeint ist, oder magst du das zum Beispiel mal mit Hilfe von
http://leifi.physik.uni-muenchen.de/web_ph09_g8/grundwissen/07energiestufen/energiestufen.htm
wiederholen?
Und hilft dir folgender Link,
http://www.pctheory.uni-ulm.de/didactics/quantenchemie/html/bohrAtom.html
um deine Formel (siehe (10.9)) samt Herleitung und den Variablen, die darin vorkommen, besser zu verstehen? |
|
 |
kaliber44
Anmeldungsdatum: 09.06.2008
Beiträge: 7
|
 kaliber44 Verfasst am: 08. Sep 2008 18:01 Titel: kaliber44 Verfasst am: 08. Sep 2008 18:01 Titel: |
 |
|
Hi, sorry ich kenn mich mit Latex nicht aus,hab grad nachgeguckt ist anscheinend ne Software, kenn mich aber damit nicht aus. Geht das schnell zu erlernen, wenn ja sag bitte bescheid wäre ja auch vorteilhaft für die Zukunft. Ja, in der Eile hab ich wirklich paar Fehler in die Formel eingebaut, hier noch mal die Formel, aber richtig:
W(n)=-1/8*((m(e)*e^4)/(E(0)^2*h^2*n^2)
Das E sollte epsilon E(o) sein.
Ok, ich glaub ich habs jetzt kapiert. Also W(1)=-2,175*10^-18, dann sollte ich so wahrscheinlich vorgehen:
W(12)=-2,175*10^-18*1/12^2=-1.52*10^-20
W(10)=-2,175*10^-18*1/10^2=-2.19*10^-20
Die Ergebnisse subtrahieren, dann kommt man auf deltaW=6,68*10^-21, das Ergebnis dann durch die Konstante h teilen,sodass ich auf f komme,von 1*10^13(basirend auf der Formel W=h*f)(alle Ergebnisse gerundet).
Ist das richtig oder falsch? |
|
 |
wishmoep
Anmeldungsdatum: 07.09.2008
Beiträge: 1342
Wohnort: Düren, NRW
|
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 08. Sep 2008 18:13 Titel: dermarkus Verfasst am: 08. Sep 2008 18:13 Titel: |
 |
|
Diese Rechnung meinst du richtig, mit den Zahlenwerten darin bin ich bis auf kleine Rundungsfehler einverstanden. 
Aber achte unbedingt noch darauf, dass du jeweils immer die Einheiten mit dazuschreibst, denn die Zahlen alleine ergeben natürlich keinen Sinn, und Ergebnisse ohne Einheit sind nutzlos. |
|
 |
kaliber44
Anmeldungsdatum: 09.06.2008
Beiträge: 7
|
 kaliber44 Verfasst am: 08. Sep 2008 20:50 Titel: kaliber44 Verfasst am: 08. Sep 2008 20:50 Titel: |
 |
|
|
Danke,für die Hilfe! |
|
 |
Hystrix
Anmeldungsdatum: 20.09.2008
Beiträge: 1
|
 Hystrix Verfasst am: 21. Sep 2008 11:54 Titel: Hystrix Verfasst am: 21. Sep 2008 11:54 Titel: |
 |
|
Könnte man das nich auch noch anderes rechnen?
Wir haben die Balmer Formel verallgemeinteret zu
 \quad m \geq n;~n \in \mathbb{N} )
})
dann einfach für  und und  einsetzten, dann müsste man doch auch auf das ergebniss kommen. einsetzten, dann müsste man doch auch auf das ergebniss kommen. |
|
 |
mitschelll
Anmeldungsdatum: 06.12.2007
Beiträge: 362
|
 mitschelll Verfasst am: 21. Sep 2008 15:38 Titel: mitschelll Verfasst am: 21. Sep 2008 15:38 Titel: |
 |
|
Klar, das geht auch.
Die Formel hat auch einen Namen: Man nennt sie Rydberg-Formel. Die kann man zur Berechnung der Energie, der Frequenz, der Wellenlänge usw. aufstellen. Man bekommt dann jeweils eine andere Konstante vor der Klammer.
_________________
Es irrt der Mensch, solang' er strebt.
Johann Wolfgang von Goethe |
|
 |
|

















