| Autor |
Nachricht |
Galileo995703
Anmeldungsdatum: 28.08.2007
Beiträge: 55
|
 Galileo995703 Verfasst am: 29. Dez 2007 19:38 Titel: Durchmesser des CO2-Moleküls abschätzen Galileo995703 Verfasst am: 29. Dez 2007 19:38 Titel: Durchmesser des CO2-Moleküls abschätzen |
 |
|
meine aufgabe besteht darin den durchmesser eines co2 moleküls abzuschätzen, wobei ich das co2-molekül als kugel annehm...
aber irgendwie find ich da überhaupt keinen denkansatz |
|
 |
Galileo995703
Anmeldungsdatum: 28.08.2007
Beiträge: 55
|
 Galileo995703 Verfasst am: 29. Dez 2007 19:39 Titel: Galileo995703 Verfasst am: 29. Dez 2007 19:39 Titel: |
 |
|
|
oder nehm ich hierbei das kritische volumen.....gilt dies nur für ein molekül? |
|
 |
Galileo995703
Anmeldungsdatum: 28.08.2007
Beiträge: 55
|
 Galileo995703 Verfasst am: 29. Dez 2007 19:50 Titel: Galileo995703 Verfasst am: 29. Dez 2007 19:50 Titel: |
 |
|
wäre dies so käme ich auf:


Werte eingesetzt:

hierbei bin ich mir aber mit der einheit nicht sicher...daher hab ich sie nicht angehängt |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 29. Dez 2007 19:53 Titel: dermarkus Verfasst am: 29. Dez 2007 19:53 Titel: |
 |
|
2 Tipps:
1) Endergebnisse ohne Einheit dran haben keine Aussagekraft. Und wenn du mit Einheiten rechnest, siehst du viel schneller, ob etwas richtig sein kann oder falsch sein muss.  Soll das Ergebnis deiner Rechnung wirklich aussagen, dass der Durchmesser eines CO2-Moleküls gleich 6 cm sein soll Soll das Ergebnis deiner Rechnung wirklich aussagen, dass der Durchmesser eines CO2-Moleküls gleich 6 cm sein soll  Kann das stimmen? Kann das stimmen?
2) Weißt du schon, was das sogenannte Kovolumen ist, wo es in der Van-der-Waals-Gleichung steht, und kannst du am besten in Worten formulieren, was es bedeutet? |
|
 |
Galileo995703
Anmeldungsdatum: 28.08.2007
Beiträge: 55
|
 Galileo995703 Verfasst am: 29. Dez 2007 20:17 Titel: Galileo995703 Verfasst am: 29. Dez 2007 20:17 Titel: |
 |
|
|
was das kovolumen is weiß ich nicht....vielleicht soll ich daher den durchmesser auch nur abschätzen....aber wie kann ich das machen? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 29. Dez 2007 20:29 Titel: dermarkus Verfasst am: 29. Dez 2007 20:29 Titel: |
 |
|
Du darfst auch gerne nachschlagen oder in Wikipedia, ... spicken 
Noch ein Tipp zum Kovolumen:
Was ist das 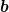 in der Van-der-Waals-Gleichung, und was bedeutet es genauer? in der Van-der-Waals-Gleichung, und was bedeutet es genauer?
Was siehst du der Van-der-Waals-Gleichung für den Fall 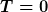 an? an?
(Der Hauptteil dieser Aufgabe besteht darin, zu verstehen, was das Kovolumen ist  ) ) |
|
 |
Galileo995703
Anmeldungsdatum: 28.08.2007
Beiträge: 55
|
 Galileo995703 Verfasst am: 29. Dez 2007 21:08 Titel: Galileo995703 Verfasst am: 29. Dez 2007 21:08 Titel: |
 |
|
ahh....ok.....das b in der van-der waals gleichung ist das kovolumen...und dies wiederum entspricht in etwa dem eigenvolumen der atome von einem mol des gases....d.h. für mich das ich bei meiner rechnung das kovolumen, also das b nehmen muss, und in meine obige rechnung für v einsetzen muss, damit ich auf den durchmesser des co2-moleküls komme.....oder?
für dem fall 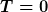 müsste ja die van-der-waals-gleichung auch 0 werden, da ja rechts wie links in der gleichung das gleiche stehen muss.... müsste ja die van-der-waals-gleichung auch 0 werden, da ja rechts wie links in der gleichung das gleiche stehen muss.... |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 29. Dez 2007 21:15 Titel: dermarkus Verfasst am: 29. Dez 2007 21:15 Titel: |
 |
|
| Galileo995703 hat Folgendes geschrieben: | ahh....ok.....das b in der van-der waals gleichung ist das kovolumen...und dies wiederum entspricht in etwa dem eigenvolumen der atome von einem mol des gases....
|
Genau 
| Zitat: |
d.h. für mich das ich bei meiner rechnung das kovolumen, also das b nehmen muss, und in meine obige rechnung für v einsetzen muss, damit ich auf den durchmesser des co2-moleküls komme.....oder?
|
Fast. Eins hast du dabei noch vergessen:
Wieviele Moleküle sind 1 mol? Wie berücksichtigst du das in deiner Rechnung?
| Zitat: |
für dem fall 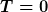 müsste ja die van-der-waals-gleichung auch 0 werden, da ja rechts wie links in der gleichung das gleiche stehen muss.... müsste ja die van-der-waals-gleichung auch 0 werden, da ja rechts wie links in der gleichung das gleiche stehen muss.... |
Einverstanden. Wenn du bei konstantem Druck die Temperatur auf Null senkst, dann wird auf der linken Seite der Gleichung das Volumen V so lange kleiner, bis =0) ist, also bis das Volumen, das 1 mol der Moleküle einnehmen, nur noch ihr eigenes ist. Denn bei T=0 ist zwischen den Molekülen kein Platz mehr frei, und der Platz, den die Moleküle einnehmen, ist nur noch (in etwa) durch ihr eigenes Volumen gegeben. ist, also bis das Volumen, das 1 mol der Moleküle einnehmen, nur noch ihr eigenes ist. Denn bei T=0 ist zwischen den Molekülen kein Platz mehr frei, und der Platz, den die Moleküle einnehmen, ist nur noch (in etwa) durch ihr eigenes Volumen gegeben.  |
|
 |
Galileo995703
Anmeldungsdatum: 28.08.2007
Beiträge: 55
|
 Galileo995703 Verfasst am: 29. Dez 2007 21:34 Titel: Galileo995703 Verfasst am: 29. Dez 2007 21:34 Titel: |
 |
|
ok...stimmt...das mit dem einen mol hatte ich nich bedacht...
)
Meine Rechnung:

Dies in meine Durchmesser-Formel eingesetzt:

Kann dieses Ergebnis richtig sein? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 29. Dez 2007 21:47 Titel: dermarkus Verfasst am: 29. Dez 2007 21:47 Titel: |
 |
|
Prima, mit deinem Ansatz bin ich jetzt komplett einverstanden 
Magst du mal, um selbst zu beurteilen, ob dein Ergebnis nun in der richtigen Größenordnung liegt, sagen, was du selbst ganz grob als Ergebnis erwartet hattest? Kennst du zum Beispiel eine Vergleichs-Zahl als Größenordnung auswendig? Wie groß ist so ein Atom ungefähr, zum Beispiel das kleinste Atom, also das Wasserstoffatom? Kannst du also das Ergebnis, das dir dein Taschenrechner ausgespuckt hat, grob bestätigen? |
|
 |
Galileo995703
Anmeldungsdatum: 28.08.2007
Beiträge: 55
|
 Galileo995703 Verfasst am: 29. Dez 2007 21:55 Titel: Galileo995703 Verfasst am: 29. Dez 2007 21:55 Titel: |
 |
|
mein ergebnis liegt in der richtigen größenordnung, denn die hülle eines wasserstoffatoms hat ungefähr den durchmesser  ... ...
somit denke ich das ich in der richtigen größenordnung liege
hast du auch eine ahnung wie ich bei der aufgabe mit der wegsumme vorgehen muss...die ich im vorhergehenden thread geschrieben habe?
danke nochmal für die echt klasse hilfe!
                |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 29. Dez 2007 22:10 Titel: dermarkus Verfasst am: 29. Dez 2007 22:10 Titel: |
 |
|
| Galileo995703 hat Folgendes geschrieben: | mein ergebnis liegt in der richtigen größenordnung, denn die hülle eines wasserstoffatoms hat ungefähr den durchmesser  ... ...
somit denke ich das ich in der richtigen größenordnung liege
|
Einverstanden 
Dann bleibt nun nur noch, das Ergebnis sinnvoll zu runden, dann bist du fertig  |
|
 |
|
















 Soll das Ergebnis deiner Rechnung wirklich aussagen, dass der Durchmesser eines CO2-Moleküls gleich 6 cm sein soll
Soll das Ergebnis deiner Rechnung wirklich aussagen, dass der Durchmesser eines CO2-Moleküls gleich 6 cm sein soll  Kann das stimmen?
Kann das stimmen?
 )
)