| Autor |
Nachricht |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 08. Apr 2023 19:39 Titel: Druck/Dampf am Anfang des Siedepunktes berechnen frage1 Verfasst am: 08. Apr 2023 19:39 Titel: Druck/Dampf am Anfang des Siedepunktes berechnen |
 |
|
Hallo Leute,
kann mir jemand erklären, wie man auf die Zusammensetzung des Dampfes am Anfang des Siedepunktes gekommen ist? Ich kann die Rechnung nicht nachvollziehen. Wie kommt man auf die Umformung pA/pB = pges *yA / pges * yB =
?? Mich haben die Rechenschritte ein wenig verwirrt. Ich habe hier Verständnisprobleme. Warum ist pA= pges * yA? Woher kommt diese Umformung?
Könnt ihr mir bitte eine Rückmeldung geben und erklären wie man hier vorgegangen ist?
| Beschreibung: |
|
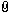
Download |
| Dateiname: |
701F8798-51FD-4A47-B1E9-8B70E19DC3CE.jpeg |
| Dateigröße: |
57.01 KB |
| Heruntergeladen: |
202 mal |
| Beschreibung: |
|
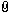
Download |
| Dateiname: |
4FC94EC2-4C9D-4E96-86D8-B378227413F3.jpeg |
| Dateigröße: |
51.18 KB |
| Heruntergeladen: |
158 mal |
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 08. Apr 2023 19:56 Titel: Re: Druck/Dampf am Anfang des Siedepunktes berechnen Myon Verfasst am: 08. Apr 2023 19:56 Titel: Re: Druck/Dampf am Anfang des Siedepunktes berechnen |
 |
|
| frage1 hat Folgendes geschrieben: | | Wie kommt man auf die Umformung pA/pB = pges *yA / pges * yB =
?? Mich haben die Rechenschritte ein wenig verwirrt. Ich habe hier Verständnisprobleme. Warum ist pA= pges * yA? Woher kommt diese Umformung? |
Das ist doch immer so bei einem Gasgemisch, wenn sich die einzelnen Komponenten wie ideale Gase verhalten: Für den Partialdruck von Gas i gilt

Hier werden die Stoffmengenanteile im Dampf nicht mit xA, xB, sondern mit yA und yB bezeichnet. xA und xB sind die Stoffmengenanteile in der Flüssigkeit.
Nach dem Raoultschen Gesetz betragen die Partialdrücke von A und B 50mbar bzw. 60mbar. Aus der obigen Gleichung folgt yA/yB=pA/pB. Anderseits gilt yA+yB=1. Damit hat man zwei Gleichungen für yA, yB. Das wird dann in der Lösung vielleicht etwas umständlich aufgelöst.
|
|
 |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 09. Apr 2023 05:07 Titel: frage1 Verfasst am: 09. Apr 2023 05:07 Titel: |
 |
|
Vielen Dank für deine Rückmeldung Myon!
Aber wie kommt man dann auf diese Formel pA/pB = pges *yA / pges * yB ? Also warum pges*yA ? Wie hat man hier umgeformt?
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 09. Apr 2023 08:32 Titel: Myon Verfasst am: 09. Apr 2023 08:32 Titel: |
 |
|
Im Flüssigkeitsgemisch sind zwei Substanzen mit Stoffmengenanteilen (Molenbrüchen) xA und xB. Das Raoultsche Gesetz besagt nun, dass sich im Gleichgewicht über der Flüssigkeit Partialdrücke der beiden Gase von

einstellen. pA*, pB* sind die Dampdrücke, die sich über den Flüssigkeiten einstellen würden, wenn es sich um reine Stoffe handeln würde.
Im Aufgabenteil a) wird nach der Stoffzusammensetzung des Dampfes beim Beginn des Siedepunktes gefragt. Diese ergibt sich daraus, dass die Stoffmengenanteile in einem Gas proportional zu den Partialdrücken im Gas sind, wenn es sich um ideale Gase handelt. Denn es gilt

und damit

Der Druck beim Beginn des Siedens entspricht, Irrtum vorbehalten, nicht dem berechneten Gesamtdruck im Gleichgewicht, sondern dem höheren Partialdruck über dem Gemisch. Auf diesen Druck muss der Gesamtdruck durch Abpumpen verringert werden.
|
|
 |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 09. Apr 2023 10:23 Titel: frage1 Verfasst am: 09. Apr 2023 10:23 Titel: |
 |
|
Danke dir vielmals für deine Erklärung!
Aber es sind so einige Dinge noch nicht ganz einleuchtend. Aber bevor ich weitere Fragen bzgl. der Aufgabe a) stelle, wollte ich zusätzlich noch die Aufgabe b) durchgehen, wenn es für dich auch in Ordnung ist.
Da wird ja die folgende Frage gestellt: Wie ist der Druck beim letzten verbleibenden Tropfen? Und in der Lösung steht: Beim letzten Tropfen hat die Gasphase die gleiche Zusammensetzung wie die flüssige Phase zu Beginn.
Ich verstehe diese Erklärung nicht. Ich habe hier noch Verständnisprobleme. Wieso hat die Gasphase die gleiche Zusammensetzung wie die flüssige Phase? Wie kann ich mir das erklären?
Edit: Also sie haben die Aufgabe b) folgendermaßen gerechnet. Wie sind sie hier auf xA,L gekommen? Also wie haben sie da die Gleichung nach xA,L aufgelöst? Ich weiß auch nicht, ob meine Frage berechtigt ist, da mir die Auflösung nach x keine Schwierigkeiten bereiten soll, aber irgendwie kann ich die Rechenschritte nicht wirklich nachvollziehen
| Beschreibung: |
|
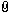
Download |
| Dateiname: |
2EDA1DB6-F973-403F-B14D-09E1D0511D6D.jpeg |
| Dateigröße: |
381.9 KB |
| Heruntergeladen: |
141 mal |
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 09. Apr 2023 19:28 Titel: Myon Verfasst am: 09. Apr 2023 19:28 Titel: |
 |
|
Zu a) Die Flüssigkeit beginnt zu verdampfen, wenn der berechnete Druck von 110mbar erreicht ist. Die Lösung ist schon richtig.
Zu b)
| frage1 hat Folgendes geschrieben: | Und in der Lösung steht: Beim letzten Tropfen hat die Gasphase die gleiche Zusammensetzung wie die flüssige Phase zu Beginn.
Ich verstehe diese Erklärung nicht. Ich habe hier noch Verständnisprobleme. Wieso hat die Gasphase die gleiche Zusammensetzung wie die flüssige Phase? |
Anders als in der "anderen" Aufgabe wird hier kein Dampf abgepumpt. Die stoffliche Zusammensetzung von Dampf und Flüssigkeit insgesamt bleibt also konstant. Da am Ende praktisch alles gasförmig ist, muss die Zusammensetzung des Dampfes gleich der ursprünglichen Zusammensetzung der Flüssigkeit sein.
Wenn xA, xB und xA', xB' die Stoffmengenanteile der Flüssigkeit am Anfang und beim letzten Tropfen sind und yA', yB' die Stoffmengenanteile des Dampfes, wenn nur noch ein Tropfen Flüssigkeit vorhanden ist, so gilt yA'=xA, yB'=xB.
Die Stoffmengenanteile im Dampf sind wieder proportional zu den Partialdrücken, also

Nun Auflösen nach xA', xB', z.B. durch Multiplikation mit den Nennern:
y_\mathrm{A}'p_\mathrm{B}^\star=x_\mathrm{A}'y_\mathrm{B}'p_\mathrm{A}^\star)

Zuletzt noch den gesuchten Gesamtdruck berechnen:

|
|
 |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 09. Apr 2023 22:40 Titel: frage1 Verfasst am: 09. Apr 2023 22:40 Titel: |
 |
|
Vielen Dank für die ganzen Erklärungen Myon!
Ich hab' nun einen groben Überblick, was die Aufgabe angeht.
Ich kehre wieder zur Aufgabe a) zurück. Ich hab' die Stoffzusammensetzung des Dampfes zu Beginn des Siedepunktes immer noch nicht gecheckt. Warum ist pA = pA/pges bzw. pB = pB/pges ? Was ist in diesem Fall pges? Ich versteh` die Formeln noch nicht. Was ist eigentlich pges in diesem Fall? Ich habe hier noch eine große Lücke...
|
|
 |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 10. Apr 2023 18:36 Titel: frage1 Verfasst am: 10. Apr 2023 18:36 Titel: |
 |
|
|
Edit: Also die Rechnungen habe ich alle verstanden. Ich kann mir darunter nur bildlich nichts vorstellen, also wie der ganze Prozess theoretisch/praktisch abläuft. Also ich check' noch nicht warum wir das so rechnen..
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 11. Apr 2023 20:51 Titel: Myon Verfasst am: 11. Apr 2023 20:51 Titel: |
 |
|
Schau Dir vielleicht einmal diese Seite an, insbesondere das Dampfdruckdiagramm und die Erklärung dazu.
http://www.pci.tu-bs.de/aggericke/PC1/Kap_V/Phasengleichgewichte.htm
Sind die Stoffmengenanteile der Flüssigkeit bekannt, folgen die Stoffemengenanteile des Dampfes über das Raoultsche Gesetz, und umgekehrt ebenfalls - sofern die beiden Phasen im Gleichgewicht sind.
Bei a) liegt zu Beginn alles flüssig vor, die beiden Stoffe im Verhältnis 1:2. Über das Raoultsche Gesetz folgen die Partialdrücke über der Flüssigkeit, wenn sich der erste Dampf bildet. Das Verhältnis der Partialdrücke entspricht dem Stoffmengenverhältnis des Dampfes.
Bei b) läuft es umgekehrt. Es ist praktisch nur noch Dampf vorhanden im Stoffemengenverhältnis 1:2. Aus dem Raoultschen Gesetz folgt wiederum die Zusammensetzung der Flüssigkeit, denn für beide Phasen muss gelten

mit pA'/pB'=yA'/yB'=1:2.
Praktisch könnte dies so aussehen: Die Flüssigkeit befindet sich in einem geschlossenen Behälter, dessen Volumen mit einem Kolben verändert werden kann. Zu Beginn drückt der Kolben mit einem Druck, der über dem Dampfdruck (entsprechend der Temperatur und Flüssigkeitszusammensetzung) liegt, auf die Flüssigkeit. Wird der Druck reduziert, beginnt sich Dampf über der Flüssigkeit zu bilden, sobald der Dampfdruck unterschritten wird. Der Anteil des flüchtigeren Stoffes, d.h. des Stoffes mit dem höheren Dampfdruck pA*, ist im Dampf gegenüber der Flüssigkeit erhöht. Wird das Volumen weiter vergrössert, ändert sich kontinuierlich die Zusammensetzung der Flüssigkeit und des Dampfes - bis zuletzt alles dampfförmig vorliegt mit der Zusammensetzung der ursprünglichen Flüssigkeit.
Während der Expansion muss Wärme zugeführt werden, um die Temperatur konstant zu halten. Die Verdampfung benötigt Energie, und bei der Volumenvergrösserung leistet das Gas Arbeit.
|
|
 |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 16. Apr 2023 17:30 Titel: frage1 Verfasst am: 16. Apr 2023 17:30 Titel: |
 |
|
1000 Dank für die ausführliche Erklärung Myon!!
Falls im Nachhinein weitere Fragen auftauchen, melde ich mich.
|
|
 |
|















