| Autor |
Nachricht |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 25. Feb 2022 07:04 Titel: Verdunstung von Alkohol in einer Flasche TomS Verfasst am: 25. Feb 2022 07:04 Titel: Verdunstung von Alkohol in einer Flasche |
 |
|
Ich bin auf der Suche nach dem Ansatz für folgende Fragestellung: In einer verschlossenen Flasche mit Volumen V befindet sich ein alkoholisches Getränk (Cognac, Whisky
) der Menge  mit einem Alkoholgehalt a (Volumenprozent) also einer Alkoholmenge mit einem Alkoholgehalt a (Volumenprozent) also einer Alkoholmenge  . Im restlichen Volumen . Im restlichen Volumen  befindet sich Luft mit bekannter Luftfeuchtigkeit w sowie zu Beginn einem Alkoholgehalt Null. Gesucht ist ein Differentialgleichungssystem für die Verdunstungsrate von Wasser und Alkohol, d.h. insbs. die verbleibenden Mengen befindet sich Luft mit bekannter Luftfeuchtigkeit w sowie zu Beginn einem Alkoholgehalt Null. Gesucht ist ein Differentialgleichungssystem für die Verdunstungsrate von Wasser und Alkohol, d.h. insbs. die verbleibenden Mengen ) und und ) . An sich wären bereits die asymptotischen Werte . An sich wären bereits die asymptotischen Werte ) und und ) ausreichend. ausreichend.
Wie lautet denn der Ansatz für dieses Differentialgleichungssystem und wo finde ich notwendigen Parameter?
Die Temperatur soll über den gesamten Zeitraum als konstant angesehen werden. Weitere Stoffe neben Wasser und Alkohol werden vernachlässigt.
|
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5740
|
 DrStupid Verfasst am: 25. Feb 2022 10:36 Titel: Re: Verdunstung von Alkohol in einer Flasche DrStupid Verfasst am: 25. Feb 2022 10:36 Titel: Re: Verdunstung von Alkohol in einer Flasche |
 |
|
| TomS hat Folgendes geschrieben: | In einer verschlossenen Flasche mit Volumen V befindet sich ein alkoholisches Getränk (Cognac, Whisky
) der Menge  mit einem Alkoholgehalt a (Volumenprozent) also einer Alkoholmenge mit einem Alkoholgehalt a (Volumenprozent) also einer Alkoholmenge  . . |
So einfach ist das leider nicht. Volumenprozente beziehen sich auf die Ausgangsvolumina und nicht auf das Volumen der Mischung. Bei idealen Mischungen wäre das egal, aber Ethanol/Wasser ist keine ideale Mischung. Das Volumen der Mischung ist signifikant kleiner als die Summe der Ausgangsvolumina. Ich würde stattdessen mit Stoffmengenkonzentrationen rechnen.
| TomS hat Folgendes geschrieben: | Gesucht ist ein Differentialgleichungssystem für die Verdunstungsrate von Wasser und Alkohol, d.h. insbs. die verbleibenden Mengen ) und und ) . . |
Das wird kompliziert. Dabei sind zusätzlich zum Verteilungsgleichgewicht an der Phasengrenze auch Transportprozesse in den beiden Phasen zu berücksichtigen (Zweites Ficksches Gesetz).
| TomS hat Folgendes geschrieben: | An sich wären bereits die asymptotischen Werte ) und und ) ausreichend. ausreichend. |
Hier würde ich ausnutzen, dass es sich um ein geschlossenes System handelt. Das bedeutet, dass die Stoffmengen konstant bleiben:
 \cdot c_{H_2 O} \left( {c_{C_2 H_5 OH} } \right) + \frac{{V_g \cdot p_{H_2 O} \left( {c_{C_2 H_5 OH} } \right)}}{{R \cdot T}})
 \cdot c_{C_2 H_5 OH} + \frac{{V_g \cdot p_{C_2 H_5 OH} \left( {c_{C_2 H_5 OH} } \right)}}{{R \cdot T}})
Die Stoffmengen kann man aus den Ausgangsvolumina und -konzentrationen berechnen. Die Wasserkonzentration ) und die Gleichgewichtsdampfdrücke und die Gleichgewichtsdampfdrücke ) und und ) in Abhängigkeit von der Alkoholkonzentration in Abhängigkeit von der Alkoholkonzentration  muss man mit Hilfe von Tabellenwerten bestimmen (da habe ich auch die Schnelle leider nichts Brauchbares gefunden). Damit bleiben das finale Gasvolumen muss man mit Hilfe von Tabellenwerten bestimmen (da habe ich auch die Schnelle leider nichts Brauchbares gefunden). Damit bleiben das finale Gasvolumen 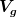 und die Alkoholkonzentration als Unbekannte übrig. Das Gasvolumen lässt sich relativ leicht eliminieren, indem man eine Gleichung nach und die Alkoholkonzentration als Unbekannte übrig. Das Gasvolumen lässt sich relativ leicht eliminieren, indem man eine Gleichung nach 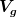 umstellt und in die andere einsetzt. Die Alkoholkonzentration muss man dann numerisch ermitteln. umstellt und in die andere einsetzt. Die Alkoholkonzentration muss man dann numerisch ermitteln.
|
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 27. Feb 2022 11:56 Titel: TomS Verfasst am: 27. Feb 2022 11:56 Titel: |
 |
|
Danke für den Ansatz.
Ich habe etwas anders gerechnet, wäre schön, wenn du mal drüber schauen könntest. Ich gehe zunächst von Stoffmengen aus, nicht von Volumina. Griechische Buchstaben  bezeichnen Stoffmenge und -anteil in in der Dampfphase, bezeichnen Stoffmenge und -anteil in in der Dampfphase,  die selben Größen in der flüssigen Phase. die selben Größen in der flüssigen Phase.
Daltonsches Gesetz:




Raoultsches Gesetz:



zusammen:


 bezeichnet die Gleichgewichtsdampfdrücke (über dem reinen Stoff) bei gegebener Temperatur. bezeichnet die Gleichgewichtsdampfdrücke (über dem reinen Stoff) bei gegebener Temperatur.
Ich betrachte die Flüssigkeit, zunächst mit der ursprünglichen Konzentration, d.h. direkt nach dem erstmaligen Ausschenken und Verschließen, dann später, wenn sich in der geschlossenen Flasche ein Gleichgewicht eingestellt hat. ° bezeichnet die Größen zu Beginn.
Bilanzgleichungen:



da vorher und nachher identischer Druck, Temperatur und Volumen vorliegen; der Term trägt im Endergebnis ohnehin nur in der Größenordnung

bei.
Anwenden der Bilanzgleichungen liefert
\,\frac{p}{\nu} = x_i \, p_i^\ast)
Betrachtet man nur den Alkohol i=a, so ist

und somit


Soweit erst mal ...
_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago. |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5740
|
 DrStupid Verfasst am: 27. Feb 2022 12:50 Titel: DrStupid Verfasst am: 27. Feb 2022 12:50 Titel: |
 |
|
| TomS hat Folgendes geschrieben: | Raoultsches Gesetz:
[...]

|
Das gilt nur für ideale Mischungen. Deshalb habe ich meine Gleichungen so formuliert, dass man mit empirischen Werten für die Konzentrationsabhängigkeit der Gleichgewichtsdampfdrücke rechnen kann.
| TomS hat Folgendes geschrieben: | | da vorher und nachher identischer Druck, Temperatur und Volumen vorliegen |
Die Temperatur und das Gesamtvolumen bleiben gleich, aber der Druck wird sich durch den verdunstenden Alkohol erhöhen. Ich gehe dem Problem aus dem Weg, indem ich den Druck gar nicht verwende. Dadurch muss ich mich auch nicht um die eingeschlossene Luft kümmern. Das setzt natürlich voraus, dass man eventuelle Druckabhängigkeiten der Gleichgewichtsdampfdrücke vernachlässigen kann.
| TomS hat Folgendes geschrieben: | Anwenden der Bilanzgleichungen liefert
\,\frac{p}{\nu} = x_i \, p_i^\ast) |
Abgesehen von den obigen Einschränkungen entspricht das der Bilanz, mit der auch ich rechne.
|
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 28. Feb 2022 09:15 Titel: TomS Verfasst am: 28. Feb 2022 09:15 Titel: |
 |
|
Erst mal danke.
| DrStupid hat Folgendes geschrieben: | | Das gilt nur für ideale Mischungen. Deshalb habe ich meine Gleichungen so formuliert, dass man mit empirischen Werten für die Konzentrationsabhängigkeit der Gleichgewichtsdampfdrücke rechnen kann. |
Na ja, man muss ja mal Theorie und Experiment abgleichen.
Eine übliche Korrektur ist übrigens

mit Fugazität phi Aktivität gamma.
https://en.wikipedia.org/wiki/Fugacity
https://en.wikipedia.org/wiki/Activity_coefficient
| DrStupid hat Folgendes geschrieben: | | TomS hat Folgendes geschrieben: | | da vorher und nachher identischer Druck, Temperatur und Volumen vorliegen |
Die Temperatur und das Gesamtvolumen bleiben gleich, aber der Druck wird sich durch den verdunstenden Alkohol erhöhen. |
Nee, auch die Temperatur bleibt nicht exakt gleich, das sind alles nur Näherungen.
| DrStupid hat Folgendes geschrieben: | | Ich gehe dem Problem aus dem Weg, indem ich den Druck gar nicht verwende. |
Verstehe ich nicht. Solange ich von einer konstanten Stoffmenge in der gasförmigen Phase ausgehe und die Gültigkeit der idealen Gasgleichungen voraussetze, sind unsere Ansätze doch exakt äquivalent.
Du hast den Druck doch nur durch die ideale Gasgleichungen eliminiert - die ja auch nur eine Näherung ist. Solange das Füllvolumen mit Flüssigkeit hoch ist, sind alle diese alle diese Effekte von der Ordnung  klein. klein.
Eine vergleichsweise große Unsicherheit besteht in der Art und Weise, wie die Flasche einmalig oder in mehreren Schritten bis zu einem gewissen Füllstand entleert wird und dabei Luft aus der Flache mit der Umgebung ausgetauscht wird. Den Effekt halte ich in der Praxis für deutlich relevanter als die bisher diskutierten Unsicherheiten.
| DrStupid hat Folgendes geschrieben: | | Abgesehen von den obigen Einschränkungen entspricht das der Bilanz, mit der auch ich rechne. |
Danke.
_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago. |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5740
|
 DrStupid Verfasst am: 28. Feb 2022 09:51 Titel: DrStupid Verfasst am: 28. Feb 2022 09:51 Titel: |
 |
|
| TomS hat Folgendes geschrieben: | Eine übliche Korrektur ist übrigens

mit Fugazität phi Aktivität gamma. |
Die sind auch konzentrationsabhängig. Die Aktivität von Ionen in wässriger Lösung kann man noch theoretisch abschätzen (Debye-Hückel), aber bei einem Alkohol/Wasser-Gemisch landest Du am Ende doch wieder bei empirischen Werten. Da kannst Du auch gleich empirische Werte für den Gleichgewichtsdampfdruck verwenden.
| TomS hat Folgendes geschrieben: | | Nee, auch die Temperatur bleibt nicht exakt gleich |
Oben hast Du geschrieben:
| TomS hat Folgendes geschrieben: | | Die Temperatur soll über den gesamten Zeitraum als konstant angesehen werden. |
Das kannst Du natürlich ändern, aber dann wird das Ganze nochmal deutlich komplizierter, weil dann nicht nur Konzentrations- sondern auch Temperaturabhängigkeiten berücksichtigt werden müssen.
| DrStupid hat Folgendes geschrieben: | | Solange ich von einer konstanten Stoffmenge in der gasförmigen Phase ausgehe und die Gültigkeit der idealen Gasgleichungen voraussetze, sind unsere Ansätze doch exakt äquivalent. |
Die Stoffmenge in der gasförmigen Phase ist nicht konstant. Wenn das der Fall wäre, dann gäbe es nichts zu berechnen. Hier geht es doch gerade um den Stofftransport aus der flüssigen in die gasförmigen Phase.
| DrStupid hat Folgendes geschrieben: | | Eine vergleichsweise große Unsicherheit besteht in der Art und Weise, wie die Flasche einmalig oder in mehreren Schritten bis zu einem gewissen Füllstand entleert wird und dabei Luft aus der Flache mit der Umgebung ausgetauscht wird. |
Das entspricht auch nicht Deinen ursprünglichen Annahmen. Oben hast Du vorausgesetzt, dass der initale Alkoholgehalt der Gasphase Null ist. Auch hier gilt, dass Du das verändern kannst, aber damit ändert sich auch der Ansatz. Der Stoffaustausch mit der Umgebung ist ein Thema für sich. Den kann man wahrscheinlich gar nicht sinnvoll berechnen.
|
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 28. Feb 2022 09:59 Titel: TomS Verfasst am: 28. Feb 2022 09:59 Titel: |
 |
|
Der eigentlich spannende Punkt ist ja der Effekt des Entleerens und des Gasvolumens. D.h. man formuliert


um, in dem man das Gesamtvolumen V einmal vollständig mit Flüssigkeit und ein anderes mal vollständig mit Gas gefüllt ansieht. Daraus folgen die jeweiligen maximalen Stoffmengen. Für einen Volumenbruchteil v des Gesamtvolumens V, das von der Flüssigkeit eingenommen wird, gilt dann
 = \frac{p_a^\ast}{p} \frac{\nu^0}{n^0} = \frac{p_a^\ast}{p} \frac{\nu^\text{max}}{n^\text{max}} \cdot \frac{1-v}{v} )
D.h. der wesentliche Effekt folgt im Grenzfall von kleinem v.
Wenn ich mich nicht verrechnet habe, erhalte ich für 50% (vol). Alkohol außerdem


_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago. |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5740
|
 DrStupid Verfasst am: 28. Feb 2022 10:46 Titel: DrStupid Verfasst am: 28. Feb 2022 10:46 Titel: |
 |
|
| TomS hat Folgendes geschrieben: | Der eigentlich spannende Punkt ist ja der Effekt des Entleerens und des Gasvolumens. D.h. man formuliert


um, in dem man das Gesamtvolumen V einmal vollständig mit Flüssigkeit und ein anderes mal vollständig mit Gas gefüllt ansieht. |
Ich verstehe nicht so ganz, worum es eigentlich geht. Ursprünglich klang es so, als ob eine leere Flasche teilweise gefüllt und dann verschlossen wird. Nur dann kann man ja davon ausgehen, dass der initiale Alkoholgehalt in der Gasphase Null ist.
Später klang es dann so, als ob eine volle Flasche schrittweise entleert und zwischendurch verschlossen wird. Dann geht man am besten davon aus, dass die Gasphase zunächst mit Alkohol gesätigt ist und dann ein bestimmtes Flüssigkeitsvolumen durch frische Luft ersetzt wird. Das ist dann der Ausgangangspunkt für die Berechnung des neuen Gleichgewichts.
Jetzt sprichst Du davon, das Volumen einmal vollständig mit Luft bzw. Gas zu füllen. Das klingt wieder vollkommen anders. Deshalb muss ich an dieser Stelle fragen, worum es eigentlich geht, damit wir nicht aneinander vorbei reden.
| TomS hat Folgendes geschrieben: | Wenn ich mich nicht verrechnet habe, erhalte ich für 50% (vol). Alkohol außerdem

|
Ich komme auf einen anderen Wert. Der Dampfdruck von reinem Ethanol ist rund 58 hPa. 50 Vol% Ethanol entsprechen ungefähr einem Stoffmengenanteil von 0,24. Wenn ich in Ermangelung von empirischen Daten für den Dampfdruck über der Mischung das Raoultsche Gesetz verwende, dann ergibt das einen Gleichgewichtsdampfdruck von rund 14 hPa. Wenn der initiale Alkoholgehalt der Gasphase Null ist, dann kommt der komplette Gleichgewichtsdampfdruck des Alkohols zum Luftdruck von 1013 hPa dazu. Damit gilt im Gleichgewicht unter Vernachlässigung des veränderten Alkoholgehalts in der flüssigen Phase

|
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 28. Feb 2022 13:39 Titel: TomS Verfasst am: 28. Feb 2022 13:39 Titel: |
 |
|
| DrStupid hat Folgendes geschrieben: | | TomS hat Folgendes geschrieben: | Der eigentlich spannende Punkt ist ja der Effekt des Entleerens und des Gasvolumens. D.h. man formuliert


um, in dem man das Gesamtvolumen V einmal vollständig mit Flüssigkeit und ein anderes mal vollständig mit Gas gefüllt ansieht. |
Ich verstehe nicht so ganz, worum es eigentlich geht. |
Sorry, das ist nur ein Missverständnis.
| DrStupid hat Folgendes geschrieben: | | Ursprünglich klang es so, als ob eine leere Flasche teilweise gefüllt und dann verschlossen wird. Nur dann kann man ja davon ausgehen, dass der initiale Alkoholgehalt in der Gasphase Null ist. |
| DrStupid hat Folgendes geschrieben: | | Später klang es dann so, als ob eine volle Flasche schrittweise entleert und zwischendurch verschlossen wird. Dann geht man am besten davon aus, dass die Gasphase zunächst mit Alkohol gesätigt ist und dann ein bestimmtes Flüssigkeitsvolumen durch frische Luft ersetzt wird. Das ist dann der Ausgangangspunkt für die Berechnung des neuen Gleichgewichts. |
| DrStupid hat Folgendes geschrieben: | | Jetzt sprichst Du davon, das Volumen einmal vollständig mit Luft bzw. Gas zu füllen. Das klingt wieder vollkommen anders. |
Ok, ich sehe, ich muss das nochmal klarstellen.
Eine Flasche ist zu 100% mit Whisky gefüllt; die winzige Luftmenge oben drüber vernachlässigen wir.
Die Flasche wird in der Praxis glasweise zu ca. 4 cl ausgeschenkt. Dabei findet bei jedem Ausschenkvorgang ein teilweises Entweichen der bereits teilweise mit Alkohol gesättigten Luft und ein Eintreten von frischer, ungesättigter Luft statt. Bis zum nächsten Ausschenkvorgang - in einer Stunde oder ein paar Tagen - findet ein Verdunsten des Alkohols aus dem Whisky statt. Das iterieren wir. Diese reale Betrachtung ist mir für den Anfang aber zu kompliziert (ich habe das nur erwähnt, weil du auf Näherungen hingewiesen hast, ich jedoch der Meinung bin, dass der Fall des iterierten Ausschenken viel höhere und völlig unbekannte Ungenauigkeiten liefert).
Deswegen betrachte ich eine halb volle Flasche mit Alkoholgehalt Null in der Luft oben auf, wobei in der Folge Verdunstung und Sättigung eintritt. Das ist aber äquivalent dazu, dass ich eine volle Flasche betrachte, sofort die Hälfte ausschenke und in der Folge Sättigung eintritt.
Meine letzte Formel sagt genau das, die einzige Erweiterung ist, dass ich nicht von Füllstand v = 50% ausgehe sondern v variabel halte.
_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago. |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5740
|
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5740
|
 DrStupid Verfasst am: 28. Feb 2022 18:16 Titel: DrStupid Verfasst am: 28. Feb 2022 18:16 Titel: |
 |
|
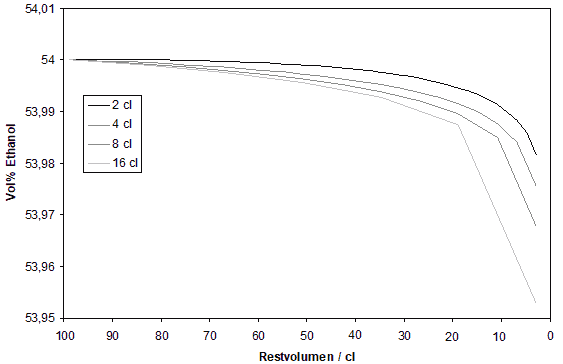
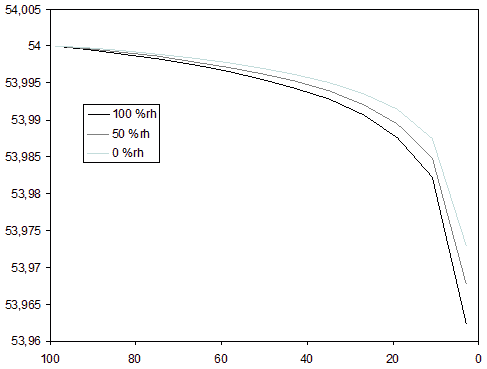
Ich habe jetzt mal den Fall durchgerechnet, dass bei jedem Ausschenken genau so viel Luft in die Flasche strömt, wie Flüssigkeit rausfließt (siehe Anhang). Die Ausgangskonzentration ist jeweils 54 Vol%, aber das Ausschenken erfolgt in unterschiedlichen Schritten von 2, 4, 8 bzw. 16 cl. Die relative Luftfeuchtigkeit habe ich auf 50 % gesetzt.
Auch nach meiner Rechnung spielt die Abnahme der Konzentration bei realistischen Restmengen praktisch keine Rolle.
| Beschreibung: |
|
| Dateigröße: |
5.09 KB |
| Angeschaut: |
3290 mal |
|
Zuletzt bearbeitet von DrStupid am 28. Feb 2022 23:58, insgesamt einmal bearbeitet |
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 28. Feb 2022 22:20 Titel: TomS Verfasst am: 28. Feb 2022 22:20 Titel: |
 |
|
| DrStupid hat Folgendes geschrieben: | | Auch nach meiner Rechnung spielt die Abnahme der Konzentration bei realistischen Restmengen praktisch keine Rolle. |
Ja.
| DrStupid hat Folgendes geschrieben: | | Die relative Luftfeuchtigkeit habe ich auf 50 % gesetzt. |
An welcher Stelle geht das denn in deine Rechnungen ein? Bei mir nur in Termen der Größenordnung

_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago. |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5740
|
 DrStupid Verfasst am: 28. Feb 2022 22:46 Titel: DrStupid Verfasst am: 28. Feb 2022 22:46 Titel: |
 |
|
| TomS hat Folgendes geschrieben: | | An welcher Stelle geht das denn in deine Rechnungen ein? |
Bei der Berechnung der Gesamtstoffmenge des Wassers zu Beginn des Prozesses und nach jedem Ausschenken.
|
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 28. Feb 2022 23:03 Titel: TomS Verfasst am: 28. Feb 2022 23:03 Titel: |
 |
|
| DrStupid hat Folgendes geschrieben: | | TomS hat Folgendes geschrieben: | | An welcher Stelle geht das denn in deine Rechnungen ein? |
Bei der Berechnung der Gesamtstoffmenge des Wassers zu Beginn des Prozesses und nach jedem Ausschenken. |
Klar.
Aber hat diese Größe überhaupt einen merklichen Einfluss, solange die Restmenge Flüssigkeit noch deutlich mehr Wasser enthält das das darüber befindliche Luftvolumen?
_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago. |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5740
|
 DrStupid Verfasst am: 28. Feb 2022 23:54 Titel: DrStupid Verfasst am: 28. Feb 2022 23:54 Titel: |
 |
|
| TomS hat Folgendes geschrieben: | | Aber hat diese Größe überhaupt einen merklichen Einfluss, solange die Restmenge Flüssigkeit noch deutlich mehr Wasser enthält das das darüber befindliche Luftvolumen? |
Groß ist der Unterschied nicht, aber er ist da:
| Beschreibung: |
|
| Dateigröße: |
4.55 KB |
| Angeschaut: |
3291 mal |
|
|
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 01. März 2022 05:49 Titel: TomS Verfasst am: 01. März 2022 05:49 Titel: |
 |
|
Nochmal zum Verständnis.
Jeder Partialdruck ändert sich unabhängig von allen anderen, wenn man den Gesamtdruck konstant hält und chemische Reaktionen außer Acht lässt. Ob also der Partialdruck in der Gasphase von Wasser oder "Luft" stammt, ist für den Partialdruck von Alkohol unerheblich.
Zumindest ist das in meinem Ansatz so. Was übersehe ich?
_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago. |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5740
|
 DrStupid Verfasst am: 01. März 2022 09:00 Titel: DrStupid Verfasst am: 01. März 2022 09:00 Titel: |
 |
|
| TomS hat Folgendes geschrieben: | | Jeder Partialdruck ändert sich unabhängig von allen anderen, wenn man den Gesamtdruck konstant hält und chemische Reaktionen außer Acht lässt. |
Ja. Sie ändern sich auch unabhängig voneinander, wenn man den Gesamtdruck nicht konstant hält (wovon ich in meiner Rechnung ausgehe).
| TomS hat Folgendes geschrieben: | | Was übersehe ich? |
Der Alkoholgehalt der flüssigen Phase ändert sich nicht nur durch Verdunstung von Alkohol, sondern auch durch Verdunstung oder Kondensation von Wasser. Letzteres hängt von der Luftfeuchtigkeit ab.
|
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 03. März 2022 06:44 Titel: TomS Verfasst am: 03. März 2022 06:44 Titel: |
 |
|
| DrStupid hat Folgendes geschrieben: | | Der Alkoholgehalt der flüssigen Phase ändert sich nicht nur durch Verdunstung von Alkohol, sondern auch durch Verdunstung oder Kondensation von Wasser. Letzteres hängt von der Luftfeuchtigkeit ab. |
Letzteres [Verdunstung oder Kondensation von Wasser hängt von der Luftfeuchtigkeit ab] ist natürlich richtig.
Aber da folgendes
| DrStupid hat Folgendes geschrieben: | | Sie ändern sich unabhängig voneinander
|
| TomS hat Folgendes geschrieben: | \,\frac{p}{\nu} = x_a \, p_a^\ast)
 |
gilt, spielt die genaue initiale Zusammensetzung des Gases  für für  keine Rolle. Es ändern sich lediglich die einzelnen keine Rolle. Es ändern sich lediglich die einzelnen  wobei wobei


invariant ist.
_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago. |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5740
|
 DrStupid Verfasst am: 03. März 2022 09:50 Titel: DrStupid Verfasst am: 03. März 2022 09:50 Titel: |
 |
|
| TomS hat Folgendes geschrieben: | Aber da folgendes
| DrStupid hat Folgendes geschrieben: | | Sie ändern sich unabhängig voneinander
|
| TomS hat Folgendes geschrieben: | \,\frac{p}{\nu} = x_a \, p_a^\ast)
 |
gilt |
Das gilt nur näherungsweise. Wenn man so genau rechnen will, dass der Einfluss der Luftfeuchtigkeit erkennbar wird, dann kann man n und p nicht mehr als konstant annehmen. Sie hängen von der Verteilung aller Komponenten ab. Das ist in meinem Ansatz oben mit dem Gasvolumen Vg berücksichtigt, das in den Bilanzgleichungen aller Komponenten auftaucht. Damit sind die Gleichungern nicht mehr unabhängig voneinander, sondern bilden ein nichtlineares Gleichungssystem.
|
|
 |
|