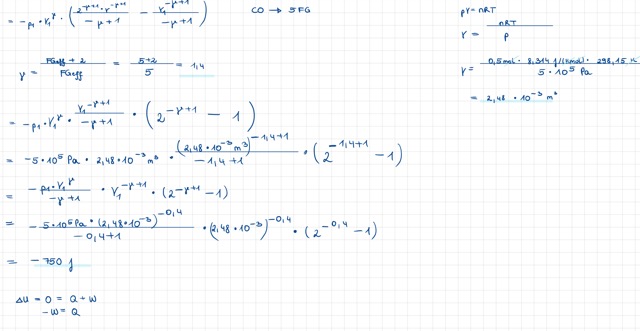| Autor |
Nachricht |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 20. Nov 2021 19:51 Titel: Reversible/ adiabatische Expansion frage1 Verfasst am: 20. Nov 2021 19:51 Titel: Reversible/ adiabatische Expansion |
 |
|
Hallo alle miteinander!
Da ich auf meine letzte Frage keine Antwort bekommen habe, stelle ich die Frage hier erneut.
Die Aufgabe lautet:
Ein Zylinder mit Kolben wird mit n=0,5 mol Kohlenmonoxidgas (wird als ideales Gas angenommen) befüllt, wobei p1=5 bar, T1=25 °C gemessen wird.
c) Wie groß ist die Volumenarbeit w und der Wärmeaustausch q bei dieser Expansion (diskutieren Sie das Vorzeichen)?
d) Wie groß ist die Volumenarbeit w, der Wärmeaustausch q und die Änderung der Inneren Energie dU, wenn diese Expansion adiabatisch erfolgt?
e) Berechnen Sie daraus die Temperatur T3. Zeichnen Sie schematisch ein entsprechendes p,V-Diagramm.
Meine Fragen:
Warum ist bei der isolierten Expansion die Wärme q=0 ? Wie hätte man das wissen sollen? Also es ist ja dQ=d -w(isotherm), die Wärme ist gleich der verrichteten Arbeit, aber wieso? Wie kann ich mir das erklären?
Und bei der adiabatischen haben wir im Vergleich zur reversiblen weniger Arbeut geleistet. Aber wieso? Könnt ihr mir das erklären?
Ich wäre wirklich sehr froh, wenn ihr mir weiterhelfen könnt, da ich mich tagelang mit diesem Thema auseinandergesetzt habe. Ich hoffe, dass ich diesmal eine Antwort bekomme und bedanke mich im Voraus für jegliche Hilfe !
| Beschreibung: |
|
| Dateigröße: |
55.49 KB |
| Angeschaut: |
2156 mal |
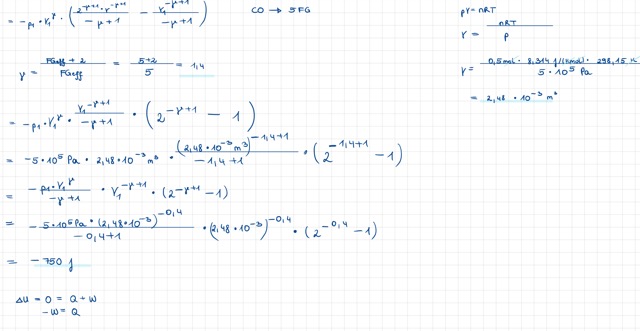
|
| Beschreibung: |
|
| Dateigröße: |
65.03 KB |
| Angeschaut: |
2156 mal |

|
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 5955
|
 Myon Verfasst am: 20. Nov 2021 21:30 Titel: Re: Reversible/ adiabatische Expansion Myon Verfasst am: 20. Nov 2021 21:30 Titel: Re: Reversible/ adiabatische Expansion |
 |
|
| frage1 hat Folgendes geschrieben: | Warum ist bei der isolierten Expansion die Wärme q=0 ? Wie hätte man das wissen sollen? Also es ist ja dQ=d -w(isotherm), die Wärme ist gleich der verrichteten Arbeit, aber wieso? Wie kann ich mir das erklären?
Und bei der adiabatischen haben wir im Vergleich zur reversiblen weniger Arbeut geleistet. Aber wieso? Könnt ihr mir das erklären? |
Nur ganz kurz, ich kann morgen ausführlicher antworten, wenn das bis dahin nicht schon jemand anders getan hat.
(Wärme-)isoliert heisst kein Wärmeaustausch, also dQ=0.
Die Adiabaten verlaufen steiler als die Isothermen. Bei einer Expansion nimmt der Druck stärker ab (die Temperatur sinkt, da die Expansionsarbeit auf Kosten der inneren Energie geht), und das Gas leistet weniger Arbeit.
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 5955
|
 Myon Verfasst am: 21. Nov 2021 09:32 Titel: Myon Verfasst am: 21. Nov 2021 09:32 Titel: |
 |
|
Für die Arbeit dW erhalte ich in b) und c) etwa die gleichen Werte. Die Arbeit ist negativ, da von aussen keine Arbeit dem System zugeführt wird, sondern im Gegenteil das Gas bei der Expansion Arbeit leistet.
In b) gilt wegen dU=0 nun dQ=-dW, d.h. dQ ist positiv - es wird Wärme zugeführt. Dazu noch eine Anmerkung, auch zu den Fragen im ersten Thread zur gleichen Aufgabe: Die Wärme ist im Gegensatz zur inneren Energie keine Zustandsgrösse. Man kann nicht sagen, die Wärme des Systems hat zu- oder abgenommen, sondern man führt dem System Energie in Form von Wärme zu, oder das System gibt Wärme nach aussen ab. Das erste kann geschehen, wenn das System in thermischem Kontakt mit einem anderen System steht, welches eine höhere Temperatur hat. Umgekehrt kann ein Gas Wärme abgeben an ein System, welches eine tiefere Temperatur hat als das Gas.
In c) gilt dQ=0 und somit dU=dW, die innere Energie nimmt ab. Anstatt über die Arbeit hätte Aufgabe c) auch gelöst werden können, indem man nutzt dass bei einem idealen Gas gilt
=n\frac{f}{2}R(T_2-T_1))
T2 ergibt sich aus der Adiabatengleichung  . .
|
|
 |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 21. Nov 2021 14:14 Titel: frage1 Verfasst am: 21. Nov 2021 14:14 Titel: |
 |
|
Erstmal danke Myon, dass du mir geantwort hast.
Ich habe gerade eben bemerkt, dass meine Fragen nicht ausführlich genug waren.
Also bei c) versteh ich nicht nicht, warum delta Q gleich der verrichteten Arbeit ist. Die innere Energie muss zwar konstant bleiben wegen 1. HS der Thermodynamik, aber ich kann mir immer noch nicht erklären, warum q=-w, also warum q=860 J? Das System verrichtet Arbeit, indem das Gas expandiert. Aber welcher Zusammenhang besteht jetzt zwischen Arbeit und Wärme?
Wir führen doch dem Sytsem keine Wärme hinzu oder?
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 5955
|
 Myon Verfasst am: 21. Nov 2021 16:21 Titel: Myon Verfasst am: 21. Nov 2021 16:21 Titel: |
 |
|
Ich sehe gerade, dass ich oben mit der Nummerierung der Teilaufgaben durcheinander gekommen bin. Was zu b) stand, betrifft in richtigerweise Teilaufgabe c), was zu c) stand, betrifft Teilaufgabe d).
Also zu c), der isothermen Expansion. "Isotherm" heisst bei einem idealen Gas dU=0, da bei einem idealen Gas die innere Energie nur von der Temperatur abhängt. Aus dU=0 folgt wiederum dQ=-dW.
Mit dem Vorzeichen ist es auch vernünftig so, denn: es muss Energie zugeführt werden, damit das Gas gegen äusseren Druck expandieren und damit Arbeit verrichten kann, und gleichzeitig die Temperatur konstant bleibt. Umgesetzt werden könnte das, indem z.B. die Gefässwände auf einer konstanten Temperatur gehalten werden. Dann wird durch die Wände Wärme auf das Gas übertragen.
PS: dQ=+860J, es muss Wärme zugeführt werden!
|
|
 |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 21. Nov 2021 17:34 Titel: frage1 Verfasst am: 21. Nov 2021 17:34 Titel: |
 |
|
Vielen lieben Dank Myon!
Ich glaube, ich habs jetzt verstanden. Ich fasse es kurz zusammen:
Wir haben hier ein System vorliegen, das isotherm ist. Damit das Gas expandieren kann, muss Energie in das System zugeführt werden, d.h. Q bekommt dann ein positives Vorzeichen. Da wir isotherm sind, darf sich die Temperatur nicht ändern. Da die innere Energie von der Temperatur abhängt, ist sie auch konstant. Die innere Energie darf sich sowieso nicht ändern ( 1. Hauptsatz der Themrodynamik). Da die innere Energie konstant ist, können wir die Gleichung dU=0=q + w umformen zu dq= -dw. Für die Volumenarbeit haben wir -860 J rausbekommen, d.h. das Gas verrichtet Arbeit, indem es expandiert. Deswegen bekommt die Arbeit ein negatives Vorzeichen, da das Gas Arbeit verrichtet. Des Weiteren haben wir Energie in das System zugeführt, d.h, es wird am System Arbeit verrichtet, also das System gewinnt an Energue sozusagen. Deswegen bekommt q ein positives Vorzeichen. Was an Energie freigesetzt wurde, muss wieder Energie aufgenommen werden. Stimmt meine Überlegung so?
Und wenn wir zu d) gehen: wie sieht die adiabatische Expansion aus?
Warum ist eigentlich dU= w? Ich weiß zwar, dass bei einem adiabatischen Prozess keine Wärme mit der Umgebung ausgetauscht wird, aber wie hängen dU und dw zusammen? Wieso können wir sagen, dass die Arbeit gleich der inneren Energie ist. Und wieso ändert sich hier die Temperatur, obwohl kein Wärmetausch stattfindet? Muss dann die Temperatur nicht konstant bleiben?
Da hab ich noch Verständnisprobleme.
Und nochmals danke für deine Hilfe!
|
|
 |
Nils Hoppenstedt

Anmeldungsdatum: 08.01.2020
Beiträge: 2022
|
 Nils Hoppenstedt Verfasst am: 21. Nov 2021 20:39 Titel: Nils Hoppenstedt Verfasst am: 21. Nov 2021 20:39 Titel: |
 |
|
| frage1 hat Folgendes geschrieben: | Damit das Gas expandieren kann, muss Energie in das System zugeführt werden, d.h. Q bekommt dann ein positives Vorzeichen.
|
Es ist nicht klar, was du hier unter "Energie" verstehst. Daher nochmal konkret: Das Gas nimmt während der Expansion Wärme auf, daher ist dQ > 0 und verrichtet gleichzeitig Arbeit, daher ist dW < 0.
| frage1 hat Folgendes geschrieben: |
Da wir isotherm sind, darf sich die Temperatur nicht ändern. Da die innere Energie von der Temperatur abhängt, ist sie auch konstant.
|
Ja. Oder genauer gesagt, da die innere Energie bei fester Teilchenzahl NUR von der Temperatur abhängt.
| frage1 hat Folgendes geschrieben: |
Die innere Energie darf sich sowieso nicht ändern ( 1. Hauptsatz der Themrodynamik).
|
Auch hier bin ich mir nicht sicher, ob du obigen Satz allgemein oder im Kontext der Aufgabe meinst. Daher sei nochmal zur Sicherheit erwähnt, dass sich die innere Energie eines Systems im Allgemeinen natürlich ändern kann.
| frage1 hat Folgendes geschrieben: |
Da die innere Energie konstant ist, können wir die Gleichung dU=0=q + w umformen zu dq= -dw. Für die Volumenarbeit haben wir -860 J rausbekommen, d.h. das Gas verrichtet Arbeit, indem es expandiert. Deswegen bekommt die Arbeit ein negatives Vorzeichen, da das Gas Arbeit verrichtet.
|
Das ist richtig.
| frage1 hat Folgendes geschrieben: |
Des Weiteren haben wir Energie in das System zugeführt, d.h, es wird am System Arbeit verrichtet, also das System gewinnt an Energue sozusagen. Deswegen bekommt q ein positives Vorzeichen. Was an Energie freigesetzt wurde, muss wieder Energie aufgenommen werden. Stimmt meine Überlegung so?
|
Hier sind verschiedene Formen von Energie im Spiel: innere Energie, Wärme und Arbeit. Wenn du pauschal von "Energie" sprichst, ist nicht klar, was du meinst. Daher nochmal: Das Gas nimmt Wärme auf (dQ > 0) und verrichtet gleichzeitig Arbeit (dW < 0), während seine innere Energie gleich bleibt (dU = 0). Mehr gibt es hier eigentlich nicht zu sagen.
| frage1 hat Folgendes geschrieben: |
Und wenn wir zu d) gehen: wie sieht die adiabatische Expansion aus?
Warum ist eigentlich dU= w? Ich weiß zwar, dass bei einem adiabatischen Prozess keine Wärme mit der Umgebung ausgetauscht wird, aber wie hängen dU und dw zusammen?
|
Na, die hängen über den 1. Hauptsatz zusammen: dU = dQ + dW
| frage1 hat Folgendes geschrieben: |
Wieso können wir sagen, dass die Arbeit gleich der inneren Energie ist.
|
Ich glaube, du hast den 1. HS noch nicht richtig verstanden. dU = dW bedeutet, dass die Arbeit gleich der Änderung der inneren Energie ist.
| frage1 hat Folgendes geschrieben: |
Und wieso ändert sich hier die Temperatur, obwohl kein Wärmetausch stattfindet? Muss dann die Temperatur nicht konstant bleiben?
|
Die Temperatur ändert sich, da das System durch das Verrichten von Arbeit Energie verliert.
Viele Grüße,
Nils
_________________
Ihr da Ohm macht doch Watt ihr Volt! |
|
 |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 05. Dez 2021 13:11 Titel: frage1 Verfasst am: 05. Dez 2021 13:11 Titel: |
 |
|
|
Nils Hoppenstedt, ich hab mich wieder mit diesem Thema auseinandergesetzt und hab den großteils verstanden. Danke dir vielmals! Aber eine Frage hätte ich noch: Warum hängt die innere Energie eines Systems NUR von der Temperatur ab? Liegt das daran, dass das gas während der Expansion Wärme aufnimmt und durch das Verrichten von Arbeit wieder Wärme verliert und die Temperatur sich dabei ändert. Zuerst muss Wärme an ein System zugeführt werden, damit das gas arbeit verrichten kann. Und durch das Verrichten von Arbeit verliert das Gas wieder seine Wärme, d.h., dass sich die Temperatur ständig ändert? Aber ich kann ja genau so sagen, dass die innere Energie von der Wärme q abhängt? Wie sich die innere Energie ändert hängt ja eigentlich von der Wärme ab?
|
|
 |
schnudl
Moderator

Anmeldungsdatum: 15.11.2005
Beiträge: 6979
Wohnort: Wien
|
 schnudl Verfasst am: 05. Dez 2021 13:42 Titel: schnudl Verfasst am: 05. Dez 2021 13:42 Titel: |
 |
|
| frage1 hat Folgendes geschrieben: | | Warum hängt die innere Energie eines Systems NUR von der Temperatur ab? |
Das tut sie i.A. auch nicht. Beim idealen Gas (und um das geht es hier ja) ist dies aber der Fall.
_________________
Wenn du eine weise Antwort verlangst, musst du vernünftig fragen (Goethe) |
|
 |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 05. Dez 2021 13:52 Titel: frage1 Verfasst am: 05. Dez 2021 13:52 Titel: |
 |
|
Ja, und wieso hängt dann die innere Energie beim idealen Gas NUR von der Temperatur ab?
Also was ich grundsätzlich nicht verstehe ist, warum wir sagen können dass die innere energie nur von der Temperatur abhängt , obwohl da andere Größen wie Wärme und Arbeit auch eine Rolle spielen
|
|
 |
Nils Hoppenstedt

Anmeldungsdatum: 08.01.2020
Beiträge: 2022
|
 Nils Hoppenstedt Verfasst am: 05. Dez 2021 14:55 Titel: Nils Hoppenstedt Verfasst am: 05. Dez 2021 14:55 Titel: |
 |
|
Hi,
Mach dir bitte zunächst einmal den grundsätzlichen Unterschied der Begriffe klar: die innere Energie und die Temperatur eines Systems sind Zustandsgrößen, beschreiben also den Zustand des Systems. Wärme und Arbeit sind hingegen Prozessgrößen. Sie beschreiben die Energie, die zwischen dem System und seiner Umgebung ausgetauscht wird. Die innere Energie kann also schon rein konzeptionell gar nicht von der Wärme abhängen, weil die Wärme den Zustand überhaupt nicht beschreibt. Was man aber natürlich sagen kann, ist dass die Änderung der inneren Energie von der ausgetauschten Arbeit und ausgetauschten Wärme abhängt (1. HS der Thermodynamik).
| Zitat: | Ja, und wieso hängt dann die innere Energie beim idealen Gas NUR von der Temperatur ab?
Also was ich grundsätzlich nicht verstehe ist, warum wir sagen können dass die innere energie nur von der Temperatur abhängt , obwohl da andere Größen wie Wärme und Arbeit auch eine Rolle spiele |
Erstmal was grundsätzliches: Die innere Energie ist die Gesamtheit aller Energieformen, die einem System enthalten ist. Sie umfasst also sowohl die kinetische Energie der Teilchen (wozu auch Rotationen und Schwingungen gehören) als auch die potenzielle Energie aufgrund der anziehenden oder abstoßenden Wechselwirkung.
Das ideale Gas ist ein sehr einfaches Modell eines Systems, in dem die Teilchen untereinander außer durch elastische Stöße nicht wechselwirken. In diesem einfachen Modell besteht die innere Energie also nur aus der kinetischen Energie seiner Teilchen. Und da die Temperatur ein Maß für die kinetische Energie ist, hängt in diesem Modell die innere Energie auch nur von der Temperatur ab.
Beim realen Gas ist das schon anders. Hier wird neben der kinetischen Energie auch die potenzielle Energie der Teilchen berücksichtigt. Folglich hängt hier die innere Energie nicht nur von der Temperatur ab, sondern es gilt (im Van-der-Waals-Modell ohne innere Freiheitsgrade):

Die innere Energie hängt in diesem Modell also neben der Temperatur noch zusätzlich vom Volumen ab.
Und natürlich gibt es noch komplexere Modelle, in denen der Zusammenhang noch komplizierter ist.
Viele Grüße,
Nils
P.S.: Hier noch ein Bild aus dem Netz, das die Begrifflichkeiten ganz gut veranschaulicht. Es ist vielleicht nicht ganz optimal, da die Schwingungsenergie und die potenzielle Energie nicht aufgeführt sind, zeigt aber das grundsätzliche Konzept.
| Beschreibung: |
|
Download |
| Dateiname: |
innere-energie.png |
| Dateigröße: |
132.58 KB |
| Heruntergeladen: |
156 mal |
_________________
Ihr da Ohm macht doch Watt ihr Volt! |
|
 |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 09. Dez 2021 23:43 Titel: frage1 Verfasst am: 09. Dez 2021 23:43 Titel: |
 |
|
Sehr sehr gut erklärt Nils Hoppenstedt, danke dir vielmals!
Aber eine letzte Frage hätte ich noch:
Du hast gesagt, dass die innere Energie eine Zustandsgröße ist, d.h. Sie ist wegunabhängig. Nun stellt sich die Frage, warum die innere E. wegunabhängig ist. Wie kann ich mir das vorstellen. Denn der 1. HS der Thermodynamik besagt ja, dass sich die Änderung der inneren Energie aus der zugeführten Wärmemenge und der am Körper geleisteten Arbeit zusammensetzt. Ist das der Grund warum dU wegunabhängig ist?
|
|
 |
Nils Hoppenstedt

Anmeldungsdatum: 08.01.2020
Beiträge: 2022
|
 Nils Hoppenstedt Verfasst am: 09. Dez 2021 23:59 Titel: Nils Hoppenstedt Verfasst am: 09. Dez 2021 23:59 Titel: |
 |
|
| frage1 hat Folgendes geschrieben: |
Du hast gesagt, dass die innere Energie eine Zustandsgröße ist, d.h. Sie ist wegunabhängig. Nun stellt sich die Frage, warum die innere E. wegunabhängig ist. |
Na, weil sie eine Zustandsgröße ist und folglich nur vom Zustand abhängt. Das ist sozusagen die Definition einer Zustandsgröße.
- Nils
_________________
Ihr da Ohm macht doch Watt ihr Volt! |
|
 |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 10. Dez 2021 00:09 Titel: frage1 Verfasst am: 10. Dez 2021 00:09 Titel: |
 |
|
Tut mir leid, dass ich die Frage ungenau gestellt habe.
Also generell versteh´ich nicht was ich unter wegunabhängig verstehen soll.
Ja, die innere Energie ist eine Zustandsgröße, aber was hat die Wegunabhängigkeit mit dem Zustand eines Systems zu tun? da haperts bei mir noch.
Und nochmal danke für deine vorherige Erklärung. Dank dir habe ich den Zusammenhang zwischen innere Energie und Temperatur endlich verstanden.
|
|
 |
Nils Hoppenstedt

Anmeldungsdatum: 08.01.2020
Beiträge: 2022
|
|
 |
schnudl
Moderator

Anmeldungsdatum: 15.11.2005
Beiträge: 6979
Wohnort: Wien
|
 schnudl Verfasst am: 10. Dez 2021 18:10 Titel: schnudl Verfasst am: 10. Dez 2021 18:10 Titel: |
 |
|
| frage1 hat Folgendes geschrieben: | Tut mir leid, dass ich die Frage ungenau gestellt habe.
Also generell versteh´ich nicht was ich unter wegunabhängig verstehen soll.
Ja, die innere Energie ist eine Zustandsgröße, aber was hat die Wegunabhängigkeit mit dem Zustand eines Systems zu tun? da haperts bei mir noch.
Und nochmal danke für deine vorherige Erklärung. Dank dir habe ich den Zusammenhang zwischen innere Energie und Temperatur endlich verstanden. |
Wenn ich ein Gas mit 1bar 20°C auf 3bar 50°C erwärme, dann ist es für die innere Energie egal, ob ich zuerst erwärme und dann den Druck erhöhe oder umgekehrt. U(T=50°C, p=3bar) beschreibt den Zustand bei 50°C 3 bar und nicht wie man dorthin kommt.
_________________
Wenn du eine weise Antwort verlangst, musst du vernünftig fragen (Goethe) |
|
 |
frage1
Anmeldungsdatum: 20.02.2021
Beiträge: 569
Wohnort: bayern
|
 frage1 Verfasst am: 10. Dez 2021 19:11 Titel: frage1 Verfasst am: 10. Dez 2021 19:11 Titel: |
 |
|
|
Jetzt macht das ganze Sinn! Alles klar, vielen vielen Dank!!
|
|
 |
|
|