| Autor |
Nachricht |
MenschDerKeinenHutBesitzt
Anmeldungsdatum: 07.11.2018
Beiträge: 37
|
 MenschDerKeinenHutBesitzt Verfasst am: 08. Sep 2020 15:53 Titel: Gravitative Anziehung Proton-Elektron, Näherung sinnvoll MenschDerKeinenHutBesitzt Verfasst am: 08. Sep 2020 15:53 Titel: Gravitative Anziehung Proton-Elektron, Näherung sinnvoll |
 |
|
Hi, ich habe mich gefragt ob bspw. bei einem Wasserstoffatom das Newton'sche Gravitationsgesetz immernoch eine sinnvolle Nährung ist um die gravitative Anziehungskraft zwischen dem Proton und dem Elektron zu berechnen.
Ich beziehe mich auf das Bohr'sche Atommodell.
Meine Überlegungen bzw. Vermutungen:
a) Da die Distanz zwischen dem Proton und Elektron relativ zum jeweiligen Durchmesser sehr groß ist, kann mann beide Teilchen als Punktmassen betrachten, daran scheitert es nicht.
b) Elektronen sind sehr viel leichter als Protonen aber das sehe ich auch nicht als hinreichendes Problem an.
-------------
Welche Gründe sprechen gegen so eine Nährung?
_________________
Eventuell besitze ich demnächst einen Hut, dann ist mein Account-Name natürlich so lange unpassend bis ich den Hut verloren habe oder er mich. |
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 08. Sep 2020 16:48 Titel: TomS Verfasst am: 08. Sep 2020 16:48 Titel: |
 |
|
Also gegen das Bohrsche Atommodell spricht natürlich, dass es bekanntermaßen unzutreffend ist ;-)
Wenn es dir jedoch nur um die Gravitation geht - unter Vernachlässigung der Quantenmechanik - spricht wenig gegen die Näherung.
Es sind keine experimentellen Ergebnisse bzgl. Gravitation auf atomaren Skalen zugänglich oder bekannt, schlicht weil die Gravitation im Vergleich zur elektromagnetischen Wechselwirkung deutlich zu schwach ist, um separat messbare Effekte zu erhalten.
Kugelsymmetrische Massen können bzgl. der Gravitation exakt durch Punktmassen beschrieben werden.
Wir kennen die interne Ladungs- und Stromverteilung von Protonen sehr präzise aus Streuexperimenten.
http://www.scholarpedia.org/article/Nucleon_Form_factors
Daraus können wir theoretisch auf die Massenverteilung zurückschießen; Protonen hätten demnach zumindest ein Dipolmoment. Derartige Effekte - Punktmassen, kugelförmige Massenverteilungen, Dipolmomente, ... wären im Rahmen der Newtonschen Mechanik beschreibbar.
Aber natürlich ist erstens das Bohrsche Modell nicht zutreffend - s.o. - sowie die daraus resultierende Effekte deutlich schwächer als die elektromagnetischen und daher nicht experimentell messbar. Damit wären Abweichungen von der von dir genannten Näherung ebenfalls nicht nachprüfbar.
_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago.
Zuletzt bearbeitet von TomS am 08. Sep 2020 17:11, insgesamt einmal bearbeitet |
|
 |
MenschDerKeinenHutBesitzt
Anmeldungsdatum: 07.11.2018
Beiträge: 37
|
 MenschDerKeinenHutBesitzt Verfasst am: 08. Sep 2020 16:59 Titel: MenschDerKeinenHutBesitzt Verfasst am: 08. Sep 2020 16:59 Titel: |
 |
|
Sehr hilfreiche Antwort, vielen Dank :)
Ich kenne aktuell nur das Bohrsche Atommodell, auf welche besseren Modelle kann ich mich denn noch freuen, gibt es eines was besonders zum Verständnis beiträgt bzw. näher an der Realität ist?
Ich bin totaler Anfänger in dem Gebiet.
_________________
Eventuell besitze ich demnächst einen Hut, dann ist mein Account-Name natürlich so lange unpassend bis ich den Hut verloren habe oder er mich. |
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 08. Sep 2020 17:16 Titel: TomS Verfasst am: 08. Sep 2020 17:16 Titel: |
 |
|
| MenschDerKeinenHutBesitzt hat Folgendes geschrieben: | | Ich kenne aktuell nur das Bohrsche Atommodell, auf welche besseren Modelle kann ich mich denn noch freuen, gibt es eines was besonders zum Verständnis beiträgt bzw. näher an der Realität ist? |
1) Das Bohrsche Atommodell erklärt nicht die Stabilität von Atomen: auf Kreisbahnen bewegte Ladungen würden nach der Maxwellschen Theorie des Elektromagnetismus strahlen und innerhalb von Sekundenbruchteilen in den Kern stürzen.
2) Das Bohrsche Atommodell kann so zurechtgebastelt werden, dass es für das Wasserstoffatom in niedrigster Näherung funktioniert; es erklärt nicht die Intensität der Spektrallinien, es erklärt nicht erlaubte bzw. verbotenen Übergänge, nicht die Feinstruktur der Spektrallinien, keine komplexeren Atome mit mehreren Elektronen, ...
Daher muss man Atome definitiv quantenmechanisch beschreiben - die Mathematik dazu ist jedoch nicht mehr Schulniveau.
_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago. |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5740
|
 DrStupid Verfasst am: 08. Sep 2020 18:48 Titel: DrStupid Verfasst am: 08. Sep 2020 18:48 Titel: |
 |
|
| TomS hat Folgendes geschrieben: | | Wenn es dir jedoch nur um die Gravitation geht - unter Vernachlässigung der Quantenmechanik - spricht wenig gegen die Näherung. |
Zumindest meistens. Es gibt Fälle, in denen sich Elektronen mit relativistischen Geschwindigkeiten bewegen würden (z.B. im Quecksilber). Da funktioniert Newton auch nicht mehr. |
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 08. Sep 2020 21:12 Titel: TomS Verfasst am: 08. Sep 2020 21:12 Titel: |
 |
|
| DrStupid hat Folgendes geschrieben: | | Es gibt Fälle, in denen sich Elektronen mit relativistischen Geschwindigkeiten bewegen würden (z.B. im Quecksilber). Da funktioniert Newton auch nicht mehr. |
Da benutzen wir relativistische Quantenmechanik.
Im Sinne des Fragestellers müssten wir bei relativistischen Geschwindigkeiten und Berücksichtigung der Gravitation die allgemeine Relativitätstheorie anwenden.
Letzteres ist natürlich sinnlos.
@MenschDerKeinenHutBesitzt -
Berechne doch mal das Verhältnis der elektrischen
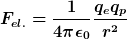
sowie der Gravitationskraft

zwischen Proton p und Elektron e.
_________________
Niels Bohr brainwashed a whole generation of theorists into thinking that the job (interpreting quantum theory) was done 50 years ago. |
|
 |
|
|















