| Autor |
Nachricht |
0302cherry
Anmeldungsdatum: 14.09.2015
Beiträge: 5
|
 0302cherry Verfasst am: 14. Sep 2015 16:49 Titel: Stickstoff erhitzen durch ein Rohr 0302cherry Verfasst am: 14. Sep 2015 16:49 Titel: Stickstoff erhitzen durch ein Rohr |
 |
|
Meine Frage:
Hallo Leute,
Durch ein Rohr mit 100 slm (standartliter/minute)soll Stickstoff von 20° auf 60° erhitzt werden und bei 5bar Überdruck.
Wie hoch ist die Heitzenergie die ich dafür brauche??
Ich hoffe ihr könnt mir auch hier helfen bitte.
Meine Ideen:
Kein Ansatz = keine Idee |
|
 |
magician4
Anmeldungsdatum: 03.06.2010
Beiträge: 914
|
 magician4 Verfasst am: 20. Sep 2015 15:39 Titel: magician4 Verfasst am: 20. Sep 2015 15:39 Titel: |
 |
|
die aufgabenstellung bleibt unklar insoweit, als nicht mitgeteilt wird ob "standardliter/min" als einstroemvolumen bei einstroemtemperatur oder als ausstroemvolumen bei ausstroemtemperatur zu verstehen sein soll
[denn das macht einen unterschied bzgl. der durchgesetzten stoffmenge, und dann eben euch energetisch]
ich entscheide mich daher willkuerlich fuer die betrachtung der ausstroembedingungen, und sodann:
ansatz:
wenn du davon ausgehst, dass das ganze bei konstantem druck stattfindet ( 5 bar überdruck = 6 bar absolut) , mithin die stroemungsgeschwinigkeit in richtung auf den ausstroempunkt hin zunimmt, dann kannst du die durchgesetzte stoffmenge/minute berechnen, weil dann in 1 minute eben

(gegeben: p = 6bar, V = 100 L , 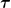 = 60°C : ich betrachte das ausstroemvolumenpro zeit, bei ausstroemtemperatur !) = 60°C : ich betrachte das ausstroemvolumenpro zeit, bei ausstroemtemperatur !)
(einheiten auf zueinander passende werte anpassen!)
mol stickstoff ausstroemen.
diese entsprechen aber eine masse von
})
gramm stickstoff, absolut
mit der spezifischen waermekapazitaet des stickstoffs bei konstantem druck

und dem geforderten 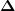 T = 40 K T = 40 K
kannst du daraus dann die benoetigte Heizenergie ( idealisiert: verlustfrei) pro 1 minute durchsatz ( und damit dann eben auch kontiniuierlier "pro minute") berechnen
gruss
Ingo |
|
 |
0302cherry
Anmeldungsdatum: 14.09.2015
Beiträge: 5
|
 0302cherry Verfasst am: 21. Sep 2015 08:54 Titel: 0302Cherry 0302cherry Verfasst am: 21. Sep 2015 08:54 Titel: 0302Cherry |
 |
|
Hey dein Ansatz ist vollkommen richtig nur verstehe ich das zwischestück nich welche masse Soll ich für M(n2) einsetzen
mol stickstoff ausstroemen.
diese entsprechen aber eine masse von
gramm stickstoff, absolut ?????
Der rest ist wieder klar |
|
 |
GvC
Anmeldungsdatum: 07.05.2009
Beiträge: 14861
|
 GvC Verfasst am: 21. Sep 2015 10:51 Titel: GvC Verfasst am: 21. Sep 2015 10:51 Titel: |
 |
|
|
Das ist doch nur die Umrechnung von mol in kg. Dabei ist n die Stoffmenge in mol und M die molare Masse in kg/mol (das was man früher als Molekulargewicht bezeichnet hat). |
|
 |
0302cherry
Anmeldungsdatum: 14.09.2015
Beiträge: 5
|
 0302cherry Verfasst am: 22. Sep 2015 11:22 Titel: 0302cherry 0302cherry Verfasst am: 22. Sep 2015 11:22 Titel: 0302cherry |
 |
|
Jia klar also manchmal da steh ich vollkommen aufm schlauch und physik bin ich mehr also ne 0 
ich komm am ende auf 0,0067 KW/h haut das hin ? oder habe ich da wo falsch umgerechnet?? 
zu meiner anderen frage was das Trimethylaluminum betrifft hab ihr da ne idee wo ich c her bekomme habe schon überall im netz geschaut aber nix gefunden
& Danke vielmals |
|
 |
magician4
Anmeldungsdatum: 03.06.2010
Beiträge: 914
|
 magician4 Verfasst am: 22. Sep 2015 22:16 Titel: magician4 Verfasst am: 22. Sep 2015 22:16 Titel: |
 |
|
| Zitat: | | zu meiner anderen frage was das Trimethylaluminum betrifft |
ich finde wieder hier, noch im gesamten forum* ) eine frage betreffend "trimethylaluminium" eine frage betreffend "trimethylaluminium"
| Zitat: | | hab ihr da ne idee wo ich c her bekomme habe schon überall im netz geschaut aber nix gefunden |
unglaublich...
du musst ein anderes internet haben als ich !
aber ich will da gern helfen: link
gruss
Ingo
*)
so zumindest die forum-stichwortsuche: da kommt nur genau dieser thread zurueck |
|
 |
0302cherry
Anmeldungsdatum: 14.09.2015
Beiträge: 5
|
|
 |
magician4
Anmeldungsdatum: 03.06.2010
Beiträge: 914
|
 magician4 Verfasst am: 24. Sep 2015 01:05 Titel: magician4 Verfasst am: 24. Sep 2015 01:05 Titel: |
 |
|
| Zitat: | | Ich glaub das ich jetzt alles habe und mit meinem angegeben Ergebnis is das nun richtig?! |
also, zunaechst einmal ist die einheit "kW/h" irgendwie recht exotisch: darueber solltest du nochmal nachdenken
(das ist weder eine absolute energie(menge), also irgendwas mit "joule" oder "kilowattstunden", wie der begriff "heizenergie" nahelegen wuerde, noch eine leistungsangabe [also J/sec oder watt, beispielsweise] - was meinem dafuerhalten nach eine natuerliche angabe zur aufgabenstellung waere: welche leistung muss ich anlegen, um den prozess kontinuierlich zu unterstuetzen? )
aber davon mal ab:
gegeben / literaturbekannt:
temperatur in °C  umrechnung auf K : 60°C = 333,15 K umrechnung auf K : 60°C = 333,15 K
druck in bar 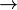 pascal (mithin N/m²) : 6 bar = 6*10^5 Pa pascal (mithin N/m²) : 6 bar = 6*10^5 Pa
volumen in L 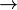 m³ : 100 L = 0.1 m³ m³ : 100 L = 0.1 m³
gaskonstante R : 8.314 J/molK
M(stickstoff) = 28,01 g/mol
somit:


um diese masse um 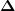 T = 40 K zu erwaermen benoetigst du T = 40 K zu erwaermen benoetigst du

... und zwar fuer jede betriebsminute (denn darauf hatte die betrachtung ja zunaechst abgestellt, auf den minutendurchsatz)
in einer stunde kommen so 1469,4 kJ zusammen oder  0.41 kWh , weshalb du eben dauerhaft eine elektrische heizleistung von 0.41 kW vorzusehen hast 0.41 kWh , weshalb du eben dauerhaft eine elektrische heizleistung von 0.41 kW vorzusehen hast
soderle, soweit dazu..
...und ansonsten, wegen des trimethylaluminiums: du benoetigst irgendwoher die spezifische waermekapazitaet des TMA (hersteller, sicherheitsdatenblatt sind gute quellen) , und dann gilt wieder E = c * m * 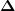 T T
 hinweis: das zeug ist nicht ohne im handling. u.a. hat es einen bemerkenswert hohen dampfdruck schon bei raumtemperatur, und ist ziemlich pyrophor hinweis: das zeug ist nicht ohne im handling. u.a. hat es einen bemerkenswert hohen dampfdruck schon bei raumtemperatur, und ist ziemlich pyrophor  sowas handhaben selbst gestandene chemiker mit professionellem respekt... sowas handhaben selbst gestandene chemiker mit professionellem respekt...
... und ich empfehle dir dringend , es uns da gleich zu tun.
 lass dich im handling durch entsprechend ausgebildete personen einweisen, und versuche nicht, das selbst-erfinderisch "irgendwie" hinzubekommen! arbeitstechnik unter schutzgas [Schlenk-technik o.ae. ] ist hier dringend angesagt! lass dich im handling durch entsprechend ausgebildete personen einweisen, und versuche nicht, das selbst-erfinderisch "irgendwie" hinzubekommen! arbeitstechnik unter schutzgas [Schlenk-technik o.ae. ] ist hier dringend angesagt!
gruss
Ingo |
|
 |
0302cherry
Anmeldungsdatum: 14.09.2015
Beiträge: 5
|
 0302cherry Verfasst am: 24. Sep 2015 14:03 Titel: 0302cherry 0302cherry Verfasst am: 24. Sep 2015 14:03 Titel: 0302cherry |
 |
|
Alles klar hab ich auch so noch mal nachgerechnet.
und wegen der TMAL geschicht weiß ich schon bescheid was das für ein zeug ist sobald es an die luft kommt fängt es an zu brennen
Aber mir ging es hier nur um die Berechnung en sonst nix weiter
Danke für die super Ausführlichen antworten
 |
|
 |
|



















