| Autor |
Nachricht |
Marleen
Anmeldungsdatum: 15.06.2006
Beiträge: 218
|
 Marleen Verfasst am: 27. Aug 2007 17:40 Titel: Adiabatischer Prozess: du = c_v * dT ??? Marleen Verfasst am: 27. Aug 2007 17:40 Titel: Adiabatischer Prozess: du = c_v * dT ??? |
 |
|
Hallo!
Ich habe vor mir den Beweis für  liegen. Woraus dann folgt: liegen. Woraus dann folgt: ^{k-1} = ( \frac{p_2 }{p_1 } )^{ \frac{k-1}{k} } )
Am Beginn des Beweises werden die Bedingungen gesetzt, die ich nicht verstehe.
Die Überschrift heißt "Adiabatischer Prozess/Formeln von Poisson"  , das verstehe ich. , das verstehe ich.
Dann geht es weiter mit:

Wieso ist hier  ? Für du gilt doch bei einem adiabatischen Prozess ? Für du gilt doch bei einem adiabatischen Prozess  . .
Im zweiten Schritt:
Allgemein gilt für Enthalpie  = du + pdv + vdp)


Wieso ist  ??? Gilt das nur bei adiabatischen Prozessen oder wann darf ich das annehmen? ??? Gilt das nur bei adiabatischen Prozessen oder wann darf ich das annehmen?
Der Vollständigerkeit schreibe ich noch den Beweis zu Ende, aber diesen Rest verstehe ich:




 } + \ln{ (v)^k } = \ln{ (Const. ) } )
 } = \ln{C} )

_________________
Info für die Helfenden:
Was ich lernen will:
http://tinyurl.com/yskhec
Was ich mathematisch drauf habe: http://www.matheboard.de/search.php?searchid=417662 |
|
 |
schnudl
Moderator

Anmeldungsdatum: 15.11.2005
Beiträge: 6979
Wohnort: Wien
|
 schnudl Verfasst am: 27. Aug 2007 20:13 Titel: Re: Adiabatischer Prozess: du = c_v * dT ??? schnudl Verfasst am: 27. Aug 2007 20:13 Titel: Re: Adiabatischer Prozess: du = c_v * dT ??? |
 |
|
| Marleen hat Folgendes geschrieben: |
Wieso ist  ??? Gilt das nur bei adiabatischen Prozessen oder wann darf ich das annehmen?[/b] ??? Gilt das nur bei adiabatischen Prozessen oder wann darf ich das annehmen?[/b] |
es ist immer bei allgemeiner Erwärmung

oder

Hält man während des Erwärmens p konstant (dp/dT = 0), dann ist

Gleichzeitig ist aber so cp definiert:

daher (bei isobaren Prozessen)

Aus dem gleichen Grund ist bei isochoren Prozessen

Vorsicht: dQ ist kein vollständiges Differential !
_________________
Wenn du eine weise Antwort verlangst, musst du vernünftig fragen (Goethe)
Zuletzt bearbeitet von schnudl am 27. Aug 2007 21:03, insgesamt 2-mal bearbeitet |
|
 |
Marleen
Anmeldungsdatum: 15.06.2006
Beiträge: 218
|
|
 |
schnudl
Moderator

Anmeldungsdatum: 15.11.2005
Beiträge: 6979
Wohnort: Wien
|
 schnudl Verfasst am: 27. Aug 2007 20:54 Titel: Re: Adiabatischer Prozess: du = c_v * dT ??? schnudl Verfasst am: 27. Aug 2007 20:54 Titel: Re: Adiabatischer Prozess: du = c_v * dT ??? |
 |
|
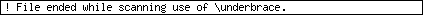 _{ V} }_{C_V} dT + \left( \frac{\partial U}{\partial V}\right)_{ T} dV)
Nun ist aber beim idealen Gas der zweite Term Null, da U(T, V) = U(T)
_{ T} = 0 )
Deshalb gilt für das ideale Gas
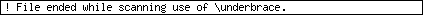 _{ V} }_{C_V} dT = c_V dT)
_________________
Wenn du eine weise Antwort verlangst, musst du vernünftig fragen (Goethe)
Zuletzt bearbeitet von schnudl am 27. Aug 2007 23:11, insgesamt einmal bearbeitet |
|
 |
Marleen
Anmeldungsdatum: 15.06.2006
Beiträge: 218
|
 Marleen Verfasst am: 27. Aug 2007 21:18 Titel: Re: Adiabatischer Prozess: du = c_v * dT ??? Marleen Verfasst am: 27. Aug 2007 21:18 Titel: Re: Adiabatischer Prozess: du = c_v * dT ??? |
 |
|
| Marleen hat Folgendes geschrieben: |

|
Ich darf also die Gleichung  nur bei isochorem Prozess anwenden. Bei isochoren Prozess gilt doch nur bei isochorem Prozess anwenden. Bei isochoren Prozess gilt doch  . In der zitierten Gleichung steht aber: . In der zitierten Gleichung steht aber:

Warum nicht  ? ?
_________________
Info für die Helfenden:
Was ich lernen will:
http://tinyurl.com/yskhec
Was ich mathematisch drauf habe: http://www.matheboard.de/search.php?searchid=417662 |
|
 |
magneto42
Anmeldungsdatum: 24.06.2007
Beiträge: 854
|
|
 |
Marleen
Anmeldungsdatum: 15.06.2006
Beiträge: 218
|
 Marleen Verfasst am: 27. Aug 2007 22:05 Titel: Marleen Verfasst am: 27. Aug 2007 22:05 Titel: |
 |
|
hmm, und hier habe ich einen Musterlösungsweg von unserem Dozenten, wo  verwendet wird, obwohl es sich um keinen isochoren Prozess handelt: verwendet wird, obwohl es sich um keinen isochoren Prozess handelt:
"Luftreservoir mit 3m³ hat einen Druck von 5,4bar (absolut) und eine Temperatur von 45°C. Die Wärmekapazität von Luft ist ) und k=1,4. Wenn diese Luft in in anderes Reservoir gehen kan mit 10m³, dann bekommen wir einen Druck von 1,5 bar (absolut). und k=1,4. Wenn diese Luft in in anderes Reservoir gehen kan mit 10m³, dann bekommen wir einen Druck von 1,5 bar (absolut).
Gefragt wird:
1. Der Polytropenexponent n.
2. Die Endtemperatur in K und C.
3. Die verrichtete Arbeit per kg und in total.
4. Die aufgenommene Wärme
5. Die innere Energie."
Ich schreibe mal nur die Musterlösungen Teilaufgaben 1, 2 und 5 auf.
1)
^{n} = \frac{ p_2 }{ p_1 } \Rightarrow n = \frac{ \ln{ \frac{1.5}{5.4} } }{ \ln{ \frac{3}{10} } } = 1.064 )
2)
^{n-1} = (45K+273K) ( \frac{3}{10} )^{1.064-1} = 294K = 21°C )
5)
 = 0.716 kJ/(kg \cdot K) \cdot (294K-318K) = -17.18 kJ/kg)
Obwohl es sich um keinen isochoren Prozess handelt, wird hier trotzdem die Gleichung  zur Hilfe genommen. Das Ergebnis stimmt aber, wenn ich die innere Engergie so berechne zur Hilfe genommen. Das Ergebnis stimmt aber, wenn ich die innere Engergie so berechne  Aber wieso? Aber wieso?  [/latex] [/latex]
_________________
Info für die Helfenden:
Was ich lernen will:
http://tinyurl.com/yskhec
Was ich mathematisch drauf habe: http://www.matheboard.de/search.php?searchid=417662 |
|
 |
schnudl
Moderator

Anmeldungsdatum: 15.11.2005
Beiträge: 6979
Wohnort: Wien
|
 schnudl Verfasst am: 27. Aug 2007 23:12 Titel: schnudl Verfasst am: 27. Aug 2007 23:12 Titel: |
 |
|
Die Beantwortung deiner Frage ist in der speziellen Zustandsgleichung idealer Gase begründet. Allgemein ist
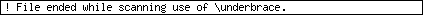 _{ V} }_{C_V} dT + \left( \frac{\partial U}{\partial V}\right)_{ T} dV)
Nun ist aber beim idealen Gas der zweite Term Null, da U(T, V) = U(T)
_{ T} = 0 )
Deshalb gilt für das ideale Gas
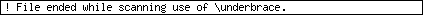 _{ V} }_{C_V} dT = c_V dT)
Allgemein gilt dies nur für dV = 0, also isochore Zustandsänderungen !
Ebenso ist H(T, P) = H(T) und es gilt für das ideale Gas
 _{ p} }_{C_p} dT = c_p dT)
Ansonsten eben nur für isobare Zustandsänderungen, da allgemein
_{T} \ne 0)
_________________
Wenn du eine weise Antwort verlangst, musst du vernünftig fragen (Goethe) |
|
 |
Marleen
Anmeldungsdatum: 15.06.2006
Beiträge: 218
|
 Marleen Verfasst am: 28. Aug 2007 04:04 Titel: Marleen Verfasst am: 28. Aug 2007 04:04 Titel: |
 |
|
Ich glaube wir reden jetzt aneinander vorbei. Deine mathematischen Ausführungen verstehe ich. Ich habe aber eine Aufgabe mit Musterrechenweg gesehen. Der Prozess in der Aufgabe ist nicht isochor und nicht isobar. Trotzdem wird die Formel  zum Schluss verwendet, die nur bei einem isochorem Prozess verwendet werden darf. zum Schluss verwendet, die nur bei einem isochorem Prozess verwendet werden darf.
_________________
Info für die Helfenden:
Was ich lernen will:
http://tinyurl.com/yskhec
Was ich mathematisch drauf habe: http://www.matheboard.de/search.php?searchid=417662 |
|
 |
schnudl
Moderator

Anmeldungsdatum: 15.11.2005
Beiträge: 6979
Wohnort: Wien
|
 schnudl Verfasst am: 28. Aug 2007 07:41 Titel: schnudl Verfasst am: 28. Aug 2007 07:41 Titel: |
 |
|
| Marleen hat Folgendes geschrieben: | Ich glaube wir reden jetzt aneinander vorbei. Deine mathematischen Ausführungen verstehe ich. Ich habe aber eine Aufgabe mit Musterrechenweg gesehen. Der Prozess in der Aufgabe ist nicht isochor und nicht isobar. Trotzdem wird die Formel  zum Schluss verwendet, die nur bei einem isochorem Prozess verwendet werden darf (oder eben ... siehe unten). zum Schluss verwendet, die nur bei einem isochorem Prozess verwendet werden darf (oder eben ... siehe unten). |
Aneinander vorbeireden ist immer leicht möglich, aber ich bin mir fast sicher, dass du oben nicht genau gelesen hast:
 gilt entweder wenn dV=0 (isochor) oder wenn U nicht von V abhängt, da dann (U ist ja immer ein vollständiges Differential in seinen Zustandsvariablen) gilt entweder wenn dV=0 (isochor) oder wenn U nicht von V abhängt, da dann (U ist ja immer ein vollständiges Differential in seinen Zustandsvariablen)
_V }_{= c_v} dT + \underbrace{ \left( \frac{\partial U}{\partial V} \right)_T }_{= 0}dV = c_v dT)
Wenn du in einer Musterlösung also  bei nicht isochorem Prozess siehst, dann kann das nur für ein System gelten, wo eben U(T,V) = U(T) ist, wie z.B. für das ideale Gas (siehe dein Luft Beispiel oben). Allgemein stimmt die Beziehung aber sicher nicht ! bei nicht isochorem Prozess siehst, dann kann das nur für ein System gelten, wo eben U(T,V) = U(T) ist, wie z.B. für das ideale Gas (siehe dein Luft Beispiel oben). Allgemein stimmt die Beziehung aber sicher nicht !
_________________
Wenn du eine weise Antwort verlangst, musst du vernünftig fragen (Goethe) |
|
 |
|
















 [/latex]
[/latex]