| Autor |
Nachricht |
Rebe92
Gast
|
 Rebe92 Verfasst am: 26. Jun 2017 20:18 Titel: Berechnung der Ionisierungsenergie eine He+ Atoms?w Rebe92 Verfasst am: 26. Jun 2017 20:18 Titel: Berechnung der Ionisierungsenergie eine He+ Atoms?w |
 |
|
Folgende Aufgabe wurde uns gegeben:
a) Bestimmen Sie die Ionisierungsenergie eines angeregten He+-Ions, bei dem sich das Elektron in einem Orbital befindet, welches durch die Einelektronwellenfunktion ψ4,2,1 beschrieben wird.
b) Bestimmen Sie die Ionisierungsenergie eines angeregten Li2+-Ions, bei dem sich das Elektron in einem Orbital befindet, welches durch die Einelektronwellenfunktion ψ4,2,1 beschrieben wird.
Nun habe ich leider keine Ahnung welche Formel ich anwenden muss.
In Quantenphysik bin ich einfach eine totale Niete, leider.
Muss dazu aber sagen das ich Biochemie studiere und ich Quantenphysik garnicht verstehen will weil es für uns nicht wichtig ist aber halt trotzdem ein Modul ist was wir brauchen.
Unser Dozent ist leider auch einfach eine Flasche und nutzt Folien und Skripte die extrem unübersichtlich sind. Teilweise sind Fehler drin. Bei Formeln schreibt er nicht dazu was die Variablen sind sodass man sich diese ergooglen muss.
Kann mir bitte jemand helfen und ganz simpel erklären wie man die Ionisierungsenergie berechnet ohne viel Vorwissen und Kentnisse? Und vorallem eine eindeutige Formel zeigen mit der das geht?
Ich wäre so dermaßen dankbar. |
|
 |
Neutrinowind
Anmeldungsdatum: 01.04.2017
Beiträge: 29
|
 Neutrinowind Verfasst am: 26. Jun 2017 22:06 Titel: Re: Berechnung der Ionisierungsenergie eine He+ Atoms?w Neutrinowind Verfasst am: 26. Jun 2017 22:06 Titel: Re: Berechnung der Ionisierungsenergie eine He+ Atoms?w |
 |
|
Die Ionisierungsenergie ist die Energie, die du brauchst, um das Elektron aus dem Ion zu lösen.
Da bei den besagten Ionen sich nur ein Elektron in der Atomhülle befindet, kannst du die Formeln für das Wasserstoffatom anwenden, wobei du allgemein eine Kernladung Z hast.
Damit solltest du alles haben, um die Aufgabe zu lösen.
| Rebe92 hat Folgendes geschrieben: |
In Quantenphysik bin ich einfach eine totale Niete, leider.
Muss dazu aber sagen das ich Biochemie studiere und ich Quantenphysik garnicht verstehen will weil es für uns nicht wichtig ist aber halt trotzdem ein Modul ist was wir brauchen.
|
Das ist keine gute Voraussetzung. Du solltest etwas an deiner Einstellung ändern.
Woher willst du wissen, dass Quantenmechanik in der Biochemie nicht wichtig ist, wenn du sie noch nicht verstanden hast? |
|
 |
Rebe92
Gast
|
 Rebe92 Verfasst am: 26. Jun 2017 22:26 Titel: Rebe92 Verfasst am: 26. Jun 2017 22:26 Titel: |
 |
|
Weil es keiner verstanden hat. Niemand den ich kenne zumindest. Jeder will nur bestehen, also durch stumpfes einsetzen der gegebenen Werte etc.
Sowas kann man verstehen, aber die Quantenmechanik und die Schrödingergleichung usw. verstehen tut niemand..
Und ich weiß nicht wie ich sie verstehen soll da, wie ich schon sagte, unser Dozent nichts taugt. Er versteht es nämlich selbst nicht richtig, zudem macht er Fehler in seinem Skript.
Kannst du mir eine Formel für die Berechnung angeben? Und erklären? Anschaulich oder zumindest simpel, wieso weshalb warum das da eingesetzt werden kann.
Es würde mir sehr helfen... bin ja bereit etwas zu tun, hab mich ja schon mit dem Skript auseinandergesetzt.. aber es ist so durcheinander und für jemanden der noch nie was mit der Schrödingergleichung oder Berechnung von elektronenVolt von Lichtquanten etc. getan hat ist es einfach nicht verständlich. Deshalb von 0. Und dann will ich mich langsam durch Skript arbeiten. Aber das Skript selbst ist einfach ne Zumutung für mich/uns.
Ich wills ja verstehen aber so wird das vorerst nichts...
Verstehst du?
Ich kann nicht einfach direkt in soetwas einsteigen wenn mein Vorwissen nicht ausreicht um die Grundprinzipien der Quantenphysik zu verstehen.. |
|
 |
Rebe92
Gast
|
 Rebe92 Verfasst am: 26. Jun 2017 22:27 Titel: Rebe92 Verfasst am: 26. Jun 2017 22:27 Titel: |
 |
|
|
Z.B. verstehe ich nicht was es mit ψ4,2,1 auf sich hat und inwiefern das eine Rolle spielt. |
|
 |
TomS
Moderator

Anmeldungsdatum: 20.03.2009
Beiträge: 21442
|
 TomS Verfasst am: 27. Jun 2017 07:14 Titel: TomS Verfasst am: 27. Jun 2017 07:14 Titel: |
 |
|
Mit
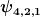
ist vermutlich der Zustand

gemeint.
Zu berechnen ist dann zunächst die Energie dieses Zustandes

Die Ionisierungsenergie ist die Energie, die aufgebracht werden muss, um das Elektron von diesem Zustand in den untersten ungebundenen Zustand zu bringen (das wäre für n gegen Unendlich die Energie Null). Die Ionisierungsenergie ist also gerade

Ich hoffe, ihr kennt die Formel für die Energieniveaus in wasserstoffartigen Ionen mit einem Elektron sowie Kernladungszahl Z. |
|
 |
Rebe92
Gast
|
 Rebe92 Verfasst am: 02. Jul 2017 11:52 Titel: Rebe92 Verfasst am: 02. Jul 2017 11:52 Titel: |
 |
|
Ja kennen wir, danke für die Hilfe, hat mir schon geholfen.
Vielleicht noch ne Frage anbei:
Wie sieht die Lösung der Schrödingergleichung aus?
Die Frage stellt sich mir wegen folgendem:
Wenn wir ein komplizierteres Atom haben als ein Wasserstoffatom, dann haben wir ja einen Raum um den Kern welcher mit der Wahrscheinlichkeit der Präsenz des Elektrons gefüllt ist. Am Kern selbst beträgt diese Wahrscheinlichkeit 0, allerdings je weiter man weggeht desto höher ist die Chancen und irgendwann fällt sie wieder ab. Nun haben wir haben aber z.B. ein Bor-Atom welche ein Elektron in der p-Schale hat. Die p-Schale selbst ist aber nicht rund sondenr hantelförmig? Wie beschreibt man nun die Wahrscheinlichkeit? Immerhin ist es ja abhängig davon wo es sich befindet?
Oder um es anders zu erklären:
Wie sieht die Gleichung der Schrödingergleichung aus wenn sie gelöst ist? Wahrscheinlichkeit kann man als Zahl ohne Einheit schreiben, aber man braucht doch 2 Werte? Einmal für die Entfernung, einmal für die Wahrscheinlichkeit?
Sagen wir, wir geben den Radius in die Schrödingergleichung ein, nun haben wir einen bestimmten Wert den wir rausbekommen welcher die Wahrscheinlichkeit angibt? Verstehe ich das so richtig?
Ich verstehe halt einfach nicht richtig wie man aus dieser komischen Formel mit 4 Zeichen einen Wert für eine Wahrscheinlichkeit erhält und inwiefern die imaginäre Zahl eine Rolle spielt.
Bekommt man eine implizite oder explizite Lösung welche ganz klar sagt wie groß die Wahrscheinlichkeit ist?
Und wie gibt man die 3 Raumkoordinaten an bei einem hantelförmigen Orbital, z.B. wenn das Elektron ionisiert wird und auf die p-Schale springt? |
|
 |
|
|















