| Autor |
Nachricht |
Gast
Gast
|
 Gast Verfasst am: 18. Apr 2005 15:28 Titel: Bohrsches Atommodell Gast Verfasst am: 18. Apr 2005 15:28 Titel: Bohrsches Atommodell |
 |
|
Hallo,
ich habe folgende Probleme beim Verständnis rund um das Bohrsche Atommodell:
Hertz-Versuch
Das Versuchsergebnis ist ja dieses Spannungs-Stromdiagramm mit den "Maxima" bei k*4,9V.
Uns wurde nun gesagt, daß ein Elektron welches (z.B.) durch 9,8V beschleunigt wurde in der Lage ist, 2 Stöße mit Teilchen des Quecksilberdampfes zu vollführen und dabei jeweils ein Valenzelektron in den 1. Anregungszustand zu versetzen.
Soweit, sogut. Warum aber versetzt dieses beschleunigte Elektron nicht ein Valenzelektron des Quecksilberdampfes in den 2. angeregten Zustand? Ist das generell nicht möglich?
elastische Stöße
Uns wurde gesagt, daß ein beschleunigtes Elektron welches mit einem anderen Valenzelektron zusammenstößt, das Valenzelektron auf das nächsthöhere Energieniveau anhebt und mit der verbleibenden Energie weiterfliegt.
Warum ist das so? Also warum gibt das beschleunigte Elektron genau diese benötigte Energie ab und fliegt dann weiter? Warum gibt es nicht seine gesamte Energie ab und das gestoßene Valenzelektron, welches nun ein Stück über das nächste Energieniveau hinausgestoßen wurde, gibt seinerseits die "überflüssige" Energie ab um auf das "gewünschte" Energieniveau zu kommen?
Und die letzte Frage:
Weshalb müssen Photonen eine bestimmte Energie besitzen um Elektronen anregen zu können? Warum klappt das nicht wenn sie zu viel Energie besitzen?
Danke. |
|
 |
Lucky

Anmeldungsdatum: 11.04.2005
Beiträge: 41
|
 Lucky Verfasst am: 18. Apr 2005 18:59 Titel: Lucky Verfasst am: 18. Apr 2005 18:59 Titel: |
 |
|
Ich beantworte mal die letzte Frage:
Photonen mit sehr hoher Energie sorgen dafür, dass das Elektron quasi auf die "unendliche" bahn des Atoms angeregt werden, ergo aus dem atomaren Verbund herausgelöst werden. Den Vorgang nennt man dann Ionisierung. Die Energie, die zur Ionisierung aufgebracht werden muss setzt sich zusammen durch ) , wobei n1 der derzeitige Zustand des Elektrons ist (z.b. 1) und n2 -> unendlich läuft...also, der Term wegfällt. , wobei n1 der derzeitige Zustand des Elektrons ist (z.b. 1) und n2 -> unendlich läuft...also, der Term wegfällt.
Nun lassen sich Wellenlänge und somit die Energie berechnen.
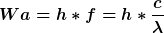 (Wa = Austrittsarbeit) (Wa = Austrittsarbeit)

achja...und die restliche Energie (überschüssige Energie) wird dann in kinetische Energie des Elektrons umgewandelt und ist relevant für die Geschwindigkeit, mit der das Elektron sich nach der Ionisierung weiterbewegt.
Das heißt:
Ekin = kinetische Energie des Elektrons nach Ionisierung
Eph = Die Energie des Photons (hochenergetisch!)
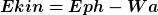
EDIT:
Achja...und Elektronen brauchen eine bestimmte Mindestenergie um überhaupt angeregt zu werden. Das liegt an der Quantelung der Energiebeträge bei einem Atom. Die Formel für die Energiebeträge habe ich oben bereits erwähnt! Die Formel müsste dir geläufig sein, oder? |
|
 |
Gast
Gast
|
 Gast Verfasst am: 18. Apr 2005 19:57 Titel: Gast Verfasst am: 18. Apr 2005 19:57 Titel: |
 |
|
Erstmal danke für die Antwort.
Die ionisierung ist mir schon geläufig. Was mir rein vom Verständnis her Schwierigkeiten bereitet ist folgendes: Nehmen wir z.B. mal Wasserstoff her, dessen Elektron sich im Grundzustand befindet. Um dieses Elektron nun auf das 2. Energieniveau anzuheben muß ich 10,2eV aufbringen. Soll das per Bestrahlung mit Photonen geschehen, so müssen die Photonen ja genau eine Frequenz von 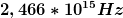 haben. haben.
Ich frage mich nun, weshalb überhaupt nichts passiert, wenn ich Photonen mit sagen wir 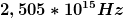 auf das Wasserstoffatom loslasse (entspräche rechnerisch dem 4,2ten Energieniveau). Also warum lassen Photonen mit "falschen" Energiewerten die Elektronen völlig kalt und geben nicht einen Teil ihrer Energie an das Elektron ab? auf das Wasserstoffatom loslasse (entspräche rechnerisch dem 4,2ten Energieniveau). Also warum lassen Photonen mit "falschen" Energiewerten die Elektronen völlig kalt und geben nicht einen Teil ihrer Energie an das Elektron ab?
Hoffe ich stehe nicht total auf der Leitung - aber ich verstehs einfach nicht  |
|
 |
|
|
















