| Autor |
Nachricht |
Romeo

Anmeldungsdatum: 27.02.2008
Beiträge: 148
|
 Romeo Verfasst am: 02. Okt 2008 12:52 Titel: Besetzungen für Halbleiter/Leiter Romeo Verfasst am: 02. Okt 2008 12:52 Titel: Besetzungen für Halbleiter/Leiter |
 |
|
Hi,
ich hab ein paar Fragen zu folgender Aufgabe, irgndwie werde ich da nicht schlau raus, ich hab zwar mehr oder weniger die Lösungen dazu, versteh aber nicht wieso einige Werte benutzt wurden.
 http://img361.imageshack.us/img361/6878/besetzungzq2.jpg http://img361.imageshack.us/img361/6878/besetzungzq2.jpg
Beispielsweise würde ich bei Aufgabenteil a.) wegen des fcc-Gittertypes (4 Gitterpunkte) N=4 setzen und mein Volumen wäre Gitterkonstante hoch 3. Was aber anscheinand nicht das korrekte Ergebnis liefert, aber wieso? In meiner Lösung steht, dass ich N=(0,01m)^3 wähle, verstehe aber nicht warum.
Zu Aufgabenteil b.) würde ich folgende Formel benutzen, ist das ok? Mit T=0K wird ja sicher die Fermi-Energie gemeint sein.
^{\frac{2}{3}})
Hier würde ich den Wert (aus a.)) für n=N/V einsetzen.
Dann mir da jemand vielleicht weiterhelfen?
_________________
Grüße Romeo |
|
 |
wishmoep
Anmeldungsdatum: 07.09.2008
Beiträge: 1342
Wohnort: Düren, NRW
|
 wishmoep Verfasst am: 02. Okt 2008 13:10 Titel: Re: Besetzungen für Halbleiter/Leiter wishmoep Verfasst am: 02. Okt 2008 13:10 Titel: Re: Besetzungen für Halbleiter/Leiter |
 |
|
| Romeo hat Folgendes geschrieben: | | a.) wegen des fcc-Gittertypes (4 Gitterpunkte) N=4 setzen und mein Volumen wäre Gitterkonstante hoch 3. Was aber anscheinand nicht das korrekte Ergebnis liefert, aber wieso? In meiner Lösung steht, dass ich N=(0,01m)^3 wähle, verstehe aber nicht warum. |
Wenn du die Gitterkonstante hoch 3 nehmen würdest, hättest du etwas wie  - kein Volumen, oder? - kein Volumen, oder?
Zumal die Gitterkonstante doch in Metern angegeben wird.  
Vielleicht könnte man die Zahl der Atome pro Elementarzelle mit  berechnen? berechnen? |
|
 |
Romeo

Anmeldungsdatum: 27.02.2008
Beiträge: 148
|
 Romeo Verfasst am: 02. Okt 2008 14:12 Titel: Re: Besetzungen für Halbleiter/Leiter Romeo Verfasst am: 02. Okt 2008 14:12 Titel: Re: Besetzungen für Halbleiter/Leiter |
 |
|
| wishmoep hat Folgendes geschrieben: | Wenn du die Gitterkonstante hoch 3 nehmen würdest, hättest du etwas wie  - kein Volumen, oder? - kein Volumen, oder?
Zumal die Gitterkonstante doch in Metern angegeben wird.  
|
Dachte A steht für Ångström und damit ist die Einheit gemeint, Umrechungsfaktor: 1A = 10^-10m
Ich denke schon, dass es als Volumen gemeint ist.
_________________
Grüße Romeo |
|
 |
wishmoep
Anmeldungsdatum: 07.09.2008
Beiträge: 1342
Wohnort: Düren, NRW
|
 wishmoep Verfasst am: 02. Okt 2008 14:17 Titel: wishmoep Verfasst am: 02. Okt 2008 14:17 Titel: |
 |
|
|
Ah - ja. Für den Fall stimme ich dir zu. Wie steht es denn mit der von mir eben geposteten Formel? |
|
 |
Romeo

Anmeldungsdatum: 27.02.2008
Beiträge: 148
|
 Romeo Verfasst am: 02. Okt 2008 14:32 Titel: Romeo Verfasst am: 02. Okt 2008 14:32 Titel: |
 |
|
Also mit der von dir geposteten Formel, falls ich sie richtig interpretiere, kommt auch nicht das Ergebnis auf meinem Lösungszettel raus (ich bin ja der Meinung, der Lösungzettel ist falsch  ). ).
u - atomare Masse
 - relative Masse (oder ist damit die Ruhemasse gemeint?) - relative Masse (oder ist damit die Ruhemasse gemeint?)
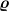 - Dichte - Dichte
Welchen Wert bekommst du für die Atomdichte heraus?
_________________
Grüße Romeo |
|
 |
wishmoep
Anmeldungsdatum: 07.09.2008
Beiträge: 1342
Wohnort: Düren, NRW
|
 wishmoep Verfasst am: 02. Okt 2008 14:41 Titel: wishmoep Verfasst am: 02. Okt 2008 14:41 Titel: |
 |
|
| Romeo hat Folgendes geschrieben: | (ich bin ja der Meinung, der Lösungzettel ist falsch  ). ). |
Das sind sie meistens :-D. Ich mache mir immer Sorgen, wenn ich das gleiche Ergebnis wie in den Lösungen angegeben raus habe... dann muss iwo ein Fehler sein.
| Romeo hat Folgendes geschrieben: | | Welchen Wert bekommst du für die Atomdichte heraus? |
Die Interpretation ist schon richtig, ich denke als Dichte kann man die effektive Masse pro Gitterkonstantenkubus nehmen.

Bei 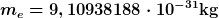 und und 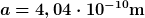 |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 02. Okt 2008 16:15 Titel: dermarkus Verfasst am: 02. Okt 2008 16:15 Titel: |
 |
|
| wishmoep hat Folgendes geschrieben: | ich denke als Dichte kann man die effektive Masse pro Gitterkonstantenkubus nehmen.
|
Ui  , entschuldige den Schuss vor den Bug, wishmoep, aber bei dieser Aufgabe scheinst du mir ein bisschen arg ins blaue hinein zu spekulieren, ohne zu wissen, was mit den Worten der Aufgabenstellung gemeint ist. , entschuldige den Schuss vor den Bug, wishmoep, aber bei dieser Aufgabe scheinst du mir ein bisschen arg ins blaue hinein zu spekulieren, ohne zu wissen, was mit den Worten der Aufgabenstellung gemeint ist.
Die effektive Masse in der Aufgabenstellung ist die effektive Masse eines Elektrons im Potential des Kristallgitters. Mit der Berechnung der Dichte unseres Aluminiumkristalls hat sie nichts zu tun.
Die Zellendichte des Aluminiumkristalls kann man berechnen als
Zellendichte = 1/(Volumen einer Elementarzelle)
und die Atomdichte des Aluminiumkristalls kann man berechnen als
Atomdichte = Zellendichte * (Anzahl von Aluminiumatomen pro Basis des kubisch raumzentrierten Kistallgitters)
Die Massendichte des Aluminiumkristalls
Massendichte = (Anzahl der Aluminiumatome pro Basis des kubisch flächenzentrierten Kristallgitters) mal (Masse eines Aluminiumatoms) pro (Volumen einer Elementarzelle des fcc-Kristallgitters)
braucht man in dieser Aufgabe nicht zu berechnen. |
|
 |
Romeo

Anmeldungsdatum: 27.02.2008
Beiträge: 148
|
 Romeo Verfasst am: 02. Okt 2008 16:44 Titel: Romeo Verfasst am: 02. Okt 2008 16:44 Titel: |
 |
|
| dermarkus hat Folgendes geschrieben: |
Die Zellendichte des Aluminiumkristalls kann man berechnen als
Zellendichte = 1/(Volumen einer Elementarzelle)
und die Atomdichte des Aluminiumkristalls kann man berechnen als
Atomdichte = Zellendichte * (Anzahl von Aluminiumatomen pro Basis des kubisch raumzentrierten Kistallgitters)
|
Also hab ich es doch richtig bedacht?
^3} = 6.066188 \cdot 10^{28})
Wieso kommen in die auf meinem Lösungzettel auf das:
^3}{(4,04 A)^3})
_________________
Grüße Romeo |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 02. Okt 2008 17:11 Titel: dermarkus Verfasst am: 02. Okt 2008 17:11 Titel: |
 |
|
| Romeo hat Folgendes geschrieben: |
Also hab ich es doch richtig bedacht?
^3} = 6.066188 \cdot 10^{28})
|
Ja. Aber da fehlt noch die Einheit. In welcher Einheit hast du die Atomdichte ausgerechnet?
| Zitat: |
Wieso kommen in die auf meinem Lösungzettel auf das:
^3}{(4,04 \, \rm A)^3})
|
2 Fragen an dich: Was meinst du:
* Was bezeichnet dein Lösungszettel mit dem Buchstaben n? Die Zellendichte oder die Atomdichte?
* In welcher Einheit hat dein Lösungszettel diese Dichte ausgerechnet? |
|
 |
Romeo

Anmeldungsdatum: 27.02.2008
Beiträge: 148
|
 Romeo Verfasst am: 02. Okt 2008 18:28 Titel: Romeo Verfasst am: 02. Okt 2008 18:28 Titel: |
 |
|
^3} = 6.066188 \cdot 10^{28} \frac{1}{m^3})
Da bin ich echt froh, dass es doch korrekt ist... Danke!
Naja Lösungszettel. Also ich hatte diese Aufgabe mal in einen meiner Physikübungszettel, die bei uns nach der Bearbeitung von den ensprechneden Tutoren korrigiert werden, ist ja meistens so üblich. Tja und mein Tutor ist wohl der Meinung, dass in den Zähler des Bruches (0,01m)^3 gehört und die Atomdichte damit Einheitenlos ist. Wobei ich mir die 0,01m auch nie erklären konnte und das hoch drei sowieso nicht.
Aber egal, jetzt weiß ich es besser, ist ja so auch viel logischer! 
_________________
Grüße Romeo |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 02. Okt 2008 22:03 Titel: dermarkus Verfasst am: 02. Okt 2008 22:03 Titel: |
 |
|
| Romeo hat Folgendes geschrieben: | ^3} = 6.066188 \cdot 10^{28} \frac{1}{m^3})
Da bin ich echt froh, dass es doch korrekt ist... Danke!
|
Mit diesem Ergebnis bin ich zwar einverstanden, weil es eine der Antworten auf die Fragen in a) ist, aber was du da ausgerechnet hast, ist nicht das, was die Aufgabenstellung als n= N/V bezeichnet hat.
Die zwei Fragen zum Lösungszettel hast du bisher noch nicht beantwortet.
Mit dem Ergebnis des Lösungszettels bin ich einverstanden.
Denn erstens meint dieses Ergebnis die Zellendichte (nach der ist in der Aufgabe auch gefragt !),
und zweitens ist das Ergebnis der Zahlenwert der Zellendichte in der Einheit "Elementarzellen pro cm^3".
(Die Einheit "pro cm^3" würde ich in diesem Zusammenhang als deutlich üblicher empfinden als die Einheit "pro m^3".) |
|
 |
Romeo

Anmeldungsdatum: 27.02.2008
Beiträge: 148
|
 Romeo Verfasst am: 02. Okt 2008 23:06 Titel: Romeo Verfasst am: 02. Okt 2008 23:06 Titel: |
 |
|
Mh, tschuldigung, dann hatte ich es wohl noch nicht richtig verstanden.
Zellendichte:
^3} = 24752475,25 \frac{1}{cm^3} )
Atomdichte:

Faktor 4 wegen des fcc-Gittertypes
Auf dem Lösungszettel steht:
^3 = 1,516547 \cdot 10^{22})
Das du mir bitte sagen, wie ich es zuordnen muss und wo der Zusammenhang zum Ergebnis des Lösungszettels ist?!
_________________
Grüße Romeo |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 03. Okt 2008 00:39 Titel: dermarkus Verfasst am: 03. Okt 2008 00:39 Titel: |
 |
|
| Romeo hat Folgendes geschrieben: |
Zellendichte:
^3} = 24752475,25 \frac{1}{cm^3} )
|
Vorsicht, da hast du dich glaube ich einfach nur beim Ergebnis im Taschenrechner vertippt.
| Zitat: |
Atomdichte:

Faktor 4 wegen des fcc-Gittertypes
|
Hoppla, da hast du dich beim Umrechnen von 1/m^3 in 1/cm^3 grob in der Zehnerpotenz vertan. Hast du vielleicht vergessen, dass es Kubik... sind und nicht einfach nur m und cm? |
|
 |
Romeo

Anmeldungsdatum: 27.02.2008
Beiträge: 148
|
 Romeo Verfasst am: 03. Okt 2008 01:51 Titel: Romeo Verfasst am: 03. Okt 2008 01:51 Titel: |
 |
|
Ja - du hast vollkommen recht. Es ist spät und die Konzentration lässt deutlich nach...
Zellendichte:

Atomdichte:
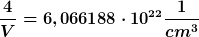
_________________
Grüße Romeo |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 03. Okt 2008 02:00 Titel: dermarkus Verfasst am: 03. Okt 2008 02:00 Titel: |
 |
|
Einverstanden  |
|
 |
|


















 ).
).
 , entschuldige den Schuss vor den Bug, wishmoep, aber bei dieser Aufgabe scheinst du mir ein bisschen arg ins blaue hinein zu spekulieren, ohne zu wissen, was mit den Worten der Aufgabenstellung gemeint ist.
, entschuldige den Schuss vor den Bug, wishmoep, aber bei dieser Aufgabe scheinst du mir ein bisschen arg ins blaue hinein zu spekulieren, ohne zu wissen, was mit den Worten der Aufgabenstellung gemeint ist.
