| Autor |
Nachricht |
SamFisher39
Anmeldungsdatum: 14.10.2017
Beiträge: 4
|
 SamFisher39 Verfasst am: 14. Okt 2017 13:11 Titel: Anzahl der aufprallenden Teilchen auf Körper SamFisher39 Verfasst am: 14. Okt 2017 13:11 Titel: Anzahl der aufprallenden Teilchen auf Körper |
 |
|
Meine Frage:
Sauerstoffmoleküle in der Luft bei Standardbedingungen (T=20°C, p=1013 mbar)
1.) Wie viele O2-Teilchen gibt es im Kubikmeter? (rel. Sauerstoffanteil an Luft: 21%)
2.) Welche mittlere thermische Geschwindigkeit haben sie?
3.) Welcher Molekülfluss (Teilchen durch eine Fläche und Zeit) ergibt sich? Wie groß ist die Anzahl von Molekülen, die pro Sekunde auf die Körperoberfläche eines ausgewachsenen Menschen (A=2 m2) trifft?
1.) und 2.) meine ich beantwortet zu haben, aber zu 3.) wäre ich über jegliche Hilfe dankbar!
Meine Ideen:
Meine (ich hoffe richtigen) Ergebnisse zu:
 [EDIT]N = 5.25*10^{24} )
 \overline{v}=440\frac{m}{s})
Zu 3.) fehlt mir leider jeglicher Ansatz. Wir haben in der Vorlesung leider gar nichts zum Thema Molekülfluss besprochen. Finde auch durch Google nichts. Ich nehme an, dass die Wiki Seite zu "Effusion (Physik)" (kommt wenn ich nach "molekülfluss" google) nicht das ist, wonach ich suche.
Zuletzt bearbeitet von SamFisher39 am 15. Okt 2017 15:26, insgesamt einmal bearbeitet |
|
 |
SamFisher39
Anmeldungsdatum: 14.10.2017
Beiträge: 4
|
 SamFisher39 Verfasst am: 15. Okt 2017 11:08 Titel: SamFisher39 Verfasst am: 15. Okt 2017 11:08 Titel: |
 |
|
Hat denn niemand eine Idee zu diesem Problem?  |
|
 |
isi1
Anmeldungsdatum: 03.09.2006
Beiträge: 2903
Wohnort: München
|
 isi1 Verfasst am: 15. Okt 2017 11:37 Titel: isi1 Verfasst am: 15. Okt 2017 11:37 Titel: |
 |
|
| SamFisher39 hat Folgendes geschrieben: | | Hat denn niemand eine Idee zu diesem Problem? ?( |
Hast es mal mit dem Impulssatz versucht? der Druck p wird doch durch den elastischen Rückprall der Stickstoff- und Sauerstofmoleküle erzeugt. | Bernoullische Gleichung hat Folgendes geschrieben: |
p = 2/3 * n * w
(n: Anzahl der Moleküle je Volumeneinheit,
w: mittlere kinetische Energie eines Moleküls). |
_________________
Grüße aus München, isi ≡≈ ¹₁₂½√∠∞±∫αβγδεηκλπρσφω ΔΣΦΩ |
|
 |
SamFisher39
Anmeldungsdatum: 14.10.2017
Beiträge: 4
|
 SamFisher39 Verfasst am: 15. Okt 2017 14:38 Titel: SamFisher39 Verfasst am: 15. Okt 2017 14:38 Titel: |
 |
|
Also ich hätte jetzt N....Stöße/sec, 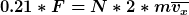 . Die 0.21 deshalb weil ca 21% der Luft aus . Die 0.21 deshalb weil ca 21% der Luft aus  besteht. Zur Vereinfachung hab ich die Masse und mittlere Geschwindigkeit der anderen Luft-Moleküle ( besteht. Zur Vereinfachung hab ich die Masse und mittlere Geschwindigkeit der anderen Luft-Moleküle (  , usw...) als die von , usw...) als die von  genommen. Dann hab ich die Geschwindigkeit über die Halbkugel gemittelt, weil uns ja nur eine Richtung der Geschwindigkeit interessiert. genommen. Dann hab ich die Geschwindigkeit über die Halbkugel gemittelt, weil uns ja nur eine Richtung der Geschwindigkeit interessiert.
 \overline{v}=\frac{2}{\pi}\overline{v}=\overline{v_x})
Und dadurch komm ich also auf

Kann das stimmen? Ich bin mir bei der mittleren Geschwindigkeit in x-Richtung ziemlich unsicher... |
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 15. Okt 2017 15:17 Titel: Myon Verfasst am: 15. Okt 2017 15:17 Titel: |
 |
|
Noch zu a: Dein Resultat wäre die Anzahl der Luftmoleküle pro qm, gefragt ist nach der Anzahl O2-Moleküle.
Zu c: die Frage nach dem Molekülfluss durch eine Fläche irritiert mich ein wenig. Denn der Fluss wäre ja gleich null, wenn die Geschwindigkeiten der Moleküle isotrop verteilt sind. Wahrscheinlich ist gemeint, wieviel Moleküle pro qm auf eine Fläche auftreffen.
Mit

komme ich auf etwa  , also eine ähnliche Grössenordnung. , also eine ähnliche Grössenordnung.
( wäre gleich null. Es gilt wäre gleich null. Es gilt  . Dann noch ein Faktor 1/2, da nur die eine Hälfte der Moleküle gegen eine Fläche geht, der Rest in die entgegengesetzte Richtung) . Dann noch ein Faktor 1/2, da nur die eine Hälfte der Moleküle gegen eine Fläche geht, der Rest in die entgegengesetzte Richtung)
PS: Verstehe nicht ganz, wieso Du nicht nur die Masse der Sauerstoffmoleküle berücksichtigst. |
|
 |
SamFisher39
Anmeldungsdatum: 14.10.2017
Beiträge: 4
|
 SamFisher39 Verfasst am: 15. Okt 2017 15:24 Titel: SamFisher39 Verfasst am: 15. Okt 2017 15:24 Titel: |
 |
|
zu 1.) hab falsch abgeschrieben. Es sollten 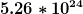 sein. sein.
zu 3.)Was bedeutet denn

und was ist das n? Die Anzahl der Teilchen pro qm? Kann ich die Formel irgendwo nachschlagen? |
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 6200
|
 Myon Verfasst am: 15. Okt 2017 15:42 Titel: Myon Verfasst am: 15. Okt 2017 15:42 Titel: |
 |
|
Ja, n wäre die Teilchendichte. In meiner Vorlesungsaufzeichnung kommt das so vor mit dem Faktor 1/6 in Zusammenhang mit der Herleitung des Drucks aus der Geschwindigkeitsverteilung bzw. der mittleren kinetischen Energie der Teilchen.
Allerdings muss ich sagen, dass ich bezüglich der durchschnittlichen Geschwindigkeit v_x auch grad unsicher bin. |
|
 |
as_string
Moderator

Anmeldungsdatum: 09.12.2005
Beiträge: 5796
Wohnort: Heidelberg
|
 as_string Verfasst am: 16. Okt 2017 14:58 Titel: as_string Verfasst am: 16. Okt 2017 14:58 Titel: |
 |
|
Kommt die 1/6 nicht einfach daher, dass man drei Raumrichtungen hat, in die das Teilchen jeweils in zwei verschiedene (positiver und negativer) Richtung fliegen kann? Zwei mal drei ergibt 6 also hat man nur ein Sechstel der Teilchen, die von einer Seite auf eine beliebig im Raum ausgerichtete Fläche prallen.
Gruß
Marco |
|
 |
|
















