| Autor |
Nachricht |
jentowncity
Anmeldungsdatum: 08.05.2005
Beiträge: 132
Wohnort: hamburg
|
 jentowncity Verfasst am: 30. Mai 2008 19:29 Titel: Mischen impossible jentowncity Verfasst am: 30. Mai 2008 19:29 Titel: Mischen impossible |
 |
|
Hallo an alle!
Kämpfe gerade mit dem folgenden Problem:
Ein Behälter sei durch Trennwände in drei Kammern eingeteilt. Die linke enthalte  Teilchen eines idealen Gases, die rechte Teilchen eines idealen Gases, die rechte 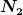 Teilchen Teilchen
a) eines anderen idealen Gases,
b) des gleichen idealen Gases.
In beiden Kammern hersche die selbe Temperatur  . Die mittlere ( . Die mittlere ( ) Kammer sei leer. ) Kammer sei leer.
Wie ändert sich die Entropie des Systems, wenn die Wände durchstochen werden? Was ist das Gibbssche Paradoxon?
Also mein Lösungvorschlag ist bisher: für a)
+S_{2}(T,V_{2},N_{2}))
+S_{2}(T,V_{1}+V_{2}+V_{3},N_{2}))
für b) ist der Anfangszustand gleich, und der Endzustand ist:
)
Für das ideale Gas hatten wir in der Vorlesung die Formel
+ln(\frac{V}{N})+C)) mit nur vom Referenzzustand abhängigen Konstante C. Zur Vereinfachung könnte man das noch schreiben als: mit nur vom Referenzzustand abhängigen Konstante C. Zur Vereinfachung könnte man das noch schreiben als:
)
Wenn ich jetzt alles einsetze und  bilde, kommt bei mir folgendes raus (mit bilde, kommt bei mir folgendes raus (mit  und und  ): ):
für a)

und für b)

Stimmt das soweit? Und das unterschiedliche Ergebnis soll hier das Gibbsche Paradoxon sein?  |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 31. Mai 2008 18:26 Titel: dermarkus Verfasst am: 31. Mai 2008 18:26 Titel: |
 |
|
Deine Rechnung scheint mir, ausgehend von der fertigen Formel aus deiner Vorlesung, Sinn zu machen.
Magst du nun aber noch in deinen Vorlesungsaufschrieben, Büchern, etc. nachschauen, was man unter den Gibbschen Paradoxon versteht, um das auch selbst zu verstehen und in Worten formulieren zu können?
Kannst du zum Beispiel schon sagen, warum das "Paradoxon" heißt? Von was für einem Modellexperiment handelt es? Was wäre die "intuitiv" zu erwartende Lösung? Was ist die tatsächliche Lösung? Worin liegt dabei etwas paradoxes, gibt es da einen scheinbaren Widerspruch? Worin besteht die Auflösung dieses scheinbaren Widerspruches? |
|
 |
jentowncity
Anmeldungsdatum: 08.05.2005
Beiträge: 132
Wohnort: hamburg
|
 jentowncity Verfasst am: 01. Jun 2008 12:05 Titel: jentowncity Verfasst am: 01. Jun 2008 12:05 Titel: |
 |
|
Danke für die Antwort dermarkus!
Also ich hab mir das nochmal angesehen mit dem Gibbsschen Paradoxon:
Eigentlich wird dabei das Experiment mit nur zwei Kammern betrachtet, statt drei. Im Falle des gleichen Gases würde man intuitiv nach dem Öffnen der Trennwand keine Entropiezunahme erwarten (bei gleichem Druck und gleicher Temperatur), da es der selbe thermodynamische Zustand ist wie mit der Wand dazwischen. Das Paradoxe dabei ist, dass es eigentlich nicht auf die Art des Gases ankommen sollte und für alle Fälle immer die selbe Formel gültig sein sollte. Dies wird auch klar, wenn man im Falle des gleichen Gases jedes Teilchen betrachtet. Dann wird klar, dass die Gase auch dann durchmischen, wenn sie gleich sind (also Entropiezunahme). Die Auflösung wäre demnach, dass die Entropie eine Makrovariable ist, die einen Makrozustand beschreibt, der aus verschiedenen Mikrozuständen hervorgehen kann, zwischen denen aber nicht unterschieden wird (Entartung). Dies könnte man ändern (wenn man eine ganz genaue Beschreibung haben will, ohne solche Paradoxien) indem man berücksichtigt, dass die Teilchen nicht unterscheidbar sind, was wohl später in der Statistik aufgelöst wird.
Kommt das soweit der Wahrheit nahe? Für den Fall mit drei Kammern, könnte man die Durchmischung auch so durchführen, dass man erst die beiden Gase miteinander mischt (Rückführung auf den Fall aus der Literatur) und das Gemisch dann in die leere Kammer expandieren lässt, oder? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 01. Jun 2008 23:25 Titel: dermarkus Verfasst am: 01. Jun 2008 23:25 Titel: |
 |
|
Ich bin einverstanden, dass es für das Gibbsche Paradoxon ausreicht, nur zwei Kammern zu betrachten.
Magst du aber den Rest deiner Überlegungen nochmal überprüfen, zum Beispiel gerne auch durch Vergleich mit Quellen wie
http://de.wikipedia.org/wiki/Gibbssches_Paradoxon
? Was wäre die Erwartung für den Ausgang des Experimentes, wenn man klassisch von durchnummerierten Teilchen ausgeht? Und wie würdest du das ganze formulieren, wenn man diese klassische Vorhersage als "intuitive" Erwartung bezeichnen möchte? |
|
 |
jentowncity
Anmeldungsdatum: 08.05.2005
Beiträge: 132
Wohnort: hamburg
|
 jentowncity Verfasst am: 02. Jun 2008 17:47 Titel: jentowncity Verfasst am: 02. Jun 2008 17:47 Titel: |
 |
|
Ah ok, habs jetzt verstanden. Ich hab davor das Huhn mit dem Ei etwas verwechselt.
Vielen Dank für deine Hilfe dermarkus!  |
|
 |
|
|

















