| Autor |
Nachricht |
FalkC.
Anmeldungsdatum: 04.03.2011
Beiträge: 3
|
 FalkC. Verfasst am: 04. März 2011 16:20 Titel: Kalorimetrie | Wärmeenergie FalkC. Verfasst am: 04. März 2011 16:20 Titel: Kalorimetrie | Wärmeenergie |
 |
|
Hallo Zusammen!
Kupfer mit der Masse 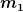 = 1kg und der Temperaur = 1kg und der Temperaur  = 300C° wird in einem Kalorimetergefäß aus Aluminium mit der Masse = 300C° wird in einem Kalorimetergefäß aus Aluminium mit der Masse = 0,5kg gegeben. Das Kalorimetergefäß mit darin Wasser hat die Temperatur 20C°. = 0,5kg gegeben. Das Kalorimetergefäß mit darin Wasser hat die Temperatur 20C°.
 = 50C° = 50C°
 = 4180 J/kg*K = 4180 J/kg*K
 = 900 J/kg*K = 900 J/kg*K
 = 383 J/kg*K = 383 J/kg*K
a.) Wieviel Wasser ist im Kalorimeter?
b.) Welche Energie hat das Kaloriemeter mit dem Wasser durch die Hinzugabe des Kupfers?
c.) Welche Energie gibt das Kalorimeter einschließlich Inhalt an die Umgebung ab, wenn es wieder auf 20C° abkühlt?
a.)
 = =
 * * * * - -) + +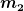 * * * * - -) = =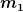 * * *( *( - - ) )
nach  umgestellt kommt bei mir 0,656kg heraus. umgestellt kommt bei mir 0,656kg heraus.
soweit klar, müsste passen.
b.)
Jetzt gehts los.
Meine Annahme: alles was im Kalorimeter ist, hat die selbe Temperatur( =50C°) daher: =50C°) daher:
 * * + +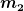 * * + +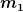 * * )*( )*( ) )
Werte eingesetzt ergibt bei mir : 178,545*10^3 J
c.) Der selbe Weg wie bei b.) nur anstelle der 50C° --> 30C° eingesetzt.
Ergebnis : 107,127*10^3
Frage: Ich habe leider keinerlei Lösung und weiss nicht ob es richtig ist, kann jemand einmal gegenrechnen?
Bei b.) und c.) bin ich mir nicht sicher, ob ich so vorgehen kann. Steckt irgendwo der Wurm drin, oder passt es so? Wenn noch was unklar ist, bitte sagen.
Grüße und ein schönes Wochenende
Zuletzt bearbeitet von FalkC. am 04. März 2011 17:35, insgesamt einmal bearbeitet |
|
 |
magician4
Anmeldungsdatum: 03.06.2010
Beiträge: 914
|
 magician4 Verfasst am: 04. März 2011 17:25 Titel: Re: Kalorimetrie | Wärmeenergie magician4 Verfasst am: 04. März 2011 17:25 Titel: Re: Kalorimetrie | Wärmeenergie |
 |
|
zu a: vom weg her einverstanden
vom ergebnis hab ich grad 0.684 kg raus, aber auch nach zweimaligem nachrechnen find ich meinen fehler nicht: magst du sicherheitshalber daher deine berechnung nochmal wiederholen ?
zu b:
(ich benutze deinen wassermassen-wert weiter)
wennn ich dich recht verstehe, dann meinst du hier:
wohl eher das hier:
 * * + +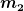 * * + +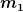 * *) * *
man kann ueber einen solchen ansatz trefflich disputieren: quasi die spezifische wärmekapazitaet ausgehend von null kelvin linear durchgehend einfach mit masse , temperatur multiplizieren... und gut isset.
in der realitaet hast du da allerdings ein paar probleme, z.b. mach wasser einen phasenuebergang zu eis unterwegs, und die spezifische waermekapazitaet von wasser ist doch eine drastisch andere als die des eises, und m.a.n. auch keineswegs hinreichend konstant ueber den betrachteten temperaturbereich
andereseits wirkt die aufgabenenstellung auf mich so, als wuerde man genau dieses von dir erwarten ( ? *stirnrunzel)
nuja...
..aber wenn du das dann schon so angehst, dann benutze die temperatur bitte nicht in °C wie du es offensichtlich getan hast, sondern in kelvin... und dann kommt auch ein groesserer wert heraus: ~ 1155 kJ
zu c:
mein ansatz
 * * + +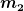 * * + +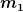 * *) * *
mit delta T = 50°C - 20°C = 30 K
gruss
ingo
|
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 04. März 2011 17:37 Titel: franz Verfasst am: 04. März 2011 17:37 Titel: |
 |
|
Technischer Hinweis
Mir sind die Bezeichnungen etwas unübersichtlich, 1, 2, 3, Alu, Cu, Wasser ... Notfalls eine Liste vorweg.
Die Temperaturen bei solchen Mischungsaufgaben zweckmäßigerweise durchweg in °C; aber statt T vielleicht t oder \vartheta 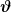 . .
Drittens LateX ruhig für komplette Formeln, nicht nur Symbole; zum Bleistift so
+m_2 c_2\left(T_m-T_2\right) ...) . .
|
|
 |
FalkC.
Anmeldungsdatum: 04.03.2011
Beiträge: 3
|
|
 |
magician4
Anmeldungsdatum: 03.06.2010
Beiträge: 914
|
 magician4 Verfasst am: 04. März 2011 18:40 Titel: magician4 Verfasst am: 04. März 2011 18:40 Titel: |
 |
|
zu b:
ich halte fragen wie "welche energie hat.." in unspezifiziert immer fuer etwas problematisch: schliesslich koennte man ja auf die verwegene idee kommen (auch wenn mir dies grad aufgabenfremd scheint) zur "gesamtenergie" dann z.b. das energetische massenaequivalent nach einstein mit einzuberechnen u.ae.
der von mir angesprochene phasenuebergang betraf uebrigens nicht die verdampfungsenthalpie, sondern die schmelzenthalpie (denn gerade die z.b. liegt ja zwischen 0 K und 50°C, bei 273K naemlich [bei normaldruck] fuer wasser)
zu c bin ich nach wie vor nicht einverstanden: wenn ichs recht sehe berechnest du da die "gesamtenergie" von 0 K bis 30°C = 303 K
gefragt ist hingegen die differenzenergie des gesamtsystems zwischen 50°C (323 K) und 20°C (293 K)
du musst daher tatsaechlich delta T = 30 K multiplikativ in ansatz bringen
gruss
ingo
p.s.: es macht mir ganz leicht den eindruck, als wenn du da mit °C und K immer ein wenig am hadern bist, wann du nun was und wie benutzen sollst. falls dem so sein sollte: mach dir das ganze nochmal in ruhe klar, sonst wirds dauerhaft zuu ner boesen archillesferse.
falls ich mich getaeuscht haben sollte: nix fuer ungut
|
|
 |
FalkC.
Anmeldungsdatum: 04.03.2011
Beiträge: 3
|
 FalkC. Verfasst am: 04. März 2011 23:00 Titel: FalkC. Verfasst am: 04. März 2011 23:00 Titel: |
 |
|
Ernst zu nehmende Kritik nehme ich jeder Zeit und gerne an! Danke!  ... Habe die Aufgabe gerade nochmal überflogen... manchmal ist man einfach blind. Ich stelle morgen früh nochmal einen neuen Lösungsansatz rein. ... Habe die Aufgabe gerade nochmal überflogen... manchmal ist man einfach blind. Ich stelle morgen früh nochmal einen neuen Lösungsansatz rein.
|
|
 |
|
|


















 ... Habe die Aufgabe gerade nochmal überflogen... manchmal ist man einfach blind. Ich stelle morgen früh nochmal einen neuen Lösungsansatz rein.
... Habe die Aufgabe gerade nochmal überflogen... manchmal ist man einfach blind. Ich stelle morgen früh nochmal einen neuen Lösungsansatz rein.