| Autor |
Nachricht |
Iduna

Anmeldungsdatum: 15.01.2007
Beiträge: 313
|
 Iduna Verfasst am: 30. Mai 2007 17:29 Titel: Geschwindigkeitsberechnung von Gasteilchen Iduna Verfasst am: 30. Mai 2007 17:29 Titel: Geschwindigkeitsberechnung von Gasteilchen |
 |
|
Richtige Anwendung von n??
Welche mittlere Geschwindigkeit haben Gasteilchen bei einer Temperatur von 17°C?
a) Stickstoffteilchen 
Um die mittlere Geschwindigkeit auszurechnen habe ich ja die Formel:

Aber 
muss ich ja erst ausrechnen. Kann ich die Masse dann so ausrechnen:

 ???? ????  |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 30. Mai 2007 17:40 Titel: dermarkus Verfasst am: 30. Mai 2007 17:40 Titel: |
 |
|
Überprüf deine Formel für die mittlere Geschwindigkeit noch einmal, da ist noch ein Tippfehler drin. Vielleicht magst du zum Kontrollieren die Form dieser Gleichung verwenden, in der du direkt die kinetische Energie drinstehen siehst.
In deiner Berechnung für die Masse hast du zwar die Einheiten vergessen, aber ich glaube, du meinst das Richtige. |
|
 |
Iduna

Anmeldungsdatum: 15.01.2007
Beiträge: 313
|
 Iduna Verfasst am: 30. Mai 2007 19:26 Titel: Iduna Verfasst am: 30. Mai 2007 19:26 Titel: |
 |
|
Ja, das mit den Einheiten hatte ich versucht, aber das konnte dann nie angezeigt werden, weil ich da irgend ein Fehler drin hatte und ihn nicht gefunden hatte.
Ach bei der mittleren Geschwindigkeit hab ich die Wurzel vergessen ^^
Also über dem ganzen Teil der nach dem Gleichheitszeichen steht kommt noch eine Wurzel oben drüber. |
|
 |
Iduna

Anmeldungsdatum: 15.01.2007
Beiträge: 313
|
 Iduna Verfasst am: 30. Mai 2007 19:30 Titel: Iduna Verfasst am: 30. Mai 2007 19:30 Titel: |
 |
|
ach ja, eine Frage dazu hätte ich noch
Ist die Stoffmenge eigentlich das Gleiche wie die Avogadrokonstante?
Bei der Rechnung hier hab ich ja für n die Avogadrokonstante genommen aber die wird ja normalerweise mit  angegeben??? angegeben??? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 30. Mai 2007 23:41 Titel: dermarkus Verfasst am: 30. Mai 2007 23:41 Titel: |
 |
|
| Iduna hat Folgendes geschrieben: |
Ist die Stoffmenge eigentlich das Gleiche wie die Avogadrokonstante?
Bei der Rechnung hier hab ich ja für n die Avogadrokonstante genommen aber die wird ja normalerweise mit  angegeben??? angegeben??? |
Welche Anzahl von Teilchen bezeichnet denn die Avogadrokonstante N_A ? Wann ist diese Anzahl Teilchen also gleich groß wie die als Teilchenanzahl angegebene Stoffmenge, und wann nicht? |
|
 |
Iduna

Anmeldungsdatum: 15.01.2007
Beiträge: 313
|
 Iduna Verfasst am: 01. Jun 2007 12:35 Titel: Iduna Verfasst am: 01. Jun 2007 12:35 Titel: |
 |
|
Die Avogadrokonstante gibt an aus wie vielen Molekülen ein mol besteht.
Und was dieses mol in gramm wiegt.
Die Avogadrokonstante gibt ja auch nur eine Stoffmenge an, nämlich das mol. Das wären 6,022137*10^23 Moleküle/mol. Heisst das, dann, dass wenn ich eine Stoffmenge mit 6,022137*10^23 Moleküle/mol habe, diese Stoffmenge genauso groß ist, wie die Avogadrokonstante. Und wenn das so ist, wie weiß ich dann, wann ich mit der Avogadrokonstante zu rechnen habe und wann mit einer Stoffmenge???? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 01. Jun 2007 14:13 Titel: dermarkus Verfasst am: 01. Jun 2007 14:13 Titel: |
 |
|
| Iduna hat Folgendes geschrieben: | Die Avogadrokonstante gibt an aus wie vielen Molekülen ein mol besteht.
(...)
Das wären 6,022137*10^23 Moleküle/mol.
|
Einverstanden, da hast du nun ziemlich genau verstanden und mit der genauen Einheit ziemlich gut aufgeschrieben, was die Avogadrokonstante ist 
| Zitat: |
Und was dieses mol in gramm wiegt.
|
Das ist etwas ganz anderes als die Avogadrokonstante. Meinst du da vielleicht das Molgewicht?
| Zitat: |
Die Avogadrokonstante gibt ja auch nur eine Stoffmenge an, nämlich das mol.
|
Da hast du etwas durcheinandergebracht. Natürlich hat die Avogadrokonstante etwas mit einer Stoffmenge zu tun, und mit einem mol zu tun, aber damit das richtig und konkret verwendbar wird, was du da vielleicht versucht hast zu sagen, müsstest du es anders und genauer formulieren.
| Zitat: |
Heisst das, dann, dass wenn ich eine Stoffmenge mit 6,022137*10^23 Moleküle/mol habe,
|
Achtung, eine Stoffmenge hat ja nicht die Einheit Moleküle/mol. Löst sich deine Frage vielleicht am einfachsten, wenn du auch bei der Stoffmenge immer genau dazusagst, welche Einheit du meinst? |
|
 |
Gargy

Anmeldungsdatum: 24.11.2006
Beiträge: 1046
|
 Gargy Verfasst am: 01. Jun 2007 14:18 Titel: Gargy Verfasst am: 01. Jun 2007 14:18 Titel: |
 |
|
Ich glaube, in der Formel für die Masse ist ein Fehler drin.
Die molare Masse M hat die Einheit  . .
Also ist doch 
Damit ist 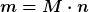 |
|
 |
Iduna

Anmeldungsdatum: 15.01.2007
Beiträge: 313
|
 Iduna Verfasst am: 02. Jun 2007 18:04 Titel: Iduna Verfasst am: 02. Jun 2007 18:04 Titel: |
 |
|
|
ups ja stimmt, ich hab die Formel verdreht >.< |
|
 |
Iduna

Anmeldungsdatum: 15.01.2007
Beiträge: 313
|
 Iduna Verfasst am: 02. Jun 2007 18:07 Titel: Iduna Verfasst am: 02. Jun 2007 18:07 Titel: |
 |
|
| dermarkus hat Folgendes geschrieben: | | Iduna hat Folgendes geschrieben: | Die Avogadrokonstante gibt an aus wie vielen Molekülen ein mol besteht.
(...)
Das wären 6,022137*10^23 Moleküle/mol.
|
Einverstanden, da hast du nun ziemlich genau verstanden und mit der genauen Einheit ziemlich gut aufgeschrieben, was die Avogadrokonstante ist 
| Zitat: |
Und was dieses mol in gramm wiegt.
|
Das ist etwas ganz anderes als die Avogadrokonstante. Meinst du da vielleicht das Molgewicht?
Ja da habe ich mich etwas zu knapp ausgedrückt. Wenn man die Molare Masse durch die Avogadrokonstante teilt, dann bekommt man das Gewicht raus.
| Zitat: |
Die Avogadrokonstante gibt ja auch nur eine Stoffmenge an, nämlich das mol.
|
Da hast du etwas durcheinandergebracht. Natürlich hat die Avogadrokonstante etwas mit einer Stoffmenge zu tun, und mit einem mol zu tun, aber damit das richtig und konkret verwendbar wird, was du da vielleicht versucht hast zu sagen, müsstest du es anders und genauer formulieren. |
Hmmm jetzt bin ich total verwirrt ^^ welche Einheit hat denn die Stoffmenge? Nur mol oder?
|
|
 |
Iduna

Anmeldungsdatum: 15.01.2007
Beiträge: 313
|
 Iduna Verfasst am: 03. Jun 2007 01:40 Titel: Iduna Verfasst am: 03. Jun 2007 01:40 Titel: |
 |
|
|
Aber woher weiß ich denn jetzt, dass ich bei dieser Aufgabe hier, die Avogadrokonstante benutzen kann? |
|
 |
Iduna

Anmeldungsdatum: 15.01.2007
Beiträge: 313
|
 Iduna Verfasst am: 03. Jun 2007 01:49 Titel: Iduna Verfasst am: 03. Jun 2007 01:49 Titel: |
 |
|
noch eine Frage dazu...
welche Einheit hat eigentlich  ??? ??? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 03. Jun 2007 22:56 Titel: dermarkus Verfasst am: 03. Jun 2007 22:56 Titel: |
 |
|
| Iduna hat Folgendes geschrieben: |
welche Einheit hat denn die Stoffmenge? Nur mol oder? |
Ja, natürlich.
Wenn du magst, dann kannst du eine Stoffmenge auch gerne in Teilchen oder in kg angeben.
| Iduna hat Folgendes geschrieben: | | Aber woher weiß ich denn jetzt, dass ich bei dieser Aufgabe hier, die Avogadrokonstante benutzen kann? |
Zeig doch einfach nochmal deine Rechnung vom Anfang, indem du sie ganz sauber mit allen Einheiten aufschreibst. Ich glaube, das wird dir helfen, sorgfältig zu überlegen, von was du sprichst, und deine Fragen könnten sich allein dadurch schon in Wohlgefallen auflösen.
| Iduna hat Folgendes geschrieben: | noch eine Frage dazu...
welche Einheit hat eigentlich  ??? ??? |
Na, damit meinst du doch die mittlere Geschwindigkeit der Teilchen. Und welche Einheit hat eine Geschwindigkeit? |
|
 |
Iduna

Anmeldungsdatum: 15.01.2007
Beiträge: 313
|
 Iduna Verfasst am: 06. Jun 2007 08:32 Titel: Iduna Verfasst am: 06. Jun 2007 08:32 Titel: |
 |
|
Also meine Rechnung würde so aussehen:

da ich  nicht gegeben habe, kann ich dies über die Formel nicht gegeben habe, kann ich dies über die Formel
 berechnen indem ich diese dann nach m umstelle berechnen indem ich diese dann nach m umstelle 
dann setz ich das alles in meine obige Formel ein

dann setz ich meine Zahlenwerte ein

naja dann bekomm ich das mal wieder mit Latex net gebacken  wär sehr lieb wenn jemand den Fehler finden würde. wär sehr lieb wenn jemand den Fehler finden würde.
[ja, LaTeX hier mag keine direkten Umlaute .. ich hab's mal korrigiert, para]
Jedenfalls weiß ich nicht, wie aus den ganzen Einheiten  rauskommt rauskommt  |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jun 2007 11:52 Titel: dermarkus Verfasst am: 06. Jun 2007 11:52 Titel: |
 |
|
Tipp: Der Nenner in der Wurzel ist ja die Masse eines Teilchens  . Welche Einheit muss die haben? . Welche Einheit muss die haben?
Was meinst du mit dem 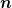 , und welche Einheiten kann es zum Beispiel haben? , und welche Einheiten kann es zum Beispiel haben? |
|
 |
Iduna

Anmeldungsdatum: 15.01.2007
Beiträge: 313
|
 Iduna Verfasst am: 06. Jun 2007 12:10 Titel: Iduna Verfasst am: 06. Jun 2007 12:10 Titel: |
 |
|
Mit 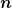 meinte ich die Stoffmenge, wofür ich aber jetzt die Avogadrokonstante verwendet hatte.... wenn ich die Stoffmenge benutzt hätte, wäre die Einheit mol gewesen. meinte ich die Stoffmenge, wofür ich aber jetzt die Avogadrokonstante verwendet hatte.... wenn ich die Stoffmenge benutzt hätte, wäre die Einheit mol gewesen.
Im Nenner, wenn ich mol wegkürze, würde dann eine Masse stehen, also in dem Fall hier kg. Also würde da z.B. stehen dass es 5 kg pro 10 Moleküle hätte. (nur ein Beispiel) |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jun 2007 12:37 Titel: dermarkus Verfasst am: 06. Jun 2007 12:37 Titel: |
 |
|
Und welche Stoffmenge verwendest du konkret in deiner Rechnung? Wieviel mol sind das 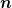 , das du hier meinst? , das du hier meinst? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jun 2007 12:57 Titel: dermarkus Verfasst am: 06. Jun 2007 12:57 Titel: |
 |
|
| Gargy hat Folgendes geschrieben: | Ich glaube, in der Formel für die Masse ist ein Fehler drin.
Die molare Masse M hat die Einheit  . .
Also ist doch 
Damit ist 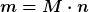 |
| Iduna hat Folgendes geschrieben: | | ups ja stimmt, ich hab die Formel verdreht >.< |
Ich merke gerade, dass du jetzt Gargys Formel nimmst. Du hattest deine Formel nicht verdreht.
Magst du das ganze am besten mal ganz einfach an einem Beispiel direkt ausrechnen?
Eine Packung Gummibärchen habe die Masse 30 g.
In der Packung seien 15 Gummibärchen drin.
Wie groß ist also die Masse eines einzelnen Gummibärchens?
Welche Masse hat ein mol unseres Stoffes?
Wieviele Teilchen sind da drin?
Wie groß ist also die Masse eines einzelnen Teilchens? |
|
 |
Iduna

Anmeldungsdatum: 15.01.2007
Beiträge: 313
|
 Iduna Verfasst am: 06. Jun 2007 16:54 Titel: Iduna Verfasst am: 06. Jun 2007 16:54 Titel: |
 |
|
Hmm aber ich hatte doch die Formel verkehrt umgestellt? Also in meinem Skript steht auch dass  und wenn ich das dann nach m umstelle bekomm ich dann für m doch das hier raus: und wenn ich das dann nach m umstelle bekomm ich dann für m doch das hier raus:  oder nicht? *verwirrt bin* oder nicht? *verwirrt bin*
Die Masse eines einzeln Gummibärchen wäre ja dann 
Ein mol hat die Masse von  kg kg
Ein mol unseres Stoffes hat  Teilchen Teilchen
Dann hat ein Teilchen die Masse von 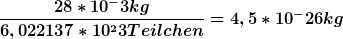 |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jun 2007 17:12 Titel: dermarkus Verfasst am: 06. Jun 2007 17:12 Titel: |
 |
|
Na, und wem vertraust du mehr? Den Gummibärchen oder deiner Interpretation, was die Formel aus dem Skript bedeuten soll?
--------------------------------------------
Magst du mal eine ganz andere kleine Aufgabe rechnen? Welche Masse m haben n mol eines Stoffes, wenn die Molmasse dieses Stoffes M ist?
Werte: Stoffmenge n= 3 mol, Molmasse M = 16 g/mol. |
|
 |
Iduna

Anmeldungsdatum: 15.01.2007
Beiträge: 313
|
 Iduna Verfasst am: 07. Jun 2007 17:29 Titel: Iduna Verfasst am: 07. Jun 2007 17:29 Titel: |
 |
|
na den Gummibärchen natürlich 
Also würde die Rechnung dann so aussehn:

 bin wieder zu doof. bin wieder zu doof.
Jedenfalls würde dann im Nenner unten das stehn:
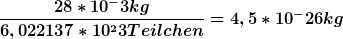 |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 07. Jun 2007 20:09 Titel: dermarkus Verfasst am: 07. Jun 2007 20:09 Titel: |
 |
|
Magst du die Rechnung für  einfach nochmal in den Taschenrechner eintippen? Dann findest du sicher ganz schnell deinen Flüchtigkeitsfehler. einfach nochmal in den Taschenrechner eintippen? Dann findest du sicher ganz schnell deinen Flüchtigkeitsfehler. |
|
 |
Iduna

Anmeldungsdatum: 15.01.2007
Beiträge: 313
|
 Iduna Verfasst am: 07. Jun 2007 20:47 Titel: Iduna Verfasst am: 07. Jun 2007 20:47 Titel: |
 |
|
ou ok, da kommt ja was ganz anderes raus 
 wäre dann 508,27 wäre dann 508,27  |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 07. Jun 2007 20:55 Titel: dermarkus Verfasst am: 07. Jun 2007 20:55 Titel: |
 |
|
Prima 
Und wie weit bist du mit der anderen kleinen Aufgabe, die dir helfen soll, zu lernen, was die Formel bedeutet, die du in deinem Skript gefunden hattest? |
|
 |
|


















 wär sehr lieb wenn jemand den Fehler finden würde.
wär sehr lieb wenn jemand den Fehler finden würde.

