| Autor |
Nachricht |
jentowncity
Anmeldungsdatum: 08.05.2005
Beiträge: 132
Wohnort: hamburg
|
 jentowncity Verfasst am: 01. Mai 2008 18:03 Titel: Temperaturausgleich jentowncity Verfasst am: 01. Mai 2008 18:03 Titel: Temperaturausgleich |
 |
|
Hallo an alle!
Habe Probleme bei folgender Aufgabe:
Zwei vollständig voneinander isolierte Flüssigkeiten  und und  mit festen Volumina und konstanten Wärmekapazitäten mit festen Volumina und konstanten Wärmekapazitäten  und und  haben anfangs die Temperaturen haben anfangs die Temperaturen  . .
Eine Carnot-Maschine benutzt die Flüssigkeit  als Wärmequelle und als Wärmequelle und  als Wärmesenke. Sie arbeitet zwischen diesen beidenReservoiren bis diese die gleiche Temperatur als Wärmesenke. Sie arbeitet zwischen diesen beidenReservoiren bis diese die gleiche Temperatur  erreicht haben. erreicht haben.
Bestimmen Sie diese Temperatur  und berechnen Sie die Arbeit, die die Carnot-Maschine verrichtet hat. und berechnen Sie die Arbeit, die die Carnot-Maschine verrichtet hat.
Also ich hab keine Ahnung wie ich das machen soll... Hab mir bis jetzt nur Folgendes überlegt: Nach einmaligem Durchlauf sollte sich die innere Energie nicht ändern, d.h.  , wobei , wobei  die dem käteren Reservoir zugefürte Wärmemenge ist. Und es gilt die dem käteren Reservoir zugefürte Wärmemenge ist. Und es gilt  . Aber ich bekomme irgendwie keine Gleichgewichtsbedingung, aus der ich dann die Temperatur . Aber ich bekomme irgendwie keine Gleichgewichtsbedingung, aus der ich dann die Temperatur  berechnen könnte berechnen könnte 
Kann mir jemand helfen? |
|
 |
para
Moderator

Anmeldungsdatum: 02.10.2004
Beiträge: 2874
Wohnort: Dresden
|
 para Verfasst am: 03. Mai 2008 18:09 Titel: para Verfasst am: 03. Mai 2008 18:09 Titel: |
 |
|
Die Überlegungen sehen soweit schonmal ziemlich gut aus. :)
Bei einem infinitesimal kleinen Durchlauf wird dem wärmeren Reservoir also eine gewisse Wärmemenge dQ1 entzogen und dem unteren eine Wärmemenge -dQ2 zugeführt. Die Differenz zwischen beiden ist, wie du schon gesagt hast, die gewonnene Arbeit:Nach diesem Durchlauf haben sich die Temperaturen der Reservoirs entsprechend geändert:Danach kann man einen neuen Kreisdurchlauf zwischen diesen veränderten Temperaturen betrachten.
Soweit alles prima. Ich vermute der Punkt an dem es bei dir noch etwas haken könnte ist, eine Beziehung zwischen dQ1 und dQ2 zu finden. Liege ich da richtig? Was lässt sich denn beim Carnot-Prozess zu den aufgenommenen/abgegeben Wärmen sagen? Ein Blick auf die Entropiebilanz, oder - daraus folgend - dem Wirkungsgrad könnte da vielleicht weiterhelfen.
_________________
Formeln mit LaTeX |
|
 |
jentowncity
Anmeldungsdatum: 08.05.2005
Beiträge: 132
Wohnort: hamburg
|
 jentowncity Verfasst am: 04. Mai 2008 10:35 Titel: jentowncity Verfasst am: 04. Mai 2008 10:35 Titel: |
 |
|
Danke para!
Ja, deine Vermutung ist schon richtig... Ich hab mir das jetzt mal genauer angesehen und den Zusammenhang zwischen 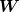 und und 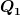 durch den Wirkungsgrad gefunden: durch den Wirkungsgrad gefunden:
)
mit ) kann ich dann schreiben: kann ich dann schreiben:
-C_{2}(T_{0}-T_{2})=C_{1}(T_{1}-T_{0})\left(1-\frac{T_{2}}{T_{1}}\right))
und wenn ich das jetzt auflöse, ergibt sich:
}{C_{1}T_{2}+C_{2}T_{1}})
Kann das so hinkommen? Irgendwie gefällt mir noch etwas dabei nicht.  |
|
 |
para
Moderator

Anmeldungsdatum: 02.10.2004
Beiträge: 2874
Wohnort: Dresden
|
 para Verfasst am: 04. Mai 2008 11:56 Titel: para Verfasst am: 04. Mai 2008 11:56 Titel: |
 |
|
| jentowncity hat Folgendes geschrieben: | Irgendwie gefällt mir noch etwas dabei nicht.  |
Ja, da ist in der Tat noch der Wurm drin. Die von dir berechnete Maschine funktioniert noch viel zu gut. ^^
Das Problem ist folgendes: der Wirkungsgrad einer Carnot-Maschine hängt ja von der oberen und der unteren Temperatur des Arbeitsgases bei einem Durchlauf ab. Deine Rechnung beschreibt das Ganze jetzt so, als nähme man ein Arbeitsgas, dass die gesamte auszutauschende Wärme bei der Temperatur T1 aufnimmt, und bei T2 wieder abgibt.
Sobald man aber dem oberen Wärmereservoir eine kleine Wärmemenge dQ1 entzogen hat, sinkt ja bereits dessen Temperatur. (Analog steigt die Temperatur T2 nach der Aufnahme von dQ2). Damit ist kein Carnot-Kreisprozess mehr zwischen T1 und T2 möglich, sondern nur noch zwischen den jetzt veränderten Temperaturen, mit einem anderen (schlechteren) Wirkungsgrad.
Das Optimum an Arbeit könnte man nun erreichen, indem man theoretisch unendlich viele Durchläufe eines Carnot-Prozesses durchführt, und dabei immer den optimalen Wirkungsgrad der jeweiligen Temperaturen erreicht. Das macht man so lange, bis beide Reservoirs die gleiche Temperatur T0 erreicht haben.
Hast du eine Idee wie du diese damit berechen könntest?
_________________
Formeln mit LaTeX |
|
 |
jentowncity
Anmeldungsdatum: 08.05.2005
Beiträge: 132
Wohnort: hamburg
|
 jentowncity Verfasst am: 04. Mai 2008 12:28 Titel: jentowncity Verfasst am: 04. Mai 2008 12:28 Titel: |
 |
|
Wie man das berechnen könnte, wenn man unendlich viele Durchläufe machen würde, habe ich keine Ahnung...
Ich hab mir das dann so gedacht, dass ich nur einen Durchlauf mache und dabei die Maschine Q1 aufnimmt und Q2 abgibt und die Differenz in Arbeit umwandelt. Dabei arbeitet die Maschine zwischen den Temperaturen T1 und T2.
Warum würde das nicht funktionieren, wenn ich das ganze in nur einem Durchlauf mache?
Und könntest du mir eventuell auf die Sprünge helfen wie man das durch unendlich viele Schritte hinbekommt? Das wird wohl irgend eine Integration von 0 bis unendlich sein, aber was soll ich integrieren? Darauf komm ich noch nicht... |
|
 |
jentowncity
Anmeldungsdatum: 08.05.2005
Beiträge: 132
Wohnort: hamburg
|
 jentowncity Verfasst am: 04. Mai 2008 16:19 Titel: jentowncity Verfasst am: 04. Mai 2008 16:19 Titel: |
 |
|
Ah, ok, ich hab jetzt verstanden warum man nicht alles in einem Durchgang erledigen kann. Das hast du ja eigentlich schon bei deinem letzten Beitrag gesagt.
Aber ich hab immer noch nicht alles durchblickt wie ich das jetzt rausbekommen kann. Meine Gedanken dazu sind bisher die folgenden:
Nach jedem Durchgang ändert sich die Arbeit so:
=\delta Q_{2n+1}-\delta Q_{2n+2}) wobei alle Qs positiv sind (damit ich nicht mit den Vorzeichen durcheinander komme). wobei alle Qs positiv sind (damit ich nicht mit den Vorzeichen durcheinander komme).
Für die Temperaturen gilt:

Aber irgendwas fehlt mir noch um einen vernünftigen Ausdruck für  zu bekommen zu bekommen 
Kann mir jemand einen Tip geben? (ich muss diese Aufgabe morgen abgeben) |
|
 |
para
Moderator

Anmeldungsdatum: 02.10.2004
Beiträge: 2874
Wohnort: Dresden
|
 para Verfasst am: 04. Mai 2008 17:17 Titel: para Verfasst am: 04. Mai 2008 17:17 Titel: |
 |
|
Auf dem Weg würde man sehr wahrscheinlich auch zum Ziel kommen, aber er sieht etwas umständlich aus.
Der Weg den ich meine führt über die Betrachtung der Entropie (auf den gleichen Zusammenhang kommt man letztlich aber auch mit dem Wirkungsgrad). Der Carnot-Prozess ist ja reversibel, d.h. die Entropieänderung ist gerade Null. Für jeden Teilprozess muss also gelten:Auch wenn man alle Teilprozesse aufsummiert (bzw. beim Übergang zu infinitesimal kleinen Wärmemengen aufintegriert), muss diese Gleichheit noch erfüllt sein.
Etwas umgeschrieben sieht das so aus:Damit kann man komfortabler über die Temperaturen summieren/integrieren. Ausgehend von den Anfangstemperaturen T1 und T2 gibt es nur eine Temperatur T0 "in der Mitte", für die die Entropieänderung wirklich Null, also diese Gleichung erfüllt, ist. Das ist die Endtemperatur die sich nach optimaler Ausnutzung mittels Carnot-Prozessen einstellt.
Ist es auf diesem Weg soweit nachvollziehbar?
_________________
Formeln mit LaTeX |
|
 |
jentowncity
Anmeldungsdatum: 08.05.2005
Beiträge: 132
Wohnort: hamburg
|
 jentowncity Verfasst am: 04. Mai 2008 18:08 Titel: jentowncity Verfasst am: 04. Mai 2008 18:08 Titel: |
 |
|
Danke para!
Über die Entropie versteh ich das jetzt auch viel besser.
Also wenn man die Ausdrücke jetzt integriert, die du dahin geschrieben hast, ergibt sich:
=C_{2}\cdot \ln\left (\frac{T_{2}}{T_{0}}\right )) und aufgelöst ergibt das: und aufgelöst ergibt das:

Ist es soweit korrekt?
Und als Arbeit, die die Maschine geleistet hat ergibt sich doch die Differenz der Wärmemengen, oder nicht? Es geht ja keine Energie verloren beim Carnot-Prozess. Das wäre dann:
-C_{2}(T_{0}-T_{2}))
Kannst du dem zustimmen? |
|
 |
para
Moderator

Anmeldungsdatum: 02.10.2004
Beiträge: 2874
Wohnort: Dresden
|
 para Verfasst am: 04. Mai 2008 19:08 Titel: para Verfasst am: 04. Mai 2008 19:08 Titel: |
 |
|
| jentowncity hat Folgendes geschrieben: | | Kannst du dem zustimmen? |
Kurz: ja. :)
_________________
Formeln mit LaTeX |
|
 |
jentowncity
Anmeldungsdatum: 08.05.2005
Beiträge: 132
Wohnort: hamburg
|
 jentowncity Verfasst am: 04. Mai 2008 22:24 Titel: jentowncity Verfasst am: 04. Mai 2008 22:24 Titel: |
 |
|
Vielen Dank für deine Hilfe para  |
|
 |
|


















