| Autor |
Nachricht |
Miseducation
Anmeldungsdatum: 11.08.2016
Beiträge: 1
|
 Miseducation Verfasst am: 11. Aug 2016 08:25 Titel: Mischtemperatur mehrerer Stoffe und Aggregatzustände Miseducation Verfasst am: 11. Aug 2016 08:25 Titel: Mischtemperatur mehrerer Stoffe und Aggregatzustände |
 |
|
Meine Frage:
Ich habe eine Thermobox, 24 l Inhalt. Diese sei ideal dicht, also keine Wärmeverlust über die Wände.
In diese Thermobox tue ich 2 kg Eis mit -10°C, 6 Flaschen Bier (alkoholfrei, also spez. Wärmek. = Wasser). und möchte nun die Misch- bzw. Gleichgewichtstemperatur ausrechnen.
M Bierflasche = 0,39 kg
TLuft = 20°C
TBier + TFlasche = 30°C
spez. Wärmekapazitäten aus Formelsammlung
Meine Ideen:
Die Richmannsche Mischungsregel geht ja nicht, da verschiedene Stoffe und Aggregatzustände. Ich habe also als Grundlage angenommen:
Qab = Qzu (also abgegebene gleich aufgenommener Wärme)
Qab: QEis + QSchmelz + QWasser - Eis schmilzt (-10 bis 0°C), taut 0°C He aus Formelsammlung, Eiswasser erwärmt sich
Qzu: QBier + QGlas + Qluft
Dan ergibt sich eine ziemlich lange Formel auf Basis Qx=Cx*Mx*(To-Tm) für Qab und Qy=Cy*My*(Tm-To) für Qzu
das dann ausmultipliziert und nach Tm umgestellt und ausgerechnet gibt bei mir -53 °C, was ja nich stimmen kann. |
|
 |
GvC
Anmeldungsdatum: 07.05.2009
Beiträge: 14861
|
 GvC Verfasst am: 11. Aug 2016 09:32 Titel: GvC Verfasst am: 11. Aug 2016 09:32 Titel: |
 |
|
|
Du hast zwar die Masse einer Bierflasche angegeben, nicht aber deren Inhalt. Von wieviel Bier reden wir denn? |
|
 |
GvC
Anmeldungsdatum: 07.05.2009
Beiträge: 14861
|
 GvC Verfasst am: 11. Aug 2016 10:58 Titel: GvC Verfasst am: 11. Aug 2016 10:58 Titel: |
 |
|
| Miseducation hat Folgendes geschrieben: | | ... das dann ausmultipliziert und nach Tm umgestellt und ausgerechnet gibt bei mir -53 °C, was ja nich stimmen kann. |
... weil Du wegen falscher Annahmen die Formel falsch angewendet hast. Mal abgesehen davon, dass Du Qab und Qzu verwechselst, woher weißt Du denn, dass das gesamte Eis schmilzt? Es könnte doch genauso gut sein, dass Flaschen samt Inhalt bereits auf 0°C abgekühlt sind, bevor alles Eis geschmolzen ist. Ob Das der Fall ist oder der Fall sei kann, kannst Du durch eine grobe Abschätzung feststellen: Wieviel Energie geben Flaschen samt Inhalt ab, wenn sie auf 0°C abgekühlt werden? Wieviel Energie könnte das Eis aufnehmen, wenn es vollständig geschmolzen ist? Wenn Du von einer Biermenge von 3 l ausgehst (6 Halbliter-Flaschen), wirst Du feststellen, dass das Bier samt Flaschen gar nicht in der Lage ist, das gesamte Eis zu schmelzen. (Die Luft lasse ich für diese Abschätzung mal außen vor, ihr Beitrag ist sowieso sehr gering.) Die sich einstellende "Mischtemperatur" wird also 0°C sein. |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 11. Aug 2016 12:38 Titel: franz Verfasst am: 11. Aug 2016 12:38 Titel: |
 |
|
Eine Frage am Rande, GvC
| Zitat: | | Es könnte doch genauso gut sein, dass Flaschen samt Inhalt bereits auf 0°C abgekühlt sind, bevor alles Eis geschmolzen ist. Ob Das der Fall ist oder der Fall sei kann, kannst Du durch eine grobe Abschätzung feststellen |
Das Schmelzen von Eis tritt ja bei vielen Fragen auf und ich habe es bisher ähnlich, also schrittweise, gehandhabt. Gibt es dafür eigentlich (für einen ausreichend großen Kreis von Aufgaben) eine allgemeine / "elegante" Lösung?
 |
|
 |
GvC
Anmeldungsdatum: 07.05.2009
Beiträge: 14861
|
 GvC Verfasst am: 11. Aug 2016 17:46 Titel: GvC Verfasst am: 11. Aug 2016 17:46 Titel: |
 |
|
| franz hat Folgendes geschrieben: | | Das Schmelzen von Eis tritt ja bei vielen Fragen auf und ich habe es bisher ähnlich, also schrittweise, gehandhabt. Gibt es dafür eigentlich (für einen ausreichend großen Kreis von Aufgaben) eine allgemeine / "elegante" Lösung? |
Meiner Meinung nach ist der eleganteste Weg zur Lösung immer, die Aufgabe zu verstehen, sich also die Mechanismen vorzustellen, die ablaufen oder ablaufen könnten. Dann kommt man ohne Weiteres zu der von mir vorgestellten und von Dir ähnlich gehandhabten Vorgehensweise. Ist Dir das nicht elegant genug? |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 11. Aug 2016 21:42 Titel: franz Verfasst am: 11. Aug 2016 21:42 Titel: |
 |
|
OT
| GvC hat Folgendes geschrieben: | | Ist Dir das nicht elegant genug? |
Stimmt ... Die Bierkühlung bedarf wohl doch keiner "Weltformel" 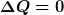 oder so. oder so.  |
|
 |
|
|

















