| Autor |
Nachricht |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 26. Nov 2010 09:58 Titel: Berechnen von Energie zur Erwärmung von Luft ruri14 Verfasst am: 26. Nov 2010 09:58 Titel: Berechnen von Energie zur Erwärmung von Luft |
 |
|
Meine Frage:
Wie viel Enerie braucht man um 1 m³ Luft um 1°C zu erwärmen? Wie stark würde sich 1 m³ Luft innerhalb einer Stunde erwärmen, wenn ein Energiestrom von 400 W zugeführt wird?
Meine Ideen:
Ich muss einige solcher Aufgaben machen. Leider kappier ich hier die eine Beispielformel nicht und kann mir kJ und so leider nichts anfangen.
Vielleicht kann mir da jemand helfen wie ich sowas rechne und was das eigentlich alles soll.
Internet erklärungen und die ERklärung im Buch verstehe ich leider nicht.
Wäre echt total lieb!!
Danke! |
|
 |
TheBartman
Anmeldungsdatum: 09.07.2009
Beiträge: 482
|
 TheBartman Verfasst am: 26. Nov 2010 12:57 Titel: TheBartman Verfasst am: 26. Nov 2010 12:57 Titel: |
 |
|
Zunächst müsstest du mal die Dichte der Luft bei "Startbedingungen" (Temperatur, Druck) wissen. Damit errechnest du die Masse von 1 m3.
Und dann hat ein schlauer Mensch die "spezifsiche Wärmekapazität" mit dem Formelzeichen c erfunden. Diese gibt an, wieviel Energie du benötigst, um 1 kg eines Stoffes (in diesem Fall Gemisch) úm 1 K zu erwärmen. Sie hat die Einheit kJ/(kg * K).
Üblicherweise sind solche Werte aber gegeben, insbesondere, da sie von den Bedingungen abhängen.
Für Teil 2 musst du wissen, dass 1 Joule = 1 Watt * Sekunde. Dann müsstest du deine 400 W mit 3600 s multiplizieren um die zugeführte Wärmeenergie zu erhalten. Diese müsstest du dann anhand der spez. Wärmekapazität umrechnen.
Bringt dich das ein bisschen auf die Sprünge?
_________________
http://www.ultimatespaceproject.de |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 26. Nov 2010 13:06 Titel: ruri14 Verfasst am: 26. Nov 2010 13:06 Titel: |
 |
|
| TheBartman hat Folgendes geschrieben: | Zunächst müsstest du mal die Dichte der Luft bei "Startbedingungen" (Temperatur, Druck) wissen. Damit errechnest du die Masse von 1 m3.
Üblicherweise sind solche Werte aber gegeben, insbesondere, da sie von den Bedingungen abhängen.
Für Teil 2 musst du wissen, dass 1 Joule = 1 Watt * Sekunde.
Bringt dich das ein bisschen auf die Sprünge? |
ich habe alles angegeben was da stand... |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 26. Nov 2010 13:20 Titel: ruri14 Verfasst am: 26. Nov 2010 13:20 Titel: |
 |
|
so muss jetzt leider kochen gehen.
Bin am Sonntag wieder da..
bye  |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 28. Nov 2010 09:30 Titel: ruri14 Verfasst am: 28. Nov 2010 09:30 Titel: |
 |
|
so, bin wieder da und würde mich freuen wenn hier jemand weitermachen könnte.
Danke! |
|
 |
bugs bunny
Gast
|
 bugs bunny Verfasst am: 28. Nov 2010 10:55 Titel: bugs bunny Verfasst am: 28. Nov 2010 10:55 Titel: |
 |
|
|
Hast du schon so was wie eine Formel? |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 28. Nov 2010 11:00 Titel: ruri14 Verfasst am: 28. Nov 2010 11:00 Titel: |
 |
|
nein, wie gesagt, das ist die Aufgabe und fertig. mehr habe ich dazu nicht.
LEIDER! |
|
 |
bugs bunny
Gast
|
 bugs bunny Verfasst am: 28. Nov 2010 11:12 Titel: bugs bunny Verfasst am: 28. Nov 2010 11:12 Titel: |
 |
|
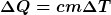
Es gibt 2 einfache Fälle für c
1.Volumen bleibt konstant cv
2.Druck bleibt konstant cp |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 28. Nov 2010 11:30 Titel: ruri14 Verfasst am: 28. Nov 2010 11:30 Titel: |
 |
|
sorry, so eine gleichung wurde in meinem Buch schonmal aufgeführt, ich habe aber keine Ahnung was die Zeichen bedeuten.
Über haupt die ganzen berechnungs Zeichen die ich hier habe kenne ich nicht.
(Hatte letztes Jahr Bücher von einer anderen SChule udn da kam sowas nicht vor.) |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 29. Nov 2010 09:13 Titel: ruri14 Verfasst am: 29. Nov 2010 09:13 Titel: |
 |
|
hallo, vielleicht kann mir hier jemand anderes nochmal weiterhelfen???
Freue mich!
Danke! |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 30. Nov 2010 10:36 Titel: ruri14 Verfasst am: 30. Nov 2010 10:36 Titel: |
 |
|
| ruri14 hat Folgendes geschrieben: | hallo, vielleicht kann mir hier jemand anderes nochmal weiterhelfen???
Freue mich!
Danke! |
Bitte... |
|
 |
o~O
Gast
|
 o~O Verfasst am: 30. Nov 2010 10:54 Titel: o~O Verfasst am: 30. Nov 2010 10:54 Titel: |
 |
|
Ohje da herrscht ja starke Verwirrung ^^ Da kram ich mal mein Wissen von Technischer Thermodynamik aus dem Studium wieder aus ^^
ok erstmal zu erstens:
V = 1m³; DeltaT = 1°C = 1K (Temperaturdifferenzen gibt man normalerweise immer im Kelvin an)
ok nehmen wir an das ganze findet unter Normdruck statt, das nimmt man meistens an wenn nichts weiter gegeben ist. Dann gilt
p * V = m * R * T (ideale Gasgleichung) gilt für gewöhnlich bei umgebungsbedingungen; R ist die spezifische Gaskonstante für Luft, steht in jedem Tafelwerk
daraus folgt
frac{P*V}{R*T} = m also schonmal die Masse die du brauchst.
nun gilt : Q = m * cp * Delta T also Masse * isobare Wärmekapazität * Temperaturdifferenz
cp ist eine komplexe Zahl, die sich nicht einfach berechnene lässt. Würde zu weit führen das zu erklären. Schau aber mal in dein Tafelwerk da steht bestimmt ein Näherungswert für cp für Luft. Ansonsten kann man auch machen aber das ist schon ein bischen Insider Wissen: cp = \frac{Kappa}{Kappa - 1} * R; wobei Kappa = 1,4 für Luft.
Damit hast du schonmal die Energie.
2tens wurde schon richtig erklärt.
Q = Q' * t also Leistung ist Wärmestrom*zeit
Q = 400W * 3600s
Aber nun muss ich eigentlich passen, denn in der aufgabe steht 1m³ dieser hat aber eine andere Masse wenn er sich erwärmt. Einzige Idee die ich hätte wäre, du nimmst an die Masse gleich bleibt. Dann wäre
Delta T = \frac{Q}{m*cp} aber wie gesagt, eigentlich geht das so nicht.
p.s. Fragen ist ja ok wenn man nicht weiter kommt, aber selber Grübeln bringt mehr Erkenntniss  |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 30. Nov 2010 11:02 Titel: ruri14 Verfasst am: 30. Nov 2010 11:02 Titel: |
 |
|
so, vielleicht können wir das in kleinen Schritten machen, da ich überhaupt kein Hintergrundwissen habe.
also du hast geschrieben:
V = 1m³; DeltaT = 1°C = 1K (Temperaturdifferenzen gibt man normalerweise immer im Kelvin an)
Schon da fangen meine Probleme bei dir an. Ich weiß nich für was V steht. WEiß nicht für was DeltaT steht und was K ist. Vermutlich Kelvin. Habe ich allerdings auch noch nie gehört.
Wäre lieb wenn wir das langsam schritt für schritt für einen 8 oder 9. klässler machen könnten.
Danke!!
bye |
|
 |
o~O
Gast
|
 o~O Verfasst am: 30. Nov 2010 11:31 Titel: o~O Verfasst am: 30. Nov 2010 11:31 Titel: |
 |
|
ok, also nun wirds seltsam Oo weil sowas sollte man eigentlich wissen.
ok also V ist das Volumen erkannt man auch an der Einheit 1m³.
Delta T ist die Temperaturdifferenz (Delta also das Dreeick, hab ich nur nicht als Zeichen gefunden).
Thermodynamische Temperaturen gibt man immer in K (Kelvin) an. Da es eine SI-Basisgröße ist. Kelvin ist hierbei die absolute Temperatur, welche bei 0°C einen Wert von 273,15K hat. (Resultiert aus dem Tripelpunkt von Wasser bei 275,16°C, aber das ist ne andere Geschichte)
Da wir an dieser Stelle aber mit dem Differenzen rechnen, ist der Wert von 1°C = 1K Temperaturdifferenz |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 30. Nov 2010 12:06 Titel: ruri14 Verfasst am: 30. Nov 2010 12:06 Titel: |
 |
|
aha. geht das auch ander? ich meine in °C anstatt Kelvin?
Ja dieses Dreieck habe ich in meinem Buch schon gesehen wusste aber nie was es bedeutet.
gut und V ist volumen. gut das hätte ich eigentlch wissen müssen.
gut. weiter. |
|
 |
o~O

Anmeldungsdatum: 30.11.2010
Beiträge: 184
|
 o~O Verfasst am: 30. Nov 2010 12:13 Titel: o~O Verfasst am: 30. Nov 2010 12:13 Titel: |
 |
|
Naja das ist so eine Sache mit dem °C und dem K.
Gelernt habe ich das an sich so:
Temperatur T immer in K
Temperatur Theta immer in °C
Temperaturdifferenzen immer in K
Ich lasse mich da gerne Berichtigen ^^ Aber man sollte sich da schon dran halten, sonst haut auch vielles mit den Einheiten nicht hin. Vorallem bei Rechnungen über den Wärmedurchgang kann man da auf die Nase fallen.
ok Normdruck bzw. Normbedingungen sollte man auch wissen.
Normdruck p = 101,325kPa
R ist die spezifische Gaskonstante, einfach mal im Tafelwerk schauen, das ist normalerweise in jedem irgendwo drin. Ansonsten kann man das auch berechnen in dem man die univierselle Gaskonstante dividiert durch die Molaremasse des Stoffes. |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 30. Nov 2010 12:32 Titel: ruri14 Verfasst am: 30. Nov 2010 12:32 Titel: |
 |
|
nun ich kenne Kelvin bzw. K nicht...
na ja,
in welchem Tafelwerk?
Normdruck... da kann ich mir jetzt leider auch nichts drunter vorstellen.
Sorry wenn da nervt aber Physik ist überhaupt nicht meins...  |
|
 |
o~O

Anmeldungsdatum: 30.11.2010
Beiträge: 184
|
 o~O Verfasst am: 30. Nov 2010 12:44 Titel: o~O Verfasst am: 30. Nov 2010 12:44 Titel: |
 |
|
ohje, ich merk schon da fehlen ein paar Grundlagen 
Naja das bekommen wir hin O_O
ok also Kelvin ist nur eine andere Form die Temperatur darzustellen. °C ist ja auch nur eine Definition des Menschen um sich Temperatur greifbar zu machen. °C ist definiert über den Gefrierpunkt von Wasser bei Umgebnungsdruck wenn ich mich Recht entsinne. Also bei 0°C gefriert Wasser, so wie man sich das gerne mal erzählt. Kelvin geht einen anderen Weg. Kelvin betrachtet das ganze von der Molekularbewegung aus. Bei 0K ist ein Zustand totaler Molekularstoppung erfolgt, also auf gut deutsch da bewegen sich keine Teilchen mehr. Das ist jedoch eine theotischer Grenzfall. Selbst das Weltall hat keine Temperatur von 0K.
So Tafelwerk, denke jedes Sekundarstuffe 1 oder 2 hat sowas, Ansonsten hier mal was ich bei mir so stehen habe
R = 287,1 J/(kg*K); spezifische Gaskonstante für Luft
Thema Normdruck: Kommt eigentlich denke ich aus der Chemie, hat was damit zu tun das man versucht Zustände zu Vergleichen. Um dies zu können musste man Werte festlegen. Hierbei hat man sich geeignigt auf 101,325kPa und 0°C. Siehe auch http://de.wikipedia.org/wiki/Normbedingungen
Darunter vorstellen brauchst du dir nicht viel, das ist halt nur ein Wert der Festgelegt wurde. Aber vielleicht zur Größenordnung. Der barometrische Luftdurck, also jener den du um dich herum hast, liegt in etwa zwischen 98kPa und 101kPa. Hängt ab vom Wetter der geographischen Position und viellem mehr.
Hoffe das bringt ein wenig Licht ins Dunkel.  |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 30. Nov 2010 12:47 Titel: ruri14 Verfasst am: 30. Nov 2010 12:47 Titel: |
 |
|
puh.. ja da fehlt einiges. Kam auch im Buch ganz plötzlich und keinerlei Erklärung wie und was.
nun also ich kann mir da unter nichts so wirklich was vorstellen.
DA bin ich wohl etwas zu blöd für.
DAs ist echt schlimm mit mir aber es will nicht ins Hirn und es ist - so empfinde ich es - total verwirrend.   |
|
 |
o~O

Anmeldungsdatum: 30.11.2010
Beiträge: 184
|
 o~O Verfasst am: 30. Nov 2010 12:54 Titel: o~O Verfasst am: 30. Nov 2010 12:54 Titel: |
 |
|
Naja statt zu weinen lieber aufpassen und lernen 
Vielleicht noch eine Anmerkung zum Delta, damit gibt man normaler Weise immer Differenzen an egal in Welcher Form. Hierbei steht das Delta (Dreieick) für Absolute Differenz. Also z.b: Delta T = T2 - T1
Es gibt noch eine partielle Differenz, aber das führt nun zu weit. Mit dieser gibt man differentiale an welche zum Ableiten oder Integrieren von Funktionen von Interesse sind.
Sonst noch Fragen zu deinen Aufgaben =? |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 30. Nov 2010 13:11 Titel: ruri14 Verfasst am: 30. Nov 2010 13:11 Titel: |
 |
|
nun, wie gesagt, nicht viel kappiert und es hat mich leider auch nicht allzuviel weitergebracht.
Trotzdem Vielen DAnk für deine Mühe und Hilfe!!!
Ich muss jetzt weg, bin aber morgenvormittag wieder da.
Bis bald
ruri!  |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 01. Dez 2010 09:31 Titel: ruri14 Verfasst am: 01. Dez 2010 09:31 Titel: |
 |
|
Also hier nochmal die Aufgabe:
Wie viel Enerie braucht man um 1 m³ Luft um 1°C zu erwärmen? Wie stark würde sich 1 m³ Luft innerhalb einer Stunde erwärmen, wenn ein Energiestrom von 400 W zugeführt wird?
kJ ist eine Energie messung.
Watt ist die Leistung. P steht für die Leistung.
°C ist die Temperatur.
So, vielleicht kann man nochmal ganz von vorne und ganz einfach erstmal eine Gleichung aufstellen?
DAnke!! |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 01. Dez 2010 12:19 Titel: franz Verfasst am: 01. Dez 2010 12:19 Titel: |
 |
|
| ruri14 hat Folgendes geschrieben: | | Wie viel Enerie braucht man um 1 m³ Luft um 1°C zu erwärmen? |
Bei Gasen muß (leider) die (mögliche) Volumenausdehnung berücksichtigt werden. Sind halt drei Variable: p, T, V und man versucht gern (zur besserern Handhabung) eine davon zu "fixieren". Hier also p (isobare Zustandsänderungen) oder V (isochore). Ansage dazu? |
|
 |
ruri14
Anmeldungsdatum: 25.10.2010
Beiträge: 64
Wohnort: Tirol
|
 ruri14 Verfasst am: 01. Dez 2010 12:25 Titel: ruri14 Verfasst am: 01. Dez 2010 12:25 Titel: |
 |
|
geht das nicht auch ohne? Ich habe davon noch nie was gehört.
Einfach nur die Aufgabe machen. |
|
 |
sussymogus
Gast
|
 sussymogus Verfasst am: 27. Okt 2022 14:34 Titel: sussymogus Verfasst am: 27. Okt 2022 14:34 Titel: |
 |
|
| ruri14 hat Folgendes geschrieben: | so muss jetzt leider kochen gehen.
Bin am Sonntag wieder da..
bye  |
Was gabs Bruda?   |
|
 |
|

























