| Autor |
Nachricht |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 05. Jun 2007 19:12 Titel: Mischungsversuche chell Verfasst am: 05. Jun 2007 19:12 Titel: Mischungsversuche |
 |
|
Hallo,
habe hier folgende Aufgabe:
Wie hoch ist die Mischungstemperatur Tm? Es werden 40l heißes Wasser (65°C) und 80l kälteres Wasser (20°C) zusammengeschüttet. Wir haben die Aufgabe dann auch angefangen:
(k steht für kalt, w für warm)
Wk = 4,19 J/g*k * 80kg * (x-20)
Wh = 4,19J/g*k * 80 kg * (65-x)
Was genau sind die beiden Energien? Der Formel nach wären das ja die Energie, die man aufwenden muss, um den jeweiligen Temperaturunterschied zu erwärem. Wofür genau steht das x und wieso muss das x da so stehen?
Danke im Voraus!
chell |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 05. Jun 2007 21:31 Titel: dermarkus Verfasst am: 05. Jun 2007 21:31 Titel: |
 |
|
Magst du mal die Formel, die du da verwendet hast, in allgemeiner Form, also mit Formelzeichen anstatt mit schon eingesetzten Werten, hinschreiben? Gibt dir das schon eine Idee, was das x sein soll?
Beim Mischen wird ja das heiße Wasser abgekühlt und das kalte Wasser erwärmt. Wozu wird die Energie verwendet, die beim Abkühlen des heißen Wassers frei wird?
Magst du die Massen in den beiden Formeln noch einmal daraufhin kontrollieren, ob sie mit den Angaben in der Aufgabenstellung übereinstimmen? |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 06. Jun 2007 06:46 Titel: chell Verfasst am: 06. Jun 2007 06:46 Titel: |
 |
|
Hallo,
also: Mir ist klar, dass ich die Massen noch in Gramm umrechnen muss, um die Aufgabe zu lösen. Und die 80 bei der einen Formel war ein Vertipper ;-) .Es geht ja jetzt auch ums Prinzip. Die allgemeine Formel ist:
W = c * m * dT wobei
c = spezifische Wärmekapazität des Stoffes
m = Masse des Stoffes
dT = Temperaturunterschied, also um wieviel wird der Stoff erwärmt.
Mir ist klar, dass die Differenz am Ende der beiden Formeln dT ist, aber nicht warum und genau wofür da x steht.
Wir die Energie, die beim Abkühlen des heißen Wassers verwendet wird, verwendet, um das kalte Wasser aufzuwärmen? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jun 2007 11:36 Titel: dermarkus Verfasst am: 06. Jun 2007 11:36 Titel: |
 |
|
Mit deiner Formel bin ich einverstanden, ich schlage allerdings vor, den Temperaturunterschied mit 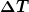 zu bezeichnen, da es sich nicht um einen infinitesimal kleinen Temperaturunterschied dT handelt, sondern einfach um die Differenz zweier Temperaturen. zu bezeichnen, da es sich nicht um einen infinitesimal kleinen Temperaturunterschied dT handelt, sondern einfach um die Differenz zweier Temperaturen.
| chell hat Folgendes geschrieben: |
Wir die Energie, die beim Abkühlen des heißen Wassers verwendet wird, verwendet, um das kalte Wasser aufzuwärmen? |
Genau 
Wie würdest du die Formeln dafür aufstellen, wenn du sie selbst mit den Bezeichnungen hinschreiben magst, die du verwenden möchtest (du brauchst dafür kein x zu verwenden) ? |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 06. Jun 2007 14:58 Titel: chell Verfasst am: 06. Jun 2007 14:58 Titel: |
 |
|
Hier die Formel, wie ich sie schreiben würde (das mit dem Delta ist mir klar, ich kann nur kein Latex :-( also schreibe ich d. Ich meine damit Delta):
W_kalt = c * m * Energie, die vom warmen Wasser kommt - 20
W_warm = c * m * 65 - Energie, die abgegeben wird ans kalte Wasser |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jun 2007 15:48 Titel: dermarkus Verfasst am: 06. Jun 2007 15:48 Titel: |
 |
|
| chell hat Folgendes geschrieben: | | das mit dem Delta ist mir klar, ich kann nur kein Latex :-( |
Das ist einfacher, als du glaubst  Schau am besten mal in unsere Kurzanleitung hier im Board: Schau am besten mal in unsere Kurzanleitung hier im Board:
http://www.physikerboard.de/topic,128,-latex-und-der-formelsatz-im-board.html
| Zitat: |
W_kalt = c * m * Energie, die vom warmen Wasser kommt - 20
W_warm = c * m * 65 - Energie, die abgegeben wird ans kalte Wasser |
Hoppla, schau mal genau hin, verwechselst du da nicht Energie mit etwas anderem? Welche Einheit haben denn die 20 und die 65, und was sind das also für Größen? Was sagtest du oben, steht da für eine Differenz? |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 06. Jun 2007 15:54 Titel: chell Verfasst am: 06. Jun 2007 15:54 Titel: |
 |
|
|
Oh, das ist ja die Differenz der Temperatur. Die haben wir immer in Kelvin (also K).Nur: Bei dieser Aufgabe gibt's ja zwei Wärmeenergien. Woraus besteht die Differenz da ganz genau? Einmal ja sicherlich aus der Temperatur des Wassers aber woraus noch (in der Formel steht ja nur x, was ist das genau?) |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jun 2007 16:03 Titel: dermarkus Verfasst am: 06. Jun 2007 16:03 Titel: |
 |
|
|
Häng dich mal nicht zu sehr an der fertigen Formel mit dem x auf, und überleg einfach mal, wie du das selber ansetzen würdest. Von welcher Temperatur auf welche Temperatur wird welches Wasser abgekühlt bzw. erwärmt? Schreib das am besten selbst mal als Formeln hin. |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 06. Jun 2007 16:14 Titel: chell Verfasst am: 06. Jun 2007 16:14 Titel: |
 |
|
| dermarkus hat Folgendes geschrieben: | | Häng dich mal nicht zu sehr an der fertigen Formel mit dem x auf, und überleg einfach mal, wie du das selber ansetzen würdest. Von welcher Temperatur auf welche Temperatur wird welches Wasser abgekühlt bzw. erwärmt? Schreib das am besten selbst mal als Formeln hin. |
Ich weiß, dass Wärmeenergie vom warmen Wasser auf das kalte Wasser übertragen wird. Das stimmt oder? Das heißt, dass das kalte Wasser um eine bestimmte Temperatur erwärmt wird und das warme Wasser um eine bestimmte Temperatur kälter wird. Ich weiß auch, dass die vom warmen Wasser abgegeben Wärmeenergie gleich der vom kalten Wasser aufgenommenen Wärmeenergie ist. Daher mein Ansatz:
 ) Dabei weiß ich aber nicht genau, warum minus 20. Das kalte Wasser wird ja erwärmt, wird also wärmer als 20° sein. Dabei weiß ich aber nicht genau, warum minus 20. Das kalte Wasser wird ja erwärmt, wird also wärmer als 20° sein.

<br />
)
Hier ist mir das Minus klar: Das warme Wasser wird von seiner Ausgangstemperatur um eine bestimmte Temperatur erwärmt. Da ja die abgegebene gleich der aufgenommen Wärmeenergie ist und in der Formel x steht (ich versuche mich nicht daran aufzuhängen ;-), müsste ja die Temperatur, um die das warme Wasser kälter wird und die Temperatur um die das kalte Wasser wärmer wird gleich sein.
So wäre mein erster Ansatz. Ich weiß aber wirklich nicht, ob das stimmt. |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jun 2007 16:18 Titel: dermarkus Verfasst am: 06. Jun 2007 16:18 Titel: |
 |
|
Verwechselst du da nicht Temperatur und Temperaturdifferenz?
Das, um was das kalte Wasser erwärmt wird, ist eine Temperaturdifferenz.
Das, worauf das kalte Wasser erwärmt wird, ist die Temperatur, die es nach dem Erwärmen hat.
Und was hat die Temperatur, die das Wasser vorher hat, und die Temperatur, die das Wasser nachher hat, mit der Temperaturdifferenz zu tun? |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 06. Jun 2007 17:31 Titel: chell Verfasst am: 06. Jun 2007 17:31 Titel: |
 |
|
|
Naja, Temperatur nach dem Erwärmen des kalten Wassers - Temperatur vor dem Erwärmen des kalten Wassers = Temperaturdifferenz? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jun 2007 17:34 Titel: dermarkus Verfasst am: 06. Jun 2007 17:34 Titel: |
 |
|
Klar  Magst du das auch so in deine Formeln schreiben? Magst du das auch so in deine Formeln schreiben? |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 06. Jun 2007 17:47 Titel: chell Verfasst am: 06. Jun 2007 17:47 Titel: |
 |
|
 )
So? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jun 2007 17:49 Titel: dermarkus Verfasst am: 06. Jun 2007 17:49 Titel: |
 |
|
Nun bist du auf dem richtigen Weg 
Wie lautet denn die Einheit an der 20, die du da noch vergessen hast?
Und schaffst du es auch, so eine Formel für das warme Wasser aufzustellen? |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 06. Jun 2007 18:24 Titel: chell Verfasst am: 06. Jun 2007 18:24 Titel: |
 |
|
|
Die Einheit ist °C. Okay, nun zu dem warmen Wasser. Das warme Wasser wird ja kühler, da es Wärmeenergie an das kalte Wasser abgibt, das diese benutzt, um sich selber zu erwärmen, oder? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jun 2007 18:49 Titel: dermarkus Verfasst am: 06. Jun 2007 18:49 Titel: |
 |
|
Einverstanden  |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 06. Jun 2007 18:54 Titel: chell Verfasst am: 06. Jun 2007 18:54 Titel: |
 |
|

<br />
)
? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jun 2007 19:04 Titel: dermarkus Verfasst am: 06. Jun 2007 19:04 Titel: |
 |
|
Einverstanden; magst du auch hier darauf achten, die Einheit nicht zu vergessen? Und die Klammern setzen, die hier nötig sind?
Nun sind deine Formeln mit den vielen Worten etwas lang und deshalb ein bisschen unübersichtlich. Magst du statt dessen eine kurze Variablenbezeichnung einführen? Wie sehen die Formeln dann aus ? |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 06. Jun 2007 19:29 Titel: chell Verfasst am: 06. Jun 2007 19:29 Titel: |
 |
|
Okay, sagen wir x sei die Temperatur des kalten Wassers nachdem die Wärmeenergie vom warmen Wasser übertragen worden ist. Dann gilt also:

<br />
W_kalt = c * m * (x - 20)
<br />
)
Jetzt noch ein paar Verständnisfragen/Aussagen:
1. Die Temperatur des warmen Wassers reduziert sich um die Temperatur, um die sich das kalte Wasser erwärmt, weil es Wärmeenergie an das kalte Wasser abgibt. Simmt das so?
2. Das kalte Wasser erwärmt sich um die Temperatur, um die sich das warme Wasser erkaltet, minus seine eigene Temperatur. Wieso hier das minus seine eigene Temperatur? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jun 2007 23:03 Titel: dermarkus Verfasst am: 06. Jun 2007 23:03 Titel: |
 |
|
Die Formel sieht schon fast gut aus, du hast aber immer noch vergessen, die nötigen Einheiten dazuzuschreiben.
In 1. und 2. bin ich nicht einverstanden, denn da hast du des öfteren Temperatur und Temperaturdifferenz und Energie durcheinandergebracht. |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 07. Jun 2007 06:45 Titel: chell Verfasst am: 07. Jun 2007 06:45 Titel: |
 |
|
Hallo,
zu den Einheiten: 65°C und 20°C. Kannst du mir sagen, inwiefern (wo) ich Energie und Temperatur verwechselt habe? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 07. Jun 2007 11:11 Titel: dermarkus Verfasst am: 07. Jun 2007 11:11 Titel: |
 |
|
Hm, eigentlich haben wir das alles oben schon mal besprochen. Magst du mal versuchen, das bisherige so genau zu lesen, dass du dann damit deine Punkte 1. und 2. nochmal neu formulieren kannst?
// edit: Hast du dich vielleicht noch zusätzlich davon verwirren lassen, dass in deinen beiden Gleichungen bisher beide Male m steht, obwohl du zwei verschiedene Sachen damit meinst? Dann solltest du dich vielleicht erst einmal darum kümmern, die Variablenbezeichungen für die beiden Massen so zu wählen, dass man sie unterscheiden kann. |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 07. Jun 2007 17:22 Titel: chell Verfasst am: 07. Jun 2007 17:22 Titel: |
 |
|
Hallo,
ich glaube, es jetzt verstanden zu haben. Stimmt das so:
Wenn ich warmes und kaltes Wasser mische, dann gibt das warme Wasser Wärmeenergie an das kalte Wasser ab. Dadurch wird das kalte Wasser wärmer. In der Formel steht das letzt Stück ja für die Temperaturdifferenz. Das warme Wasser wird kälter, da es Wärmeenergie abgibt. Hier ist also die Differenz: Anfangstemperatur - Mischtemperatur (das ist praktisch die Endtemperatur). Beim kalten Wasser ist es umgekehrt: Hier wird das Wasser erwärmt, es handelt sich bei der Differenz also um die Differenz: Um wieviel ist es erwärmt worden? Die kann man ja berechnen, indem man folgendes bildet: Mischtemperatur - Kaltwassertemperatur. Es sind also insgesamt zwei "Schritte": Warmes Wasser gibt Wärmeenergie ab, es wird kälter (dazu wird Energie gebraucht, das ist das W_warm), das kalte Wasser nimmt die Energie auf und wird wärmer (dazu wird die W_kalt Energie gebraucht). Oder ist W_warm die Energie, die es abgibt und W_kalt die Energie, die es aufnimmt? Für das Rechnen an sich ist das nicht so relevant, aber es geht mir hier um das allgemeine Verständnis. |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 07. Jun 2007 19:58 Titel: dermarkus Verfasst am: 07. Jun 2007 19:58 Titel: |
 |
|
Einverstanden 
Und die Antwort auf deine Fragen hast du eigentlich schon selbst gegeben: Wie heißt die Wärmeenergie, die das warme Wasser abgibt? |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 07. Jun 2007 22:31 Titel: chell Verfasst am: 07. Jun 2007 22:31 Titel: |
 |
|
|
Also ist W_warm die Energie, die benötigt wird zum abgeben oder die Energie, die abgegeben wird (oder beides, weil es vielleicht gleich ist)? Und W_kalt ist dann die Energie, die aufgenommen wird oder die, die zur Aufnahme benötigt wird (oder ist auch das gleich)??? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 07. Jun 2007 23:23 Titel: dermarkus Verfasst am: 07. Jun 2007 23:23 Titel: |
 |
|
|
Ich würde nicht versuchen, das hier mit "benötigt" zu formulieren. Ich habe den Eindruck, du versuchst gerade das Richtige zu sagen. |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 08. Jun 2007 06:46 Titel: chell Verfasst am: 08. Jun 2007 06:46 Titel: |
 |
|
Also ist es die Wärmeenergie, die abgegeben bzw. aufgenommen wird?
Ich frage nur, weil wir früher so Aufgaben hatten: Wieviel Energie wird benötigt um so und so viele Liter Wasser von so und so viel Grad Celsius auf so und so viel Grad Celsius zu erhöhen. Da haben wir nämlich immer die Formel: W = c * m * DT benutzt. Diese setzt man ja auch für den Aufgabentypus ein, um den es hier geht Bei den alten Aufgaben war W dann immer die Energie, die zum erhitzen benötigt wird. Wie ist das nun bei dem aktuellen Aufgabentypus? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 08. Jun 2007 13:33 Titel: dermarkus Verfasst am: 08. Jun 2007 13:33 Titel: |
 |
|
| chell hat Folgendes geschrieben: | | Also ist es die Wärmeenergie, die abgegeben bzw. aufgenommen wird? |
Ja 
Du formulierst das zwar ziemlich knapp, aber ich bin mir ziemlich sicher, dass du das Richtige meinst. |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 08. Jun 2007 13:52 Titel: chell Verfasst am: 08. Jun 2007 13:52 Titel: |
 |
|
Mit Abgeben/Aufnehmen meine ich, dass der wärme Gegenstand Wärmeenergie an den kälteren Gegenstand abgibt, wobei Gegendstand alles sein kann, Wasser, Eisenkugel, ganz egal.
Gibt er eigentlich seine gesamte Wärmeenergie ab? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 08. Jun 2007 20:52 Titel: dermarkus Verfasst am: 08. Jun 2007 20:52 Titel: |
 |
|
| chell hat Folgendes geschrieben: |
Gibt er eigentlich seine gesamte Wärmeenergie ab? |
Überleg mal: Welche Temperatur hat er denn nach dem Abkühlen? |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 08. Jun 2007 21:11 Titel: chell Verfasst am: 08. Jun 2007 21:11 Titel: |
 |
|
|
Nach dem Abkühlen hat er die Endmischtemperatur. Das heißt, er wird um Anfangstemperatur minus Mischtemperatur kälter, er gibt also nicht seine gesamte "Temperatur" ab, also wohl auch nicht seine gesamte Wärmeenergie, richtig? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 08. Jun 2007 21:16 Titel: dermarkus Verfasst am: 08. Jun 2007 21:16 Titel: |
 |
|
Einverstanden 
Schaffst du es inzwischen schon, die Aufgabe sauber zu Ende zu rechnen? |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 08. Jun 2007 23:24 Titel: chell Verfasst am: 08. Jun 2007 23:24 Titel: |
 |
|
Ja. Die Aufgabe hatte ich schon im Unterricht fertig gerechnet, aber noch nicht vollständig verstanden (Ansatz war vorgegeben). Wir haben dann weitere Aufgaben bekommen (in der folgenden Stunde). Auch da hatte ich noch Probleme. Ich habe die Aufgaben dann aber zuhause nachbereitet und dann hat es Klick gemacht. Mein Problem war, dass es um die Temperaturdifferenz geht, also: Um wieiviel ist das Warme kälter, das Kalte wärmer geworden. Weil abgegebene Wärmeenergie gleich aufgenommener ist, kann man diese gleichsetzen (die abgegebene/aufgenommene) Wärmeenergie, und voila!
Noch eine Frage: Wir hatten vorher Aufgaben, da haben wir mit derselben Formel (W = m * c * dT) die Energie ausgerechnet, die benötigt wird um eine bestimmte Menge Wasser von einer bestimmten Temperatur auf eine andere zu erhitzen. Dabei ist W ja die aufgewendete Energie. Wieso ist W bei dem Aufgabentypus mit zwei W's die abgegbene bzw. aufgenommene Energie. Eine Formel für zwei Dinge? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 09. Jun 2007 00:22 Titel: dermarkus Verfasst am: 09. Jun 2007 00:22 Titel: |
 |
|
|
Wenn ich nun eine Aufgabe so formuliere, dass die Energie W die Wärmeenergie ist, die in einen Körper reinmuss, damit er sich um die gewünschte Temperaturdifferenz erwärmt, ist das dann deiner Meinung nach eine dritte Sache? Oder ist hier dreimal dasselbe gemeint? |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 09. Jun 2007 11:25 Titel: chell Verfasst am: 09. Jun 2007 11:25 Titel: |
 |
|
|
Ist bei der W_warm/W_kalt Aufgabe W_kalt nicht die Energie, die ins kalte Wasser muss, damit es sich erwärmt (gemäß der Temperaturdifferenz)? Was ist dann W_warm? Die Energie, die ins warme Wasser, damit...? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 09. Jun 2007 12:45 Titel: dermarkus Verfasst am: 09. Jun 2007 12:45 Titel: |
 |
|
Wieso "ins" Wasser? Ist unser W_warm aus dieser Aufgabe eine Energie, die reingeht oder die rauskommt?
Zuletzt bearbeitet von dermarkus am 09. Jun 2007 13:30, insgesamt einmal bearbeitet |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 09. Jun 2007 13:21 Titel: chell Verfasst am: 09. Jun 2007 13:21 Titel: |
 |
|
|
W_warm überträgt doch Wärmeenergie an W_kalt, oder? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 09. Jun 2007 13:30 Titel: dermarkus Verfasst am: 09. Jun 2007 13:30 Titel: |
 |
|
|
Vorsicht beim Formulieren, was du sagst, ergibt keinen Sinn: Wer überträgt, und was wird übertragen? |
|
 |
chell
Anmeldungsdatum: 19.02.2007
Beiträge: 215
|
 chell Verfasst am: 09. Jun 2007 14:16 Titel: chell Verfasst am: 09. Jun 2007 14:16 Titel: |
 |
|
|
Das warme Wasser überträgt doch Wärmeenergie an das kalte Wasser, oder? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 09. Jun 2007 15:26 Titel: dermarkus Verfasst am: 09. Jun 2007 15:26 Titel: |
 |
|
|
Ja. |
|
 |
|







