| Autor |
Nachricht |
Schelle
Anmeldungsdatum: 21.09.2016
Beiträge: 2
|
 Schelle Verfasst am: 21. Sep 2016 17:13 Titel: Anfangsaktivität einer Po210-Probe Schelle Verfasst am: 21. Sep 2016 17:13 Titel: Anfangsaktivität einer Po210-Probe |
 |
|
Meine Frage:
Hallo. Ich hänge bei einer Aufgabe und komme einfach nicht voran. Diese lautet:
Zum Zeitpunkt t=0 liegen zwei radioaktive Präparate vor: Probe 1 ( 228 Ra mit der Zerfallskonstante k1 = 3,3*10^-9 1/s ) besitzt eine Anfangsaktivität von A01 = 5,2*10^6 1/s. Von der Probe 2 ( 210 Po mit der Zerfallskonstate k2 = 5,8*10^-8 1/s ) liegen 8 µg vor.
a. Welche Anfangsaktivität hat die 2. Probe?
b. Nach welcher Zeit ist die Aktivität beider Proben gleich groß, wenn der weitere Zerfall von Tochterkernen vernachlässigt wird?
Meine Ideen:
Mein Ansatz: Ich gehe mal stark davon aus, dass k eigentlich Lambda sein soll. Somit habe ich den Zusammenhang zur Halbwertszeit. Formel ist mir bekannt. Desweiteren habe ich die Formeln für die Aktivität ( https://de.wikipedia.org/wiki/Aktivität_(Physik) ). Jetzt habe ich versucht N(t) zu bestimmen, um es freudig in die Formel einzusetzen (mit Lambda multiplizieren) und komme leider nicht auf die Lösung der Teilaufgabe a. (1,33*10^9 1/s)
Ich bräuchte irgendwie einen Ansatz. Weiterhin weiß ich nicht, wie t im Exponenten in die ganze Sache involviert ist, kann ja nicht 0 sein. Vielen Dank! |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 21. Sep 2016 17:21 Titel: franz Verfasst am: 21. Sep 2016 17:21 Titel: |
 |
|
Der Zusammenhang von A und N ist bekannt, insbesondere von A(0) und N(0)?
Wenn nicht: Kennst Du N(t)? A(t) := -dN(t)/dt = ...
Es fehlt also N_2(0), gegeben m_2(0). Wie hängen Teilchenzahl und Masse bei Po210 zusammen?
Bei mir \approx 3{,}82\cdot 10^{-9}\ s^{-1}) , egal. , egal. |
|
 |
Schelle
Anmeldungsdatum: 21.09.2016
Beiträge: 2
|
 Schelle Verfasst am: 21. Sep 2016 18:10 Titel: Schelle Verfasst am: 21. Sep 2016 18:10 Titel: |
 |
|
|
Hmm also: die Teilchenzahl berechnet sich aus Stoffmenge und Avogadrozahl. Die Stoffmenge habe ich nicht. Die kann allerdings aus m/M berechnet werden, wo mir ja das M fehlt. Ansonsten sind mir die Zusammenhänge bekannt ja. |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 21. Sep 2016 20:40 Titel: franz Verfasst am: 21. Sep 2016 20:40 Titel: |
 |
|
Die Molmasse ist eher Handwerkszeug der Chemiker, also der Mittelwert der in der Erdrinde vorkommenden Isotope des betreffenden Elementes. Genauer arbeitet man vermutlich mit der Originalmasse eines Atomkerns von Po210: hier, rechts oben "Po" eingeben und dann Po210 antippen. Die Einheit 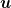 ist geläufig? Und daraufhin mit ist geläufig? Und daraufhin mit  die gesuchte A_2(0) berechnen ... die gesuchte A_2(0) berechnen ...
 |
|
 |
|
|




