| Autor |
Nachricht |
kians
Anmeldungsdatum: 21.06.2007
Beiträge: 109
|
 kians Verfasst am: 29. Jun 2007 22:11 Titel: Entropieänderung kians Verfasst am: 29. Jun 2007 22:11 Titel: Entropieänderung |
 |
|
hi
ich habe eine Frage :
die Entropieänderung ist ja
deltaS = dQ / T
isotherme wäre dQ = - dW
du ist null.
kann ich nun mit dQ= cp * m * dT rechnen
oder muss ich mit - p dv rechnen ?
ich könnte doch beides oder ?
gleiche frage so isobar
du = dQ + dw
hier gilt ja nun alles :
also dq = du + dw
muss ich nun für dQ = cp * m * dt + p dv einsetzen
oder kann ich nur mit dQ= cp * m * dT rechnen ? |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 30. Jun 2007 05:58 Titel: dermarkus Verfasst am: 30. Jun 2007 05:58 Titel: |
 |
|
Das 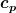 bezieht sich auf die Enthalpieänderung, also bezieht sich auf die Enthalpieänderung, also

und
 ; ;
die Enthalpie 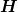 ist ist

und damit ist für konstanten Druck )
 . .
Das heißt, man muss mit

rechnen  |
|
 |
kians
Anmeldungsdatum: 21.06.2007
Beiträge: 109
|
 kians Verfasst am: 30. Jun 2007 12:44 Titel: kians Verfasst am: 30. Jun 2007 12:44 Titel: |
 |
|
ich habs ausprobiert
mann kann sowohl aus auch
steht ja auch ein = dazwischen
a = b also ist b = a
wenn ich es mit dQ= cv m dt rechne oder mit p dv
kommt das selbe ergebnis raus
intressant oder ( bei der beispiel aufgabe die ich habe sollten 5 J / K rauskommen.
mache ich mit DQ = 5,19 J / K mache ich es mit p dv = 5,21 j / K
da eh gerundet wird .... :-) |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 30. Jun 2007 16:30 Titel: dermarkus Verfasst am: 30. Jun 2007 16:30 Titel: |
 |
|
| kians hat Folgendes geschrieben: |
wenn ich es mit dQ= cv m dt rechne oder mit p dv
kommt das selbe ergebnis raus
|
Das wundert mich aber sehr. Kann es sein, dass es dann in der Beispielaufgabe, die du hier noch nicht gezeigt hast, gar nicht um einen isothermen Vorgang geht?
Denn für einen isothermen Vorgang ist ja dT=0, und damit würde ja bei deiner einen Berechnung "mit dQ= cv m dT" Null herauskommen müssen, und bei der Rechnung "mit p dV" nicht, also wäre das sicher nicht das gleiche.
---------------------------------------------------------------------
Oder kann es sein, dass die Beispielaufgabe, die du da gerade gerechnet hast, von etwas ganz anderem als einer isobaren und isothermen Volumenänderung handelt, so dass sie nichts mit dem zu tun hat, was du oben gefragt hattest?
Warum verwendest du nun plötzlich cv statt c_p beim Rechnen? Oder hast du dich da einfach nur vertippt?
Ich glaube, falls du diese offenen Fragen und Unstimmigkeiten noch hier klären möchtest, dann müsstest du unbedingt mal die gesamte wörtliche Aufgabenstellung hier zeigen, die du da gerade bearbeitest, sonst können wir nicht erraten, was du meinst. |
|
 |
kians
Anmeldungsdatum: 21.06.2007
Beiträge: 109
|
 kians Verfasst am: 30. Jun 2007 17:38 Titel: kians Verfasst am: 30. Jun 2007 17:38 Titel: |
 |
|
vertippen , ist mein Hobby :-) klar habe ich mich vertippt.
nun ich sage dir nur eins
ich habe mehrere aufgaben zur thermodynamik und diese die ich berechnet habe war eine isotherme expansion
DT= konstant !! und DU = 0 ebenfalls !!
aber
Ds ( entropie ) = Dq / T T und nicht dT
und laut energieerhaltungssatz
Du = dq + dw
ist dann dq = - dw
und ob ich mit -p dv für dw rechne oder mit cp m * dT
es kommt die selbe zahl raus [/b] |
|
 |
kians
Anmeldungsdatum: 21.06.2007
Beiträge: 109
|
 kians Verfasst am: 30. Jun 2007 17:42 Titel: kians Verfasst am: 30. Jun 2007 17:42 Titel: |
 |
|
laut theorie ist es richtig
DQ = -Dw also - p dv
p = m R T / V
oder DQ = cp m dt
a= b b=a
und aufgabe hin und her es passt
mach doch selbst ein beispiel
z.B. ( ausgedacht )
V1 = 5l V2 = 6 L P1 = 5 pa , P2 = 6 pa
so T = 300 K constant
cp = von helium z.b.
cv = ebenfalls
R = cp - cv
oder = p * v = m R T
also R = p * v / m * t
oder rechne es mit der masse von 1 mol helium also 4 g und Rn universelle |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 30. Jun 2007 18:02 Titel: dermarkus Verfasst am: 30. Jun 2007 18:02 Titel: |
 |
|
Entschuldige, aber ich habe immer noch nicht erraten können, was die Aufgabenstellung der Aufgabe war, von der du sprichst. Magst du sie nicht einfach hier mal wörtlich aufschreiben?
-------------------------
Wenn es darin um eine isotherme Expansion ging, dann ist nicht nur dT = konstant, wie du schreibst, sondern sogar dT = 0 , und damit ist es überhaupt nicht egal, wie man sein dQ ausrechnet.
Kannst du vielleicht am besten zusätzlich zur genauen Aufgabenstellung mal komplett aufschreiben, wie du diese Aufgabe gerechnet hast? Denn sonst kann ich glaube ich nicht erraten, was du meinst, und ob das, was du überlegt und gerechnet hast, richtig ist, inwiefern es richtig gemeint ist, und wo da eventuell irgendwo ein Fehler drinstecken könnte. |
|
 |
kians
Anmeldungsdatum: 21.06.2007
Beiträge: 109
|
 kians Verfasst am: 30. Jun 2007 19:19 Titel: kians Verfasst am: 30. Jun 2007 19:19 Titel: |
 |
|
| Zitat: | Wenn es darin um eine isotherme Expansion ging, dann ist nicht nur dT = konstant, wie du schreibst, sondern sogar dT = 0 , und damit ist es überhaupt nicht egal, wie man sein dQ ausrechnet.
|
isotherme expansion
p zu v propotinal
T = konstant entweder 273 K oder 500 K oder oder oder.
aber nicht = 0 !!!
ISO THERME: bei konstanter Temperatur
somit wäre die innere Energie des Systems = 0 ! dU
also da kann ich nicht zustimmen |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 30. Jun 2007 23:08 Titel: dermarkus Verfasst am: 30. Jun 2007 23:08 Titel: |
 |
|
Schau mal auf den Unterschied zwischen T und dT:
Bei einer isothermen Expansion ist die Temperatur T in der Tat konstant, aber die Temperaturänderung dT ist null. |
|
 |
kians
Anmeldungsdatum: 21.06.2007
Beiträge: 109
|
 kians Verfasst am: 01. Jul 2007 13:35 Titel: kians Verfasst am: 01. Jul 2007 13:35 Titel: |
 |
|
dt = t2 - t1
okay ich sag ja nichts
trotzdem ist es rechenbar
du = 0 dt = 0 T = konstant
also
dQ = cp * m* dt / T bei dt = 0
oder Dq = p dv / T
m R T / V * T und T kann man kürzen .
trotzdem kommt da das selbe raus !!! |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 01. Jul 2007 13:48 Titel: dermarkus Verfasst am: 01. Jul 2007 13:48 Titel: |
 |
|
| kians hat Folgendes geschrieben: |
dQ = cp * m* dt / T bei dt = 0
|
2 Tipps:
1) Warum teilst du in deiner Formel für dQ durch das T? Heißt die Formel, die du meinst, nicht
 ? ?
Durch T teilst du ja erst später, wenn du aus dem dQ die Entropie ausrechnen möchtest.
2) Bekommst du nicht auch dQ = 0 heraus, wenn du dT = 0 einsetzt? Ist nicht "irgendwas mal Null" immer gleich null? |
|
 |
kians
Anmeldungsdatum: 21.06.2007
Beiträge: 109
|
 kians Verfasst am: 05. Jul 2007 20:08 Titel: kians Verfasst am: 05. Jul 2007 20:08 Titel: |
 |
|
ds = dq / T
habe mich vertan , wie immer bist du doch schon von mir gewohnt |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 05. Jul 2007 21:23 Titel: dermarkus Verfasst am: 05. Jul 2007 21:23 Titel: |
 |
|
|
Und was meinst du zu 2) ? |
|
 |
kians
Anmeldungsdatum: 21.06.2007
Beiträge: 109
|
 kians Verfasst am: 05. Jul 2007 21:49 Titel: kians Verfasst am: 05. Jul 2007 21:49 Titel: |
 |
|
mensch ,
 also also  isotherme : du = 0 isotherme : du = 0
und laut Dq= du + dw
ist nun dq = du
also entweder kann ich mit
cp*m * dt oder mit cv* m * dt rechnen
beiden fällen ist dt = 0
aber DQ= dQ / T und T= konstant ! |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 06. Jul 2007 03:44 Titel: dermarkus Verfasst am: 06. Jul 2007 03:44 Titel: |
 |
|
Entschuldige, aber in dem, was du da gerade geschrieben hast, sind sinnentstellende Tippfehler drin, und es scheint mir nichts mit 2) zu tun zu haben. Ich stelle meine Frage neu: Bist du mit dem Folgenden einverstanden?
Bei einer isothermen Expansion ist
 und damit und damit  , ,
denn bei einem isothermen Vorgang ändert sich die Temperatur nicht.
Außerdem ist bei einer isothermen Expansion

denn alle zugeführte Wärmeenergie wird als Expansionsarbeit wieder abgeführt.
Also darf man bei einer isothermen Expansion nicht mit der Gleichung

rechnen, weil deren linke Seite ungleich Null ist, während die rechte Null ist. |
|
 |
kians
Anmeldungsdatum: 21.06.2007
Beiträge: 109
|
 kians Verfasst am: 06. Jul 2007 20:13 Titel: kians Verfasst am: 06. Jul 2007 20:13 Titel: |
 |
|
|
die firma dankt !!!!!! |
|
 |
|

















 also
also  isotherme : du = 0
isotherme : du = 0