| Autor |
Nachricht |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 16. Jul 2017 20:15 Titel: Thermische Zustandsgleichung Temperatur und Druck Änderung Silver1 Verfasst am: 16. Jul 2017 20:15 Titel: Thermische Zustandsgleichung Temperatur und Druck Änderung |
 |
|
Hallo zusammen ich schreibe bald meine Prüfung und der Professor gibt nicht mal nur Ergebnisse raus damit ich vergleichen kann..
Jetzt gerade habe ich ein Problem mit dem Aufgabentyp 6 (Thermische Zustandsgleichung) Ich weiß nicht richtig wie ich bei solchen Aufgaben vorgehen muss..
Aufgabe 6 (Thermische Zustandsgleichung)
Ein ideales Gas im Zustand p0=1bar und T0=270
C wird a) isobar und b) isotherm auf
die Hälfte seines Ausgangsvolumens komprimiert.
Wie ändert sich a) die Temperatur bzw. b) der Druck des Gases?
Hinweis: 𝑝𝑉 = 𝑁𝑅𝑇, R=8,314 J/molK
Da N nicht angegeben ist kann ich ja auch kein Volumenausrechnen oder ?
und später bei den Temperaturen wird ohne die Konstante das ganze auch schwierig ..
Hilfe bitte. |
|
 |
Bloejobb
Gast
|
 Bloejobb Verfasst am: 17. Jul 2017 07:15 Titel: Bloejobb Verfasst am: 17. Jul 2017 07:15 Titel: |
 |
|
Isobar V/T=const.
Isotherm V1/V2=p2/p1
Das n hebt sich in der Rechnung auf, sodass man auf diese Gleichungen kommt. |
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 17. Jul 2017 18:38 Titel: Silver1 Verfasst am: 17. Jul 2017 18:38 Titel: |
 |
|
Also für den Isothermen Teil habe ich nun so gerechnet:
Ich habe die Gleichung aufgestellt da die Temperatur ja konstant bleibt :
)
danach habe ich es nach P1 umgestellt:

Ist das soweit richtig ? |
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 17. Jul 2017 18:48 Titel: Silver1 Verfasst am: 17. Jul 2017 18:48 Titel: |
 |
|
Bei dem Isobaren Teil weiß ich jedoch nicht wie man auf die Gleichung kommt
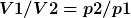 |
|
 |
autor237
Anmeldungsdatum: 31.08.2016
Beiträge: 509
|
 autor237 Verfasst am: 17. Jul 2017 19:51 Titel: autor237 Verfasst am: 17. Jul 2017 19:51 Titel: |
 |
|
Hallo Silver1!
Das Volumen brauchst du nicht explizit zu berechnen. Du weist ja, dass V_1=1/2 V_0 ist. Das hast du ja schon bei Aufgabe b richtig angewendet.
Bei Aufgabe a kannst du dies wieder nutzen. Hier muss allerdings:

gelten.
| Zitat: |
Bei dem Isobaren Teil weiß ich jedoch nicht wie man auf die Gleichung kommt
V1/V2=p2/p1
|
Das ist ja nur die umgestellte Gleichung, die du bei b Verwendet hast
 |
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 17. Jul 2017 19:53 Titel: Silver1 Verfasst am: 17. Jul 2017 19:53 Titel: |
 |
|
Ich habs jetzt Danke !
Aber kann -123 Grad für die Temperatur bei Isobar realistisch sein ?
Mfg. |
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 17. Jul 2017 19:56 Titel: Silver1 Verfasst am: 17. Jul 2017 19:56 Titel: |
 |
|
Und ich hätte noch eine Frage. Ich bearbeite gerade eine Aufgabe wo ein Gas adiabat (isentrop) auf ein Zehntel seines Ausgangsvolumens
komprimiert wird.
Meine Frage ist was genau bedeutet adiabat und inwiefern ändert sich nun meine Vorgehensweise ?
Villeicht hier auch mal die gesamte Aufgabe:
Ein ideales Gas im Zustand p0=1bar und T0=270
C wird adiabat (isentrop) auf ein Zehntel seines Ausgangsvolumens
komprimiert.
Wie ändern sich Temperatur und der Druck des Gases?
Skizzieren Sie den Prozess und typische Isothermen in einem P-V-Diagramm!
Hinweis: 𝑝𝑝 = 𝑁𝑁𝑁, R=8,314 J/molK , 𝑝𝑉𝜅 = 𝑘𝑘𝑘𝑘𝑘., κ=1,4
Danke für eure Hilfe ! |
|
 |
Heribert
Gast
|
 Heribert Verfasst am: 17. Jul 2017 19:57 Titel: Heribert Verfasst am: 17. Jul 2017 19:57 Titel: |
 |
|
Isotherm
-------
Konstant ist T.
Es gilt
p1*v1=nRT und
p2*v2=nRT
Die rechten Seiten der Gleichungen sind identisch, also kann man die linken Teile gleichsetzen:
p1*v1=p2*v2 <=> p1/p2=v2/v1
________________________
Isobar
------
Konstant ist p
Es gilt
p*V1=nRT1 <=> p/(nR)=T1/V1
p*V2=nRT2 <=> p/(nR)=T2/V2
Gleiches Spiel wie oben
T1/V1=T2/V2 |
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 17. Jul 2017 20:11 Titel: Silver1 Verfasst am: 17. Jul 2017 20:11 Titel: |
 |
|
| Heribert hat Folgendes geschrieben: | Isotherm
-------
Konstant ist T.
Es gilt
p1*v1=nRT und
p2*v2=nRT
Die rechten Seiten der Gleichungen sind identisch, also kann man die linken Teile gleichsetzen:
p1*v1=p2*v2 <=> p1/p2=v2/v1
________________________
Isobar
------
Konstant ist p
Es gilt
p*V1=nRT1 <=> p/(nR)=T1/V1
p*V2=nRT2 <=> p/(nR)=T2/V2
Gleiches Spiel wie oben
T1/V1=T2/V2 |
Aber hier kommt doch das Wort adiabat im Spiel und ich meine mich erinnern zu können das man dafür bestimmte Formeln anwenden muss
z.B

Ich weiß nur nicht was genau Adiabat bedeutet und welche Formeln es gibt.
Gibt es auch Isotherm adiabat ? |
|
 |
GvC
Anmeldungsdatum: 07.05.2009
Beiträge: 14861
|
 GvC Verfasst am: 18. Jul 2017 11:50 Titel: GvC Verfasst am: 18. Jul 2017 11:50 Titel: |
 |
|
| Silver1 hat Folgendes geschrieben: | | Aber kann -123 Grad für die Temperatur bei Isobar realistisch sein ? |
Wie kommst Du denn da drauf? |
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 5875
|
 Myon Verfasst am: 18. Jul 2017 12:53 Titel: Myon Verfasst am: 18. Jul 2017 12:53 Titel: |
 |
|
|
Das wäre richtig, nur ist T0=270 K und nicht 300 K. |
|
 |
Silver1
Anmeldungsdatum: 16.07.2017
Beiträge: 31
|
 Silver1 Verfasst am: 18. Jul 2017 12:57 Titel: Silver1 Verfasst am: 18. Jul 2017 12:57 Titel: |
 |
|
| Myon hat Folgendes geschrieben: | | Das wäre richtig, nur ist T0=270 K und nicht 300 K. |
Aber T0 ist 27 Grad und von Grad in Kelvin ist doch 273 + Grad oder nicht ? |
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 5875
|
 Myon Verfasst am: 18. Jul 2017 13:14 Titel: Myon Verfasst am: 18. Jul 2017 13:14 Titel: |
 |
|
|
Sorry, hab das in der Aufgabenstellung aufgrund der Formatierung falsch gelesen. Ja, dann ist alles richtig (bei der Umrechnung wären genaugenommen 273.15 zu addieren, aber mit den gegebenen Zahlen ist die Aufgabe wohl so gemeint, dass mit 273 gerechnet werden darf). |
|
 |
autor237
Anmeldungsdatum: 31.08.2016
Beiträge: 509
|
 autor237 Verfasst am: 18. Jul 2017 19:51 Titel: autor237 Verfasst am: 18. Jul 2017 19:51 Titel: |
 |
|
| Silver1 hat Folgendes geschrieben: | Und ich hätte noch eine Frage. Ich bearbeite gerade eine Aufgabe wo ein Gas adiabat (isentrop) auf ein Zehntel seines Ausgangsvolumens
komprimiert wird.
Meine Frage ist was genau bedeutet adiabat und inwiefern ändert sich nun meine Vorgehensweise ?
Villeicht hier auch mal die gesamte Aufgabe:
Ein ideales Gas im Zustand p0=1bar und T0=270
C wird adiabat (isentrop) auf ein Zehntel seines Ausgangsvolumens
komprimiert.
Wie ändern sich Temperatur und der Druck des Gases?
Skizzieren Sie den Prozess und typische Isothermen in einem P-V-Diagramm!
Hinweis: 𝑝𝑝 = 𝑁𝑁𝑁, R=8,314 J/molK , 𝑝𝑉𝜅 = 𝑘𝑘𝑘𝑘𝑘., κ=1,4
Danke für eure Hilfe ! |
hier ein Link:
https://de.wikipedia.org/wiki/Adiabatische_Zustands%C3%A4nderung
die Formeln, die du benötigst sind:
^{k-1})
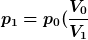^k) |
|
 |
GvC
Anmeldungsdatum: 07.05.2009
Beiträge: 14861
|
 GvC Verfasst am: 19. Jul 2017 13:41 Titel: GvC Verfasst am: 19. Jul 2017 13:41 Titel: |
 |
|
Noch einmal zur ersten Aufgabe. Wie kommst Du darauf:
| Silver1 hat Folgendes geschrieben: | | Aber kann -123 Grad für die Temperatur bei Isobar realistisch sein ? |
Ich habe den Text der Aufgabenstellung
| Silver1 hat Folgendes geschrieben: | Ein ideales Gas im Zustand p0=1bar und T0=270
C wird a) isobar ... auf
die Hälfte seines Ausgangsvolumens komprimiert. |
so interprtiert, dass die Ausgangstemperatur T0=270°C beträgt, also 543K. Was soll sonst das "C" bedeuten? Deine Rechnung mit 300K ist jedenfalls falsch. |
|
 |
|















