| Autor |
Nachricht |
Gast
|
 Gast Verfasst am: 24. Jan 2006 14:20 Titel: Der Unterschied zw. Banden- und Linienspektren Gast Verfasst am: 24. Jan 2006 14:20 Titel: Der Unterschied zw. Banden- und Linienspektren |
 |
|
Hab gegoogelt und auch hier gesucht, aber finde keine Antwort bezüglich des Unterschieds der Wellenlänge...
Bei Linienspektren wird Energie mit EINER bestimmten Wellenlänge abgestrahlt, bei kontinuierlichen Spektren Energie SÄMTLICHER Wellenlängen.
Und wie ist das bei Bandenspektren? Da diese wie die Linienspektren ja diskontinuierlich sind, ist es auch nur EINE wellenlänge? Falls ja, worin besteht der Unterschied?
Vielen Dank schonmal im Voraus! |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 24. Jan 2006 16:22 Titel: dermarkus Verfasst am: 24. Jan 2006 16:22 Titel: |
 |
|
Bandenspektren sind das Mittelding zwischen Linienspektren und kontinuierlichen Spektren.
Ein Bandenspektrum kannst du dir also vorstellen wie ein Linienspektrum mit sehr, sehr, sehr breiten Linien.
So was kommt vor, wenn beispielsweise sehr viele Niveaus sehr nahe beieinanderliegen, so dass sie überlappen, und Licht innerhalb eines gesamten Frequenzbandes (also sämtliche Frequenzen zwischen den beiden Frequenzen an den Rändern des Bandes) ausgestrahlt werden kann. |
|
 |
Enthalpus-Laplacus

Anmeldungsdatum: 02.12.2004
Beiträge: 271
Wohnort: Bavaria
|
 Enthalpus-Laplacus Verfasst am: 24. Jan 2006 16:26 Titel: Enthalpus-Laplacus Verfasst am: 24. Jan 2006 16:26 Titel: |
 |
|
Sers,
ich versuch das mal bündig zusammenzufassen obwohl die Erklärung in die Quantenmechanik führt.
Nach der Heisenberschen Unschärferelation kann der Impuls und der Ort eines Teilchens nicht gleichzeitig exakt bestimmt werden. In diesem Fall handelt es sich um ein Photon.
Neben dieser Relation zwischen Ort und Impuls gibt es noch eine zweite Unschärferelation:
Die Energie des Teilchens kann zu einem exakten Zeitpunkt nicht bestimmt werden.
(Energieunschärfe Relation)
Es gilt:

Beim übergang eines Teilchens vom Zustand mit der Energie E1 in den Zustand mit der Energie E2 wird elektromagnetische Strahlung emmitiert:
Die Teilchen im angeregten Zustand E2 kann man als Sender auffassen.
Die Sendezeit dieser Teilchen ist mit der Relaxationszeit 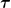 des Engeregten Zustandes verbunden. des Engeregten Zustandes verbunden.
Es gilt:

Das 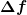 wird als natürliche Linienbreite bezeichnet. wird als natürliche Linienbreite bezeichnet.
Daher existieren keine exakten Linienspektren. Jede Spektrallinie hat eine sogennante Mittenfrequenz bei der die Strahlunsintensität maximal ist. Nach links und rechts nimmt die intensität mit zu bzw. abnehmender Frequenz ab.
Die natürliche Linienbreite ist aber wiederum ein theoretischer Wert der nur für Teilchen ohne jegliche Wechselwirkung gilt. Da dies in der Praxis nicht gegeben ist, wird die Linie zusätzlich verbreitert. Man spricht von Stoß- bzw. Druckverbreiterung.
Daneben unterscheidet man noch homogen und inhomogen verbreiterte Spektrallinien.
Bei den sogenannten Bandenspektren überlagern sich die von Teilchen aus unterschiedlichen Energieniveaus abfallenden Spektrallinien.
Edit:
Das Bandenspektrum ist also aus mehreren überlappenden einzel Spektrallinien zusammengesetzt. Wobei meistens nicht mehr zwischen den einzelnen Linien unterschieden werden kann weil sich die Energieunschärgen addieren. Zudem kommt es zu verschiebungen der Mittenfrequenzen der Linien bestimmter übergänge. Wodurch ein für einen bestimmten Stoff/ Verbindung eigenes Spektrum entsteht.
Über dieses Spektrum lässt sich der Stoff auch eindeutig Identifizieren. (siehe Spektroskopie)
_________________
MfG
Enthalpus |
|
 |
as_string
Moderator

Anmeldungsdatum: 09.12.2005
Beiträge: 5789
Wohnort: Heidelberg
|
 as_string Verfasst am: 24. Jan 2006 16:37 Titel: as_string Verfasst am: 24. Jan 2006 16:37 Titel: |
 |
|
Nicht zu vergessen die Dopplerverbreiterung, die von der thermischen Bewegung der strahlenden Atome kommt. Allerdings gibt es ja heute auch dopplerfreie Spektroskopie...
Gruß
Marco |
|
 |
Enthalpus-Laplacus

Anmeldungsdatum: 02.12.2004
Beiträge: 271
Wohnort: Bavaria
|
 Enthalpus-Laplacus Verfasst am: 24. Jan 2006 16:42 Titel: Enthalpus-Laplacus Verfasst am: 24. Jan 2006 16:42 Titel: |
 |
|
@as_string:
Das wäre ein Beispiel für eine inhomogene Linienverbreiterung. Die ist aber eher bei Gasen vertreten. Denn hier werde aufgrund des statistisch verteilten Richtung der Gasmoleküle die Resonanzfrequenzen der Molekeln verschoben. Daher ist auch das Frequenzverhalten unterschiedlich.
Bei festen Stoffen spielt die Dopplerverbreiterung in der Praxis eher eine untergeordente Rolle da die Dopplerverschiebungen relativ klein sind.
_________________
MfG
Enthalpus |
|
 |
as_string
Moderator

Anmeldungsdatum: 09.12.2005
Beiträge: 5789
Wohnort: Heidelberg
|
 as_string Verfasst am: 25. Jan 2006 03:23 Titel: as_string Verfasst am: 25. Jan 2006 03:23 Titel: |
 |
|
Naja, ich dachte jetzt auch eher an Gase... War die ganze Zeit die Rede von Festkörpern? Da muß ich wohl den Thread nochmal richtig lesen, hab ich glatt übersehen.
Gruß
Marco |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 25. Jan 2006 10:30 Titel: dermarkus Verfasst am: 25. Jan 2006 10:30 Titel: |
 |
|
Weil für Bandenspektren viele Niveaus überlappen müssen, findet man sie bei Molekülen (besonders ausgeprägt bei großen Molekülen) und in Festkörpern.
In solchen Systemen sind nämlich mehrere bis viele Atome miteinander verbunden. Wenn die Energieniveaus dieser Atome in Molekülbindungen oder gar in Festkörpern miteinander koppeln, dann werden aus den einzelnen Niveaus der Atome dabei breite Bänder.
Also hat man typischerweise die Situation, dass in Gasen Linienspektren vorliegen und in Festkörpern Bandenspektren.
@as_string: Ich meine, du hast den Thread schon gut gelesen, das mit den Festkörpern hatte hier bisher noch keiner beschrieben. Danke für die Nachfrage!
Viele Grüße, dermarkus |
|
 |
|















