| Autor |
Nachricht |
Agnodice
Anmeldungsdatum: 16.03.2007
Beiträge: 37
|
 Agnodice Verfasst am: 02. Apr 2007 22:38 Titel: Gefrierpunktserniedrigung/Dampfdruckerniedrigung Agnodice Verfasst am: 02. Apr 2007 22:38 Titel: Gefrierpunktserniedrigung/Dampfdruckerniedrigung |
 |
|
Könnte mir vielleicht bitte jemand Folgendes erklären bzw. hat jemand einen Link für mich, wo ich das nachlesen könnte (habe nämlich gerade kein Physikbuch zur Hand, in dem ich die Antwort auf meine Frage finde):
"Die Gefrierpunktserniedrigung hängt nur vom Lösungsmittel und der Anzahl n der gelösten Teilchen ab und nicht von der gelösten Substanz."
Mit dem Wissen, das ich über Gitterenergie und Solvatationsenergie habe, kommt mir das nämlich etwas seltsam vor...
Außerdem frage ich mich: Wenn ich eine Lösung (Lösungsmittel Wasser+Salz) zum Gefrieren bringe, bildet sich dann eigentlich abgesehen vom Eisgitter auch noch gleichzeitig das Gitter des Salzes (das ja zuvor durch den Lösungsprozess zerstört wurde) aus?
Zuletzt bearbeitet von Agnodice am 03. Apr 2007 10:21, insgesamt einmal bearbeitet |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
|
 |
Agnodice
Anmeldungsdatum: 16.03.2007
Beiträge: 37
|
 Agnodice Verfasst am: 03. Apr 2007 11:45 Titel: Agnodice Verfasst am: 03. Apr 2007 11:45 Titel: |
 |
|
Mh, ich frage mich gerade, was du da in der Praktikumsanleitung der Chemiker herausgelesen hast, was die Antwort auf meine Frage ist?
In der Tat habe ich eine zu meinem Zitat gehörige "Gleichung" unterschlagen, die eher eine Proportion ist. Also nochmal kompletter Textabschnitt:
| Zitat: | Es mag überraschen, soll hier aber ohne weitere Begründung lediglich festgestellt werden: Die Gefrierpunktserniedrigung hängt nur vom Lösungsmittel und der Anzahldichte hängt nur vom Lösungsmittel und der Anzahldichte 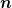 der gelösten Teilchen ab, nicht aber von deren Art, von der gelösten Substanz also: der gelösten Teilchen ab, nicht aber von deren Art, von der gelösten Substanz also:
 . . |
(ich finde hier das Proportionalitätszeichen nicht, sorry).
[\sim ... hab's mal ergänzt, para]
Dasselbe gilt natürlich für die Dampfdruckerniedrigung (habe das deshalb im Titel noch geändert).
Ich fasse also zusammen: Fügt man zu einem Lösungsmittel (am naheliegendsten Wasser) ein Salz hinzu, so ändert sich sowohl die Temperatur, bei der der Smp als auch der Sdp normalerweise liegen (bei reinem Lösungsmittel). Der Smp liegt dann unterhalb Null Grad und der Sdp oberhalb 100 Grad im Falle des Wassers.--
Und zwar umso mehr, je mehr Salz man hinzugibt.
Jetzt dachte ich immer, wenn man NaCl auf Schnee streut, so würde sich das Salzgitter unter Erwärmung lösen und das Eis darunter würde deshalb schmelzen. Aber jetzt bin ich bei dieser Gefrierpunktserniedrigung nochmal ins Schmunzeln gekommen: NaCl löst sich normalerweise in Wasser gar nicht unter Temperaturänderung, da die Gitterenergie ähnlich groß ist wie die Hydratationsenergie. Also wird das wohl tatsächlich nicht am Gitter liegen...  |
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 03. Apr 2007 22:58 Titel: dermarkus Verfasst am: 03. Apr 2007 22:58 Titel: |
 |
|
Grob gesprochen könnte dir vielleicht erstmal folgendes helfen:
In der Flüssigkeit hilft der gelöste Stoff, Energie zu sparen, weil sich die Teilchen des Lösungsmittels um diese gelösten Teilchen anlagern können. In der festen und in der gasförmigen Phase dagegen spart man nichts, weil ja nur das Lösungsmittel gefriert oder verdampft.
Also ist die flüssige Phase energetisch günstiger, also verschiebt sich der Gefrierpunkt nach unten und der Siedepunkt nach oben.
Welche Näherungen hinter dieser Betrachtung stecken, und wie man quantitativ auf Formeln kommt, um das zu beschreiben, steht zum Beispiel in dem Link. |
|
 |
|
|


