| Autor |
Nachricht |
Thejackal
Anmeldungsdatum: 08.09.2009
Beiträge: 7
|
 Thejackal Verfasst am: 09. Sep 2009 11:29 Titel: Clausius-Clapeyron-Gleichung Thejackal Verfasst am: 09. Sep 2009 11:29 Titel: Clausius-Clapeyron-Gleichung |
 |
|
Hi Board,
ich sitze gerade vor einer aufgabe und weiss einfach nicht wie ich die Lösen soll.Ich sag euch mal kurz meinen stand der Dinge:
Aufgabe:
Berechnen Sie mit Hilfe der Formel von Clausius-Clapeyron die Siedetemperatur von Wasser auf der
Celsiusskala bei einem Dampfdruck von p = 7 bar. (Ergebnis: 165 °C)
Gleichung: dp/dt = Delta s/Delta V
Also,dp ist der Druck und dt die ges. Temperatur und Delta V ist das Molare Volumen von 18g/mol.
Ich weiss einfach nichts mit dem Delta s anzufangen und deswegen bitte ich euch um Hilfe. DANKE
mfg Sascha |
|
 |
TheBartman
Anmeldungsdatum: 09.07.2009
Beiträge: 482
|
 TheBartman Verfasst am: 10. Sep 2009 15:32 Titel: TheBartman Verfasst am: 10. Sep 2009 15:32 Titel: |
 |
|
Weiß nicht ob es hilft, aber:
1. Ist das die Clapeyron-Gleichung (ohne Clausius)
2. Delta S ist die molare Entropie
3. Delta V ist das molare Volumen , nicht die molare Masse
Wo du diese Werte aber herbekommst, kann ich dir leider auch nicht sagen. |
|
 |
schnudl
Moderator

Anmeldungsdatum: 15.11.2005
Beiträge: 6979
Wohnort: Wien
|
 schnudl Verfasst am: 10. Sep 2009 17:11 Titel: schnudl Verfasst am: 10. Sep 2009 17:11 Titel: |
 |
|
Das 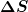 ist die Verdampfungsentropie, welche über die Verdampfungswärme über ist die Verdampfungsentropie, welche über die Verdampfungswärme über

zusammenhängt.
Das ergibt, wenn man das Volumen der Flüssigkeit vernachlässigt:

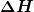 kann man in erster Näherung zunächst als konstant annehmen; aus einer Tabelle aus Wikipedia entnimmt man für Wasser bei T1=100°C/1bar einen Wert von 40,7kJ/mol. kann man in erster Näherung zunächst als konstant annehmen; aus einer Tabelle aus Wikipedia entnimmt man für Wasser bei T1=100°C/1bar einen Wert von 40,7kJ/mol.
Daraus kann man T2 ausrechnen und kommt dabei auf 165°C, wie als Lösung vorgegeben.
_________________
Wenn du eine weise Antwort verlangst, musst du vernünftig fragen (Goethe) |
|
 |
|
|