| Autor |
Nachricht |
annafragt
Anmeldungsdatum: 28.01.2021
Beiträge: 309
|
 annafragt Verfasst am: 30. Aug 2021 16:19 Titel: Gefrierpunktserniedrigung annafragt Verfasst am: 30. Aug 2021 16:19 Titel: Gefrierpunktserniedrigung |
 |
|
Meine Frage:
Hallo zusammen,
Im Anhang (Anhang 1) ist die Gleichung zur Gefrierpunktserniedrigung zu finden, auf die ich mich beziehe.
Ich weiß, dass das delta T für die Gefrierpunktserniedrigung steht, das n für die Stoffmenge der Lösung und das nl für die Stoffmenge des Lösungsmittels. Aber wofür steht das alpha?
Und wie kommt man von dieser Formel (Anhang 1) auf die markierte Formel in Anhang 2 oder haben die Formeln nichts miteinander zu tun?
Meine Ideen:
Vielen Dank schonmal und ganz liebe Grüße
| Beschreibung: |
|
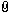
Download |
| Dateiname: |
1255419A-A2DC-4090-825B-0DA34997D48F.jpeg |
| Dateigröße: |
288.36 KB |
| Heruntergeladen: |
168 mal |
| Beschreibung: |
|
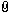
Download |
| Dateiname: |
7078F8D2-E939-4C3B-8FEF-A87D210F8989.jpeg |
| Dateigröße: |
66.34 KB |
| Heruntergeladen: |
99 mal |
|
|
 |
Nobby1
Anmeldungsdatum: 19.08.2019
Beiträge: 1553
|
 Nobby1 Verfasst am: 30. Aug 2021 20:24 Titel: Nobby1 Verfasst am: 30. Aug 2021 20:24 Titel: |
 |
|
|
Das müsste der van't Hoff Faktor sein. Bei KCl ist der 2 bei Glucose 1.
|
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 5891
|
 Myon Verfasst am: 30. Aug 2021 23:18 Titel: Myon Verfasst am: 30. Aug 2021 23:18 Titel: |
 |
|
|
Der Vant Hoff-Faktor wäre dimensionslos, die Konstante alpha hat jedoch nach der Gleichung im Scan die Einheit 1/K. alpha entspricht mehr oder weniger dem Reziprokwert der kryostatischen Konstanten, nur dass die kryostatische Konstante sich auf die Molalität (Verhältnis Stoffmenge gelöster Stoff zu Masse des Lösungsmittels) bezieht, alpha hingegen auf das Verhältnis der Stoffmengen.
|
|
 |
annafragt
Anmeldungsdatum: 28.01.2021
Beiträge: 309
|
 annafragt Verfasst am: 31. Aug 2021 00:23 Titel: annafragt Verfasst am: 31. Aug 2021 00:23 Titel: |
 |
|
Dankeschön.
Ich wollte nur noch fragen, wieso man zur Bestimmung der relativen Molekülmasse einer Unbekannten nicht dissoziierendem Substanz mit der Methode der Gefierpunktserniedrigung nur die Masse der gelösten Substanz benötigt, nicht aber die Schmelztemperatur der gelösten Substanz oder die Kryoskopische Konstante der gelösten Substanz. Vielen Dank nochmal
|
|
 |
Füsik-Gast
Gast
|
 Füsik-Gast Verfasst am: 31. Aug 2021 09:49 Titel: GE Füsik-Gast Verfasst am: 31. Aug 2021 09:49 Titel: GE |
 |
|
Die Gefrierpunktserniedrigung beruht auf den sog. kolligativen Eigenschaften des gelösten Stoffs,diese sind unabhängig von Art der teilchen oder deren genauer WW mit dem Lösungsmittel.
Es kommt nur darauf an,wieviele Teilchen beim Lösen vorliegen.
Daher benötigt du hier weder kryoskopische Konstante(falls überhaupt für KCl oder Glucose vorhanden,da diese dann als Lösungsmittel agieren würden),noch den Schmelzpunkt der gelösten Stoffe.
Füsik-Gast.
|
|
 |
annafragt
Anmeldungsdatum: 28.01.2021
Beiträge: 309
|
 annafragt Verfasst am: 31. Aug 2021 18:54 Titel: annafragt Verfasst am: 31. Aug 2021 18:54 Titel: |
 |
|
Vielen Dank für die Antwort.
Ich verstehe nur noch nicht wie man auf den im Anhang markierten Zusammenhang kommt
Eine Antwort wäre sehr hilfreich danke
| Beschreibung: |
|
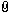
Download |
| Dateiname: |
E7360514-6C39-4D4D-9071-D7549208C7ED.jpeg |
| Dateigröße: |
264.79 KB |
| Heruntergeladen: |
95 mal |
|
|
 |
|
|
