| Autor |
Nachricht |
Jan2000
Gast
|
 Jan2000 Verfasst am: 27. Dez 2020 21:40 Titel: Zersetzung von Dimethylether Jan2000 Verfasst am: 27. Dez 2020 21:40 Titel: Zersetzung von Dimethylether |
 |
|
Meine Frage:
Hallo, hoffe das Ihr mir weiterhelfen könnt. Finde leider keinen Ansatz.
Aufgabe:
Hinshelwood untersuchte die Zersetzung von Dimethylether indem der Gesamtdruck während der Reaktion verfolgt wird. Bestimmen Sie die
Reaktionsordnung und die Geschwindigkeitskonstante.
Zeit/s: 0, 57, 85, 114, 145, 182, 219, 261, 299
p/Torr: 420, 584, 662, 743, 815, 891, 954, 1013, 1054
Meine Ideen:
Wenn man sich die Reaktion anschaut sieht man das es sich um eine Reaktion 1.Ordnung handelt. Leider weiß ich nicht wie man aus den Druckdaten, dies beweisen soll. |
|
 |
Nobby1
Anmeldungsdatum: 19.08.2019
Beiträge: 1553
|
|
 |
Jan2000
Gast
|
 Jan2000 Verfasst am: 27. Dez 2020 22:21 Titel: Jan2000 Verfasst am: 27. Dez 2020 22:21 Titel: |
 |
|
|
Vielen dank für deine Antwort aber leider hilft mir das nicht wirklich da ich nur die 1.Ordnung erraten habe, diese aber belegen muss. |
|
 |
Klimafrosch
Anmeldungsdatum: 12.10.2020
Beiträge: 33
|
 Klimafrosch Verfasst am: 27. Dez 2020 23:45 Titel: Klimafrosch Verfasst am: 27. Dez 2020 23:45 Titel: |
 |
|
Man muss den Druck in eine Konzentration umrechnen und dann eine doppelt-logarithmische Auftragung machen. (Wenn ein Gasteilchen in zwei Gasteilchen zerfällt, dann hat der Druck um ein Gasteilchen zugenommen.)
Dann erhält man immer eine Gerade. Die Steigung der Geraden gibt die Ordnung der Reaktion an. |
|
 |
Nobby1
Anmeldungsdatum: 19.08.2019
Beiträge: 1553
|
 Nobby1 Verfasst am: 28. Dez 2020 00:00 Titel: Nobby1 Verfasst am: 28. Dez 2020 00:00 Titel: |
 |
|
Die Umrechnung ist gar nicht notwendig. Wenn man ideales Verhalten voraus setzt ist p~ n
pV = nRT . Das Volumen des geschlossenen Behälters ist gleich und const. Die Temperatur wird auch konstant gehalten.R ist die allgemeine Gaskonstante. Also ist der Druck von der Anzahl der Teilchen abhängig.
Die 2 Teilchen stimmen, da Dimethylether in Methan und Formaldehyd zerfällt.
CH3OCH3 => CH4 + CH2O |
|
 |
Jan2000
Gast
|
 Jan2000 Verfasst am: 28. Dez 2020 08:06 Titel: Jan2000 Verfasst am: 28. Dez 2020 08:06 Titel: |
 |
|
Danke für eure Antworten 
Das Edukt zerfällt doch zu CH4 + CO + H2 oder nicht ?
Wenn es zu zwei Teilchen zerfallen würde wäre der Zusammenhang dann:
A/A0=2-p/p0 ?
Aber wie komme ich auf den Zusammenhang für drei Produkte ? |
|
 |
Nobby1
Anmeldungsdatum: 19.08.2019
Beiträge: 1553
|
|
 |
Klimafrosch
Anmeldungsdatum: 12.10.2020
Beiträge: 33
|
 Klimafrosch Verfasst am: 28. Dez 2020 12:03 Titel: Klimafrosch Verfasst am: 28. Dez 2020 12:03 Titel: |
 |
|
Deine Reaktionsgleichung stimmt. Aber du musst auch wissen, ob a) der Dimethylether in großer Menge in großem Überschuss flüssig vorliegt, und b) ob sich CH4, CO und H2 darin lösen können.
Nehmen wir a) an und verwerfen b). ...
Dann sagt dir z.B. ein Druck von 584 Torr ...
420 Torr sind konstant durch den flüssigen Ether vorgegeben. 164 Torr verteilen sich auf 3 Gasmoleküle. ... |
|
 |
Nobby1
Anmeldungsdatum: 19.08.2019
Beiträge: 1553
|
 Nobby1 Verfasst am: 28. Dez 2020 12:08 Titel: Nobby1 Verfasst am: 28. Dez 2020 12:08 Titel: |
 |
|
|
Dimethylether hat einen Siedepunkt von - 24 ° C bei normalen Druck. Das mit der Flüssigkeit kann man denke ich vergessen. |
|
 |
Jan2000
Gast
|
 Jan2000 Verfasst am: 28. Dez 2020 12:19 Titel: Jan2000 Verfasst am: 28. Dez 2020 12:19 Titel: |
 |
|
| Klimafrosch hat Folgendes geschrieben: | Deine Reaktionsgleichung stimmt. Aber du musst auch wissen, ob a) der Dimethylether in großer Menge in großem Überschuss flüssig vorliegt, und b) ob sich CH4, CO und H2 darin lösen können.
Nehmen wir a) an und verwerfen b). ...
Dann sagt dir z.B. ein Druck von 584 Torr ...
420 Torr sind konstant durch den flüssigen Ether vorgegeben. 164 Torr verteilen sich auf 3 Gasmoleküle. ... |
Danke für eure Antworten.
Wie kann ich den jetzt mit dem Wissen daraus das Verhältnis von [A] zu p/p0 definieren. Müsste es dann 3-p/p0 sein ? |
|
 |
Klimafrosch
Anmeldungsdatum: 12.10.2020
Beiträge: 33
|
 Klimafrosch Verfasst am: 28. Dez 2020 14:42 Titel: Klimafrosch Verfasst am: 28. Dez 2020 14:42 Titel: |
 |
|
Deine Frage lässt ja alle Möglichkeiten offen, WAS gemessen worden ist. Ich vermute man hat flüssigen Ether, der einen konstanten Partialdruck von 420 Torr liefert, egal wie viel sich von ihm zersetzt hat.
Der Zerfall des Ethers ist proportional
(p[Torr] - 420)/3
Ohne weitere Angaben über die Temperatur, Flüssigkeitsmenge Ether und Größe des Gasraumes kann man nicht viel sagen. |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5053
|
|
 |
Klimafrosch
Anmeldungsdatum: 12.10.2020
Beiträge: 33
|
 Klimafrosch Verfasst am: 28. Dez 2020 18:02 Titel: Klimafrosch Verfasst am: 28. Dez 2020 18:02 Titel: |
 |
|
Das kann natürlich auch sein. Dann wäre ein Druck von z.B. 584 Torr einem Umsatz proportional von
(584-420) / (-1+3) = 82 |
|
 |
Jan2000
Gast
|
 Jan2000 Verfasst am: 28. Dez 2020 19:09 Titel: Jan2000 Verfasst am: 28. Dez 2020 19:09 Titel: |
 |
|
Danke für eure Antwort bei dem Versuch wird der Ether als Gas eingesetzt.
Also muss ich auf der y-Achse ln((p-p0)/(-1+3)) auftragen ? gegen t ? |
|
 |
Nobby1
Anmeldungsdatum: 19.08.2019
Beiträge: 1553
|
 Nobby1 Verfasst am: 28. Dez 2020 20:57 Titel: Nobby1 Verfasst am: 28. Dez 2020 20:57 Titel: |
 |
|
Das hab ich oben schon geschrieben.
Es ist nicht Diethylether sondern Dimethylether und der ist bei Normalbedingungen gasförmig. |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5053
|
 DrStupid Verfasst am: 28. Dez 2020 21:14 Titel: DrStupid Verfasst am: 28. Dez 2020 21:14 Titel: |
 |
|
| Jan2000 hat Folgendes geschrieben: | | Also muss ich auf der y-Achse ln((p-p0)/(-1+3)) auftragen ? gegen t ? |
Schreib erstmal das Zeitgesetz für eine Reaktion n-ter Ordnung hin. Dann sehen wir weiter. |
|
 |
Jan2000
Gast
|
 Jan2000 Verfasst am: 29. Dez 2020 10:14 Titel: Jan2000 Verfasst am: 29. Dez 2020 10:14 Titel: |
 |
|
Das wäre dann:
1/A^n-1 - 1/A0^n-1 =(n-1)k×t |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5053
|
 DrStupid Verfasst am: 29. Dez 2020 13:42 Titel: DrStupid Verfasst am: 29. Dez 2020 13:42 Titel: |
 |
|
| Jan2000 hat Folgendes geschrieben: | | 1/A^n-1 - 1/A0^n-1 =(n-1)k×t |
In der Form wäre das etwas kompliziert. Ich meinte das differentielle Zeitgesetz
dA/dt = -k·A^n
Was müsste man da logarithmisch auftragen um eine Gerade zu erhalten?
Zuletzt bearbeitet von DrStupid am 29. Dez 2020 22:06, insgesamt 2-mal bearbeitet |
|
 |
Jan2000
Gast
|
 Jan2000 Verfasst am: 29. Dez 2020 15:18 Titel: Jan2000 Verfasst am: 29. Dez 2020 15:18 Titel: |
 |
|
|
Man müsste 1/A^n-1 gegen t auftragen. |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5053
|
 DrStupid Verfasst am: 29. Dez 2020 17:49 Titel: DrStupid Verfasst am: 29. Dez 2020 17:49 Titel: |
 |
|
| Jan2000 hat Folgendes geschrieben: | | Man müsste 1/A^n-1 gegen t auftragen. |
Dazu müsstest Du die Reaktionsordnung n kennen. Die sollst Du aber bestimmen.
Logarithmiere doch mal das differentielle Zeitgesetz. |
|
 |
Jan2000
Gast
|
 Jan2000 Verfasst am: 29. Dez 2020 21:40 Titel: Jan2000 Verfasst am: 29. Dez 2020 21:40 Titel: |
 |
|
ich bin mir nicht sicher aber müsste es dann nicht so lauten:
ln(A) = n*ln(A)+ln(k) |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5053
|
 DrStupid Verfasst am: 29. Dez 2020 22:05 Titel: DrStupid Verfasst am: 29. Dez 2020 22:05 Titel: |
 |
|
So ähnlich:
ln(dA/dt) = n·ln(A) + ln(-k) |
|
 |
Jan2000
Gast
|
 Jan2000 Verfasst am: 30. Dez 2020 08:48 Titel: Jan2000 Verfasst am: 30. Dez 2020 08:48 Titel: |
 |
|
| DrStupid hat Folgendes geschrieben: | So ähnlich:
ln(dA/dt) = n·ln(A) + ln(-k) |
Und wie hilft mir das jetzt weiter ? n, k, und A sind unbekannt, ich brauche ja einen Zusammenhang von p zu A. |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5053
|
 DrStupid Verfasst am: 30. Dez 2020 14:11 Titel: DrStupid Verfasst am: 30. Dez 2020 14:11 Titel: |
 |
|
| Jan2000 hat Folgendes geschrieben: | | ich brauche ja einen Zusammenhang von p zu A. |
Das wurde oben diskutiert. Du hast die Bruttoreaktion A → B + C + D und der Druck ist proportional zur Stoffmenge. Wenn ich eine dimensionslose Variable x mit
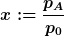
einführe, dann gilt für den Gesamtdruck
 \cdot p_0)
und somit
)
Das Zeitgesetz kannst Du auch mit dieser Variable formulieren. Aus

wird

mit
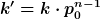
Jetzt solltest Du eigentlich alles haben was Du brauchst. |
|
 |
Jan2000
Gast
|
 Jan2000 Verfasst am: 30. Dez 2020 19:51 Titel: Jan2000 Verfasst am: 30. Dez 2020 19:51 Titel: |
 |
|
Vielen dank für deine Antwort 
k habe ich jetzt durch die Auftragung der Werte von ln(x) gegen t erhalten. Aber wie kann jetzt die Ordnung berechnen? Kann ich jetzt das nicht in die einzelnen Zeitgesetze einsetzen und schauen wo R=1 ist? |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5053
|
 DrStupid Verfasst am: 30. Dez 2020 21:56 Titel: DrStupid Verfasst am: 30. Dez 2020 21:56 Titel: |
 |
|
| Jan2000 hat Folgendes geschrieben: | | k habe ich jetzt durch die Auftragung der Werte von ln(x) gegen t erhalten. |
Das funktioniert nur bei n=1.
| Jan2000 hat Folgendes geschrieben: | | Kann ich jetzt das nicht in die einzelnen Zeitgesetze einsetzen und schauen wo R=1 ist? |
Mit der Auftragung von ln(x) gegen t hast Du das ja im Grunde schon getan. Allerdings ist das nicht sonderlich elegant und funktioniert nur bei ganzzahliger Reaktionsordnung. Versuch doch mal die Auftragung, die ich Dir weiter oben empfohlen habe:
 = n \cdot \ln \left( x \right) + \ln \left( { - k'} \right))
Damit kannst Du Reaktionsordnung und Geschwindigkeitskonstante gleichzeitig bestimmen. Noch besser wäre natürlich eine nichtlineare Regression mit den integralen Zeitgesetzen. |
|
 |
Jan2000
Gast
|
 Jan2000 Verfasst am: 31. Dez 2020 10:53 Titel: Jan2000 Verfasst am: 31. Dez 2020 10:53 Titel: |
 |
|
Vielen dank für deine Antwort 
Leider habe ich nicht ganz verstanden wie ich diesen Ansatz Auftragen soll. Entspricht dann trotzdem noch die Steigung -k ? und woraus lässt sich dann die Ordnung erkennen bzw. berechnen? |
|
 |
DrStupid
Anmeldungsdatum: 07.10.2009
Beiträge: 5053
|
 DrStupid Verfasst am: 31. Dez 2020 15:48 Titel: DrStupid Verfasst am: 31. Dez 2020 15:48 Titel: |
 |
|
| Jan2000 hat Folgendes geschrieben: | | Leider habe ich nicht ganz verstanden wie ich diesen Ansatz Auftragen soll. |
Du leitest x numerisch nach der Zeit ab und trägst dann ln(-dx/dt) gegen ln(x) auf. Wenn es sich um eine Reaktion n-ter Ordnung bezüglich x handelt, dann ergibt das eine Gerade mit der Reaktionsordnung als Anstieg die die vertikale Achse bei ln(k') schneidet. |
|
 |
Jan2000
Gast
|
 Jan2000 Verfasst am: 01. Jan 2021 11:09 Titel: Jan2000 Verfasst am: 01. Jan 2021 11:09 Titel: |
 |
|
Alles klar hab es so aufgetragen wie du es beschrieben hast hat auch gut funktioniert. Vielen, vielen Dank für die Hilfe  |
|
 |
|








