| Autor |
Nachricht |
schokofrosch
Anmeldungsdatum: 10.01.2017
Beiträge: 3
|
 schokofrosch Verfasst am: 10. Jan 2017 10:12 Titel: Eisenstab in Alugefäß schokofrosch Verfasst am: 10. Jan 2017 10:12 Titel: Eisenstab in Alugefäß |
 |
|
Meine Frage:
Ich bräuchte wirklich Hilfe bei dieser Aufgabe, irgendwie stehe ich total auf dem Schlauch. 
Ein Aluminiumdewargefäß der Masse m1=0.5 kg enthält m2=0.118 kg Wasser der Temperatur T1=20°C. Ein Eisenstab der Masse m3=0.2 kg und der Temperatur T2=75 °C wird nun in das Aluminiumgefäß gelegt. Welche Temperatur stellt sich ein, wenn Wärmeverluste zur Umgebung vernachlässigt werden können? cAl=910 J/kg°C, cFe=470 J/kg°C, cH2O=4190 J/kg°C.
Meine Ideen:
Nutzt mir hier die Formel Q=c.m.T etwas? wenn ja, wie soll ich sie hier verwenden, wenn ich keine Endtemperatur gegeben habe?
Ich komm echt nicht weiter, tut mir leid. Ich weiß nicht mal, welche Formel ich verwenden soll  |
|
 |
Myon
Anmeldungsdatum: 04.12.2013
Beiträge: 5870
|
 Myon Verfasst am: 10. Jan 2017 12:48 Titel: Myon Verfasst am: 10. Jan 2017 12:48 Titel: |
 |
|
Hallo schokofrosch
Der wärmere Eisenstab gibt Wärme ab an das Wasser und das Aluminiumgefäss, bis alle drei Körper dieselbe Temperatur T_e angenommen haben. Der Eisenstab gibt dabei die Wärmemenge
)
ab. Mit einer analogen Gleichung für das Wasser und das Aluminiumgefäss (wobei hier natürlich die Temperaturdifferenz T_e-T1 auftritt) bekommst Du die Wärmemengen, welche diese beiden Körper aufnehmen. Die vom Eisen abgegebene Wärmemenge ist gleich der Wärmemenge, welche insgesamt dem Wasser und dem Aluminium zugeführt werden. Damit kannst Du eine Gleichung aufstellen, welche Du nach T_e auflösen kannst. |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 10. Jan 2017 21:05 Titel: franz Verfasst am: 10. Jan 2017 21:05 Titel: |
 |
|
Wer sich keine Rübe über höhere oder tiefere Temperaturen machen möchte, könnte auch die Sicht auf das thermisch abgeschlossene Gesamtsystem einnehmen mit dem trivialen Ansatz 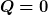 (hier sind Celsiuswerte möglich): (hier sind Celsiuswerte möglich): 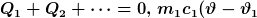+m_2c_2(\vartheta-\vartheta_2)+\cdots=0{.})
Zuletzt bearbeitet von franz am 10. Jan 2017 21:06, insgesamt einmal bearbeitet |
|
 |
schokofrosch
Anmeldungsdatum: 10.01.2017
Beiträge: 3
|
 schokofrosch Verfasst am: 10. Jan 2017 21:06 Titel: schokofrosch Verfasst am: 10. Jan 2017 21:06 Titel: |
 |
|
erst mal vielen Dank für die Hilfe! 
also ich hab das jetzt nach dieser Formel so probiert:
Q = c2*m3*(T2-Te)
Q = 470*0.2*(75-Te)
und dann als nächstes so:
Q = (c1+c3)*(m1+m2)*(Te-20)
Q = (910+4190)*(0,5+0,118)*(Te-20)
und das dann gleichgesetzt, sodass ich nach Te auflösen kann.
ich bekomme dann eine Temperatur von ca. 21,6 Grad heraus.
Ich bin mir aber nicht ganz sicher, ob ich den zweiten Teil so richtig gemacht habe, indem ich einfach die Massen und die Wärmekapazitäten zusammenaddiert habe.  |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 10. Jan 2017 21:14 Titel: franz Verfasst am: 10. Jan 2017 21:14 Titel: |
 |
|
gelöscht
Zuletzt bearbeitet von franz am 10. Jan 2017 23:46, insgesamt 3-mal bearbeitet |
|
 |
schokofrosch
Anmeldungsdatum: 10.01.2017
Beiträge: 3
|
 schokofrosch Verfasst am: 10. Jan 2017 21:34 Titel: schokofrosch Verfasst am: 10. Jan 2017 21:34 Titel: |
 |
|
Hallo franz! 
Ich denke schon, dass die Temperatur von Wasser und Gefäß gleich ist, da keine weiteren Angaben dabei stehen. Ich hab jetzt mal angenommen, das Gefäß habe auch 20 Grad.
also nach deiner Antwort würde es so lauten, damit ich das richtig verstanden hab:
0,5*910*(v-20) + 0.118*4190*(v-20) + 0,2*470*(v-75) = 0
alles ausgerechnet ergibt dann einen Wert von 16,42.
Aber was hab ich mir da jetzt eigentlich genau ausgerechnet? steigt die Temperatur des Wassers um diesen Wert an? |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 10. Jan 2017 23:47 Titel: franz Verfasst am: 10. Jan 2017 23:47 Titel: |
 |
|
Bitte keine Zwischenwerte!!
Ich schreibe durchgängig
1 Aluminium
2 Wasser
3 Eisen
Bei der Gleichung kann man die gesuchte Mischungstemperatur 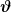 ausklammern und danach umstellen ausklammern und danach umstellen
=m_1c_1\vartheta_1+m_2c_2\vartheta_2+\cdots )
 mit mit 
Ergebnis: Celsius-Temperatur, die über 20 °C liegen muß! |
|
 |
|
|












