| Autor |
Nachricht |
Johann
Anmeldungsdatum: 29.03.2012
Beiträge: 49
|
 Johann Verfasst am: 08. Jun 2012 18:28 Titel: Gasgemischberechnung Johann Verfasst am: 08. Jun 2012 18:28 Titel: Gasgemischberechnung |
 |
|
Ich hoffe ihr könnt mir weiterhelfen, komme irgendwie nicht mehr weiter...
5 kg Methan von 0°C und 0,101325 Mpa werden mit 3 Normkubikmetern eines zweiten Gases (Bestandteile: 21 Vol % Sauerstoff, und 79 Vol % Stickstoff) gemischt.
gesucht:
a) die molaren Massen der Einzelgase (Methan, O2, N2)
b) die speziellen Gaskonstanten der Einzelgase
c) die Massen der EInzelgase
d) die Massenanteile im Gemisch
e) die Gaskonstante des Gemisches
f) die scheinbare molare Masse des Gemisches
also a) und b) habe ich gelöst aber bei c) komm ich nicht weiter...
Ich wollte eigentlich mit der Formel  rechnen. rechnen.
mi steht für Masse des Einzelgases
Mi= molare Masse des Einzelgases
ni= Stoffmenge des Einzelgases
aber hier hätte ich mit ni und mi, 2 Unbekannten...
die 3 Kubikmeter des zweiten Gases setzen sich ja aus 0,63 m³ Sauerstoff und 2,37 m³ Stickstoff zusammen,
kann ich das irgendwie anwenden? |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 08. Jun 2012 18:37 Titel: franz Verfasst am: 08. Jun 2012 18:37 Titel: |
 |
|
Sagt Dir Normbedingungen was?
Wenn ja: p V = n R T -> n -> m
Vielleicht erstmal für Methan |
|
 |
Johann
Anmeldungsdatum: 29.03.2012
Beiträge: 49
|
 Johann Verfasst am: 08. Jun 2012 19:17 Titel: Johann Verfasst am: 08. Jun 2012 19:17 Titel: |
 |
|
| franz hat Folgendes geschrieben: | Sagt Dir Normbedingungen was?
Wenn ja: p V = n R T -> n -> m
Vielleicht erstmal für Methan |
Hi,
ich habs nun so gemacht:
die Masse für Methan steht ja schon =5 kg
für Sauerstoff, erst die Stoffmenge ausgerechnet.... diese ist ja 630 Liter /22,5l /mol...= 28,125 mol
und nun um m auszurechnen...die Stoffmenge mit der molaren Masse multipliziert... = 0,9 kg.
Kann man so machen, oder?
Aber trotzdem würde mich dein weg interessieren... |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 08. Jun 2012 19:29 Titel: franz Verfasst am: 08. Jun 2012 19:29 Titel: |
 |
|
|
Ja, ich übersah, daß etwas gefragt wurde, was schon gegeben war. Aber weiter: Die lustige Bezeichnung "Normkubikmeter" bedeutet Wieviel V(O2) und V(N2)? |
|
 |
Johann
Anmeldungsdatum: 29.03.2012
Beiträge: 49
|
 Johann Verfasst am: 08. Jun 2012 20:00 Titel: Johann Verfasst am: 08. Jun 2012 20:00 Titel: |
 |
|
| franz hat Folgendes geschrieben: | | Ja, ich übersah, daß etwas gefragt wurde, was schon gegeben war. Aber weiter: Die lustige Bezeichnung "Normkubikmeter" bedeutet Wieviel V(O2) und V(N2)? |
V(O2)= 0,63 m³
V(N2) = 2,37 m³ |
|
 |
Johann
Anmeldungsdatum: 29.03.2012
Beiträge: 49
|
 Johann Verfasst am: 08. Jun 2012 20:27 Titel: Johann Verfasst am: 08. Jun 2012 20:27 Titel: |
 |
|
Ich habe mal ne andere Frage zu einer anderen Aufgabe, wollte nun kein neues Thema aufmachen.
Undzwar, wie kann man aus gegeben Masseanteilen, die gesamte molare Molare Masse errechnen?
Stehe irgendwie aufm Schlauch...
mir fehlen die Stoffmengenanteile, denn es gilt ja 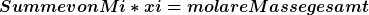 |
|
 |
franz
Anmeldungsdatum: 04.04.2009
Beiträge: 11583
|
 franz Verfasst am: 08. Jun 2012 23:19 Titel: franz Verfasst am: 08. Jun 2012 23:19 Titel: |
 |
|
| Johann hat Folgendes geschrieben: | | Ich habe mal ne andere Frage zu einer anderen Aufgabe |
Bitte neues Thema! |
|
 |
|
|
