| Autor |
Nachricht |
exp
Gast
|
 exp Verfasst am: 01. Apr 2010 17:00 Titel: Expansionsarbeit exp Verfasst am: 01. Apr 2010 17:00 Titel: Expansionsarbeit |
 |
|
Hallo, ich hoffe ihr könnt mir helfen.
Es geht um folgende Aufgabe:
| Zitat: | In einen Volumen  befinden sich befinden sich  Methan bei Methan bei 
1. Berechnen Sie die verrichtet Arbeit, wenn das Gas isotherm gegen einen konstanten Druck von  expandiert und dabei sein Volumen um expandiert und dabei sein Volumen um  vergrößert. vergrößert.
2. Berechnen Sie die Arbeit, die bei der gleichen Expansion unter reversiblen Bedingungen verrichtet wurde.
3. Berechnen Sie für den reversiblen Fall ebenfalls die Änderung der inneren Energie 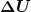 , der Enthalpie , der Enthalpie , sowie die zuzuführende Wärme , sowie die zuzuführende Wärme 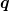 . . |
Meine Ideen bzw. Lösungsvorschläge:
1.)

2.) Damit es reversibel ist, muss der externe Druck immer dem internen Druck entsprechen, der sich über das ideale Gasgesetz berechnen lässt:
 = - 167,45 J)
Wobei ich die Stoffmenge zu 0,28 mol bestimmt habe.
Bis hierhin bin ich mir relativ sicher, dass meine Rechnung stimmt. Könnt ihr mir das bestätigen ?
Bei der Aufgabe 3, bin ich mir relativ unsicher und kann die jeweiligen Größen auch nicht berechnen.
Meine Idee:

Damit habe ich aber zwei Unbekannte...
Kann mir jmd. helfen ? |
|
 |
kleinschreiber
Gast
|
 kleinschreiber Verfasst am: 01. Apr 2010 23:22 Titel: kleinschreiber Verfasst am: 01. Apr 2010 23:22 Titel: |
 |
|
hallo
zu 1
du mußt doch die volumenänderungsarbeit berechnen
also die fläche unter der isothermen
dazu brauchst du die spezifische gaskonstante von methan |
|
 |
exp
Gast
|
 exp Verfasst am: 02. Apr 2010 13:16 Titel: exp Verfasst am: 02. Apr 2010 13:16 Titel: |
 |
|
|
Damit kann ich jetzt nicht recht wenig anfangen, kannst du das genauer erklären ? Also wie genau und warum ? |
|
 |
exp
Gast
|
 exp Verfasst am: 03. Apr 2010 12:12 Titel: exp Verfasst am: 03. Apr 2010 12:12 Titel: |
 |
|
Kann mir wirklich niemand helfen ?  |
|
 |
Anders
Gast
|
 Anders Verfasst am: 04. Apr 2010 10:52 Titel: Anders Verfasst am: 04. Apr 2010 10:52 Titel: |
 |
|
Die Volumensänderungsarbeit ist das was du bei 2. gerechnet hast
167J.Davon gehen 85.8J an ein äußeres Medium(Luft) und 81.2J an einen Kolben
Eine isotherme Zustandsänderung ist ohne Reibung reversibel;deshalb verstehe ich die zweite Frage nicht |
|
 |
exp
Gast
|
 exp Verfasst am: 04. Apr 2010 11:51 Titel: exp Verfasst am: 04. Apr 2010 11:51 Titel: |
 |
|
|
Scheinbar hast du noch weniger Ahnung als ich, dennoch Danke für deine Antwort. |
|
 |
|
|