| Autor |
Nachricht |
Kr0ete
Anmeldungsdatum: 30.01.2008
Beiträge: 8
|
 Kr0ete Verfasst am: 30. Jan 2008 19:46 Titel: Starrer, wärmeisolierter Behälter Kr0ete Verfasst am: 30. Jan 2008 19:46 Titel: Starrer, wärmeisolierter Behälter |
 |
|
Hi @ all
vielleicht kann mir hier wer helfen und mir sagen wie b,c,d geht bei der Aufgabe ich raff es grad überhaupt nicht. Aber die a hab ich raus bekommen.
Besten Dank Kr0ete
| Beschreibung: |
|
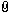
Download |
| Dateiname: |
aufgabe.JPG |
| Dateigröße: |
61.24 KB |
| Heruntergeladen: |
1058 mal |
|
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 30. Jan 2008 20:07 Titel: dermarkus Verfasst am: 30. Jan 2008 20:07 Titel: |
 |
|
Sag doch am besten mal, was du schon dazu weißt und was du bisher dazu schon zusammengestellt, gefunden und überlegt hast.
Mit welcher Gleichung hast du die a) gerechnet? Könnte dir diese Gleichung auch für die b) nützlich sein?
|
|
 |
Kr0ete
Anmeldungsdatum: 30.01.2008
Beiträge: 8
|
 Kr0ete Verfasst am: 30. Jan 2008 20:19 Titel: Kr0ete Verfasst am: 30. Jan 2008 20:19 Titel: |
 |
|
Hi
m=p*V/R*T = 1,15g
Für die b dacht ich an isentrope Zustandsänderung da reversibel.
mit k(isentropenexp)=cv+R/cv= 1,4 über die gleichung T2/T1=(V1/V2)^(k-1)
Hab ich versucht die temp T2 auszurechnen.
V1 ist 0,001m^3 V2 ist 0,0015m^3
Aber leider komm ich nicht auf das angegeben Ergebnis von T2(rechts)=398,15
|
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 30. Jan 2008 20:26 Titel: dermarkus Verfasst am: 30. Jan 2008 20:26 Titel: |
 |
|
Magst du erstmal alle Informationen sammeln und hier zusammenstellen, die du über die Luft im einen Teil des Behälters und über das Luft im anderen Teil des Behälters hast?
Eine fertige Gleichung kannst du ja erst dann verwenden, wenn du weißt, ob sie zu dieser Aufgabe passt und was konkret die Variablenbezeichungen darin bedeuten sollen.
|
|
 |
Kr0ete
Anmeldungsdatum: 30.01.2008
Beiträge: 8
|
 Kr0ete Verfasst am: 30. Jan 2008 20:45 Titel: Kr0ete Verfasst am: 30. Jan 2008 20:45 Titel: |
 |
|
Hi
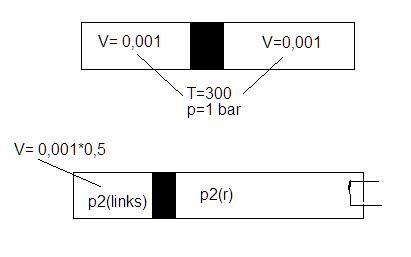
Hab mir des in etwa so vorgestellt
Hab eine Volumenänderung, druckänderung, Temperaturänderung
| Beschreibung: |
|
| Dateigröße: |
10.67 KB |
| Angeschaut: |
2042 mal |
|
|
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 30. Jan 2008 20:52 Titel: dermarkus Verfasst am: 30. Jan 2008 20:52 Titel: |
 |
|
|
Einverstanden, was bedeutet das konkret für die Drücke, Volumina und Temperaturen nach dem Erwärmen der einen Seite? Schreib mal alle Werte und alle Gleichungen auf, die du damit schon weißt!
|
|
 |
Kr0ete
Anmeldungsdatum: 30.01.2008
Beiträge: 8
|
 Kr0ete Verfasst am: 30. Jan 2008 21:04 Titel: Kr0ete Verfasst am: 30. Jan 2008 21:04 Titel: |
 |
|
mit k(isentropenexp)=cv+R/cv= 1,4
T2/T1=(V1/V2)^(k-1) für rechts oder links dacht ich mir
was anderes fällt mir nicht ein. Oder ich verstehe irgendwas grundsätzliches nicht.
|
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 30. Jan 2008 21:27 Titel: dermarkus Verfasst am: 30. Jan 2008 21:27 Titel: |
 |
|
Ich denke, für die b) denkst du viel zu kompliziert.
Wie groß ist denn die Temperatur nach dem Zusammendrücken im linken Teil?
Kannst du dann schon ausrechnen, wie groß der Druck im linken Teil dann sein muss?
// edit: Möglich, dass es hier bisher noch ich war, der zu einfach gedacht hatte. Vielleicht ist der Vorschlag unten in meinem nächsten Beitrag hilfreicher.
Zuletzt bearbeitet von dermarkus am 30. Jan 2008 21:36, insgesamt 2-mal bearbeitet |
|
 |
Kr0ete
Anmeldungsdatum: 30.01.2008
Beiträge: 8
|
 Kr0ete Verfasst am: 30. Jan 2008 21:27 Titel: Kr0ete Verfasst am: 30. Jan 2008 21:27 Titel: |
 |
|
hab leider keine ahnung wie hoch die temperatur links ist ich weiss ja nur dass sich V,T,p verändern V hab ich laut angabe geben. ich könnte also formeln für isentrop benutzen um auf T2 zu kommen.
Aber ich hab echt keine Ahnung.
Das prob hab ich höfters dass ich zu kompliziert denke ka warum.
|
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 30. Jan 2008 21:33 Titel: dermarkus Verfasst am: 30. Jan 2008 21:33 Titel: |
 |
|
Wie wäre es mit folgender Idee:
Stelle die Gleichungen für die Zustandsänderung links und die Zustandsänderung rechts erst einmal allgemein auf.
Und dann verwendest du die Information, dass der Druck links nachher gleich groß sein muss wie der Druck rechts nachher (denn sonst würde sich die Zwischenwand ja noch woandershin weiterverschieben).
Welches System von zwei Gleichungen bekommst du damit?
|
|
 |
Kr0ete
Anmeldungsdatum: 30.01.2008
Beiträge: 8
|
 Kr0ete Verfasst am: 30. Jan 2008 21:57 Titel: Kr0ete Verfasst am: 30. Jan 2008 21:57 Titel: |
 |
|
Ich würde mal sagen es ist dann isobar.
Wobei ich auch nicht aufs ergebniss komme.
p1*V1/T1=p2*V2/T2 << für recht, selbiges für links
2 ist der zustand nach der erwährmung
p2(links)=p2(rechts)
T1(r)=T1(l)
V1(r)=V1(l)
eigendlich sollt ich ja dann drauf kommen so wie ich dich verstanden habe aber ich tus nicht.
Oh mann da wirds nix mit da thermoprüfung am sammstag  
|
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 31. Jan 2008 11:27 Titel: dermarkus Verfasst am: 31. Jan 2008 11:27 Titel: |
 |
|
| Kr0ete hat Folgendes geschrieben: | Ich würde mal sagen es ist dann isobar.
|
Vorsicht, mit isobar meint man normalerweise ja eine isobare Zustandsänderung, bei der der Druck konstant bleibt. Und wir erwarten hier ja weder p1L=p2L links noch p1R=p2R. Sondern wir haben einfach nur festgestellt, dass p2L=p2R=p2 sein wird.
// edit: Hier habe ich einen nicht hilfreichen und irreführenden Teil gelöscht. //
Welche der drei Gleichungen für die adiabatische Zustandsänderung (kennst du die auch unter dem Namen Poissonsche Gleichungen oder Poisson-Gleichungen?) brauchst du also hier, um das p2 in der linken Kammer ausrechnen zu können? Welche ist die mit p und V drin?
------------------------------------------
| Zitat: |
[...] das angegeben Ergebnis von T2(rechts)=398,15
|
Du scheinst schon (von einer Musterlösung/Aufgabenbesprechung) Zwischenergebnisse zu haben, die dir für diese Aufgabe angegeben wurden, aber du hast hier vergessen, dazuzuschreiben, in welcher Einheit (Kelvin, Grad Celsius, hunderstel T_1, ... ?) sie gemeint sein sollen. Magst du mal die Zwischenergebnisse, mit denen du deine Rechnungen vergleichst, samt vollständigen Einheiten dabei angeben?
Zuletzt bearbeitet von dermarkus am 31. Jan 2008 12:41, insgesamt einmal bearbeitet |
|
 |
Kr0ete
Anmeldungsdatum: 30.01.2008
Beiträge: 8
|
 Kr0ete Verfasst am: 31. Jan 2008 11:36 Titel: Kr0ete Verfasst am: 31. Jan 2008 11:36 Titel: |
 |
|
Hi
nein Poissonsche Gleichungen oder Poisson-Gleichungen kenne ich so rein der namensgebung nicht.
Hab die aufgabe mit Isentropen formeln probiert aber leider bin ich nicht auf die ergebnisse gekommen. Evtl übersteigt die aufgabe auch mein wissen. Weiss es nicht genau, da ich die aufgabe im internet gefunden habe und ich sie nicht von mienem prof bekommen habe.
Unten sind die Ergebnisse.
| Beschreibung: |
|
| Dateigröße: |
9.22 KB |
| Angeschaut: |
1929 mal |
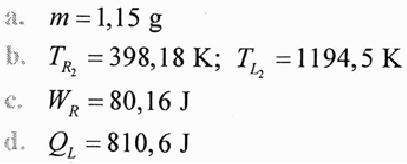
|
|
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 31. Jan 2008 13:03 Titel: dermarkus Verfasst am: 31. Jan 2008 13:03 Titel: |
 |
|
Ah, danke, damit wird das ganze für mich viel einfacher 
Vorneweg:
* Das, was bei dir die linke Seite war, ist in der Lösung die rechte und umgekehrt.
* Das, was du mit den Isentropen-Formeln meinst, dürfte genau dasselbe sein wie das, was ich als Poisson-Gleichungen kenne, nämlich:



Wenn du dir alle Angaben, die du kennst, mal für deine linke Seite aufschreibst, dann hast du:



Dann siehst du, dass du schon alle nötigen Informationen beieinander hast, um mit der ersten der drei Poissonschen Formeln den Druck  auf deiner linken Seite ausrechnen zu können (obwohl du ihn für die Lösung der Aufgabe gar nicht brauchst), und mit der zweiten der drei Poissonschen Formeln die gesuchte Temperatur auf deiner linken Seite ausrechnen zu können (obwohl du ihn für die Lösung der Aufgabe gar nicht brauchst), und mit der zweiten der drei Poissonschen Formeln die gesuchte Temperatur  . .
Wenn du jetzt noch verwendest, dass

mit  , ,
dann bekommst du schnell heraus, dass die Temperatur rechts dreimal höher sein muss als die links, damit hast du dann auch gleich schon die andere der beiden Temperaturen.
--------------------
Dabei habe ich rechts und links immer jeweils so bezeichnet wie du in deiner Skizze. Magst du das mal nachrechnen, um vor der Prüfung noch ein schönes Erfolgserlebnis zu haben? 
|
|
 |
Kr0ete
Anmeldungsdatum: 30.01.2008
Beiträge: 8
|
 Kr0ete Verfasst am: 31. Jan 2008 15:04 Titel: Kr0ete Verfasst am: 31. Jan 2008 15:04 Titel: |
 |
|
Hi
Danke für die Antwort.
Hab meinen fehler gefunden hab mit  und nicht und nicht  . .
Deshlab hab ich auch immer für  raus bekommen. raus bekommen.
Was dann auch wieder ein anderes  zur folge hatte. zur folge hatte.
Naja son misst dumme aufgabe.
Danke nochmal
|
|
 |
dermarkus
Administrator

Anmeldungsdatum: 12.01.2006
Beiträge: 14788
|
 dermarkus Verfasst am: 31. Jan 2008 16:23 Titel: dermarkus Verfasst am: 31. Jan 2008 16:23 Titel: |
 |
|
Und wegen diesem kleinen Rundungsfehler hast du dir die ganze Zeit den Kopf zerbrochen?
Da hätten wir uns einiges an Rätselraten sparen können, wenn du deine Rechnung gleich bis zu deinem Ergebnis hier aufgeschrieben hättest, anstatt dir zu sagen "Das schreibe ich lieber gar nicht erst im Forum auf, denn das stimmt ja nicht ganz genau mit der Musterlösung überein" 
|
|
 |
|